En Çok Okunanlar
Özet
Stenotrophomonas maltophilia, infektif endokardit (İE)’in nadir bir etkenidir. Biyofilm oluşturma yeteneği ve antibiyotik direnci nedeniyle tedavisi güç olan fırsatçı bir patojendir. Tedavisinde trimetoprim-sülfametoksazol ve kinolonlar ilk seçenekler olmakla birlikte uzun tedavi süresi yan etkileri de beraberinde getirebilmektedir. Hastalığın cerrahi müdahale ve mortalite riski de yüksektir. Protez kapak cerrahisi öyküsü, santral venöz kateter varlığı, geniş spektrumlu antibiyotik kullanımı S. maltophilia infeksiyonu için bilinen risk faktörleridir. Bu yazıda, protez kapak cerrahi öyküsü olmayan, kalıcı kateterden hemodiyalize giren bir hastada gelişen ve başarıyla tedavi edilen bir doğal kapak endokarditi olgusu, tedavide yaşanan güçlüklere dikkat çekilerek deneyim paylaşımı amacıyla güncel literatür eşliğinde sunuldu.
GİRİŞ
Protez kapak cerrahisi, intravasküler kateter kullanımı, immünsüpresif hastalardaki artış gibi nedenlerle, HACEK dışı Gram-negatif bakterilere bağlı gelişen infektif endokardit (İE) olguları artmaktadır (1). Hemodiyaliz hastaları, vasküler kateterler nedeniyle kan dolaşımı infeksiyonu (KDİ) açısından yüksek risk altındadır. Bu hastalarda gelişen Gram-negatif KDİ oranları artış eğilimindedir (2). Kronik böbrek yetmezliği varlığında ise İE’de mortalite oranı daha yüksektir (3). Bu yazıda, bir hemodiyaliz hastasında kateter ilişkili bakteriyemi sonrası gelişen Stenotrophomonas maltophilia doğal kapak endokarditi sunuldu.
OLGU
Altmış beş yaşında erkek hasta acil servise dört gündür devam eden, özellikle diyaliz sonrası 38.5⁰C’ı aşan ateş yüksekliği şikayetiyle başvurdu. Hipertansiyona sekonder son dönem kronik böbrek yetmezliği nedeniyle bir yıldır subklavyendeki kalıcı diyaliz kateterinden düzenli hemodiyaliz almakta olan hasta, diyaliz merkezi tarafından ateş ve kateter disfonksiyonu nedeniyle yönlendirilmişti. Yapılan fizik muayenede kateter çevresinde akıntı, eritem veya endürasyon saptanmadı. Gövde, ekstremite ve tırnak yataklarında döküntü izlenmedi. Patolojik üfürüm duyulmadı, kalp sesleri ritmikti. Diğer sistem muayeneleri olağandı.
Laboratuvar tetkiklerinde trombositopeni [75 000/mm3; referans aralığı (RA):150 000–450 000/mm3] ve C-reaktif protein (CRP) yüksekliği (19.8 mg/dl; RA <0.5 mg/dl) mevcuttu. Kateter kaynaklı bakteriyemi ön tanısıyla periferik venlerden ve kateterden kan kültürü örnekleri alındı; ampirik olarak meropenem (500 mg × 1/gün, İV) ve daptomisin (48 saatte bir 1× 6 mg/kg, İV) tedavisine başlandı. Kalıcı diyaliz kateteri teknik nedenlerle hemen çekilemedi ancak geçici bir kateter takılarak kullanımı sonlandırıldı.
Kateterden alınan kan kültürü, inkübasyonun 17. saatinde, periferik venden alınan örnek ise 20. saatte üreme sinyali verdi; Gram boyalı mikroskobik incelemede Gram-negatif basiller görüldü. Hastanın yatışının dördüncü gününde iki kültürde de MALDI-TOF MS (Matrix-Assisted Laser Desorption/Ionization Time-of-Flight Mass Spectrometry; Bruker Daltonics, Bremen, Almanya) ile S. maltophilia tanımlanması üzerine tedavi piperasilin-tazobaktam (3 × 2.25 g, İV) ve trimetoprim-sülfametoksazol (TMP-SMX; 320/1600 mg/gün, İV) olarak değiştirildi. Yatışın beşinci, antibiyotik değişikliğinden iki gün sonra alınan kontrol kültüründe de S. maltophilia üredi. Kalıcı diyaliz kateteri ancak sekizinci günde çekilebildi. Kateter ucunun semi-kantitatif (Maki) ve sıvı besiyeri (broth) yöntemleriyle yapılan mikrobiyolojik incelemesinde de S. maltophilia üremesi saptandı.
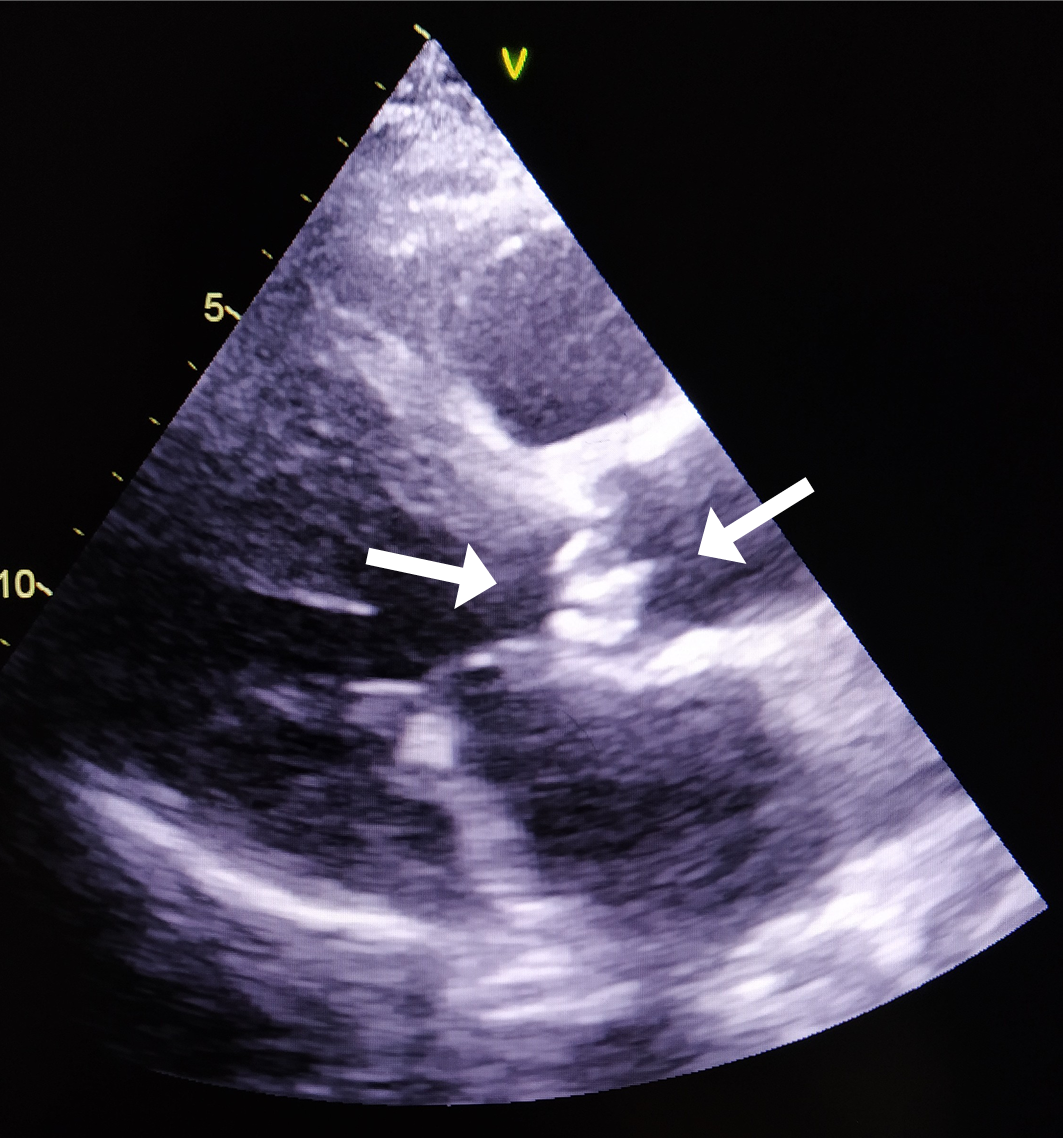
Resim 1a. Aort Kapağı Üzerinde Oklarla Gösterilen Vejetasyonun Transtorasik Ekokardiyografi (TTE) Görüntüsü
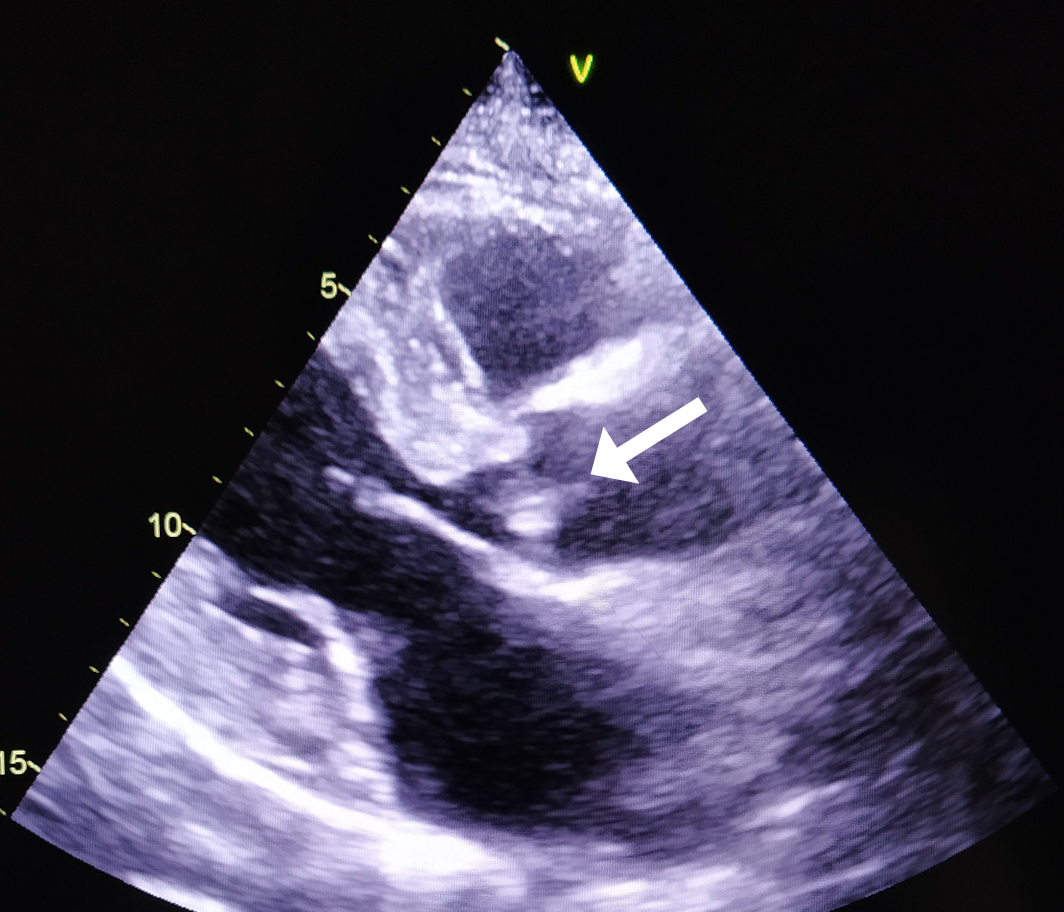
Resim 1b. Aort Kapağı Üzerinde 0.9 × 0.6 cm Boyutlarında Ölçülen, Okla Gösterilen Vejetasyonun Transtorasik Ekokardiyografi (TTE) Görüntüsü
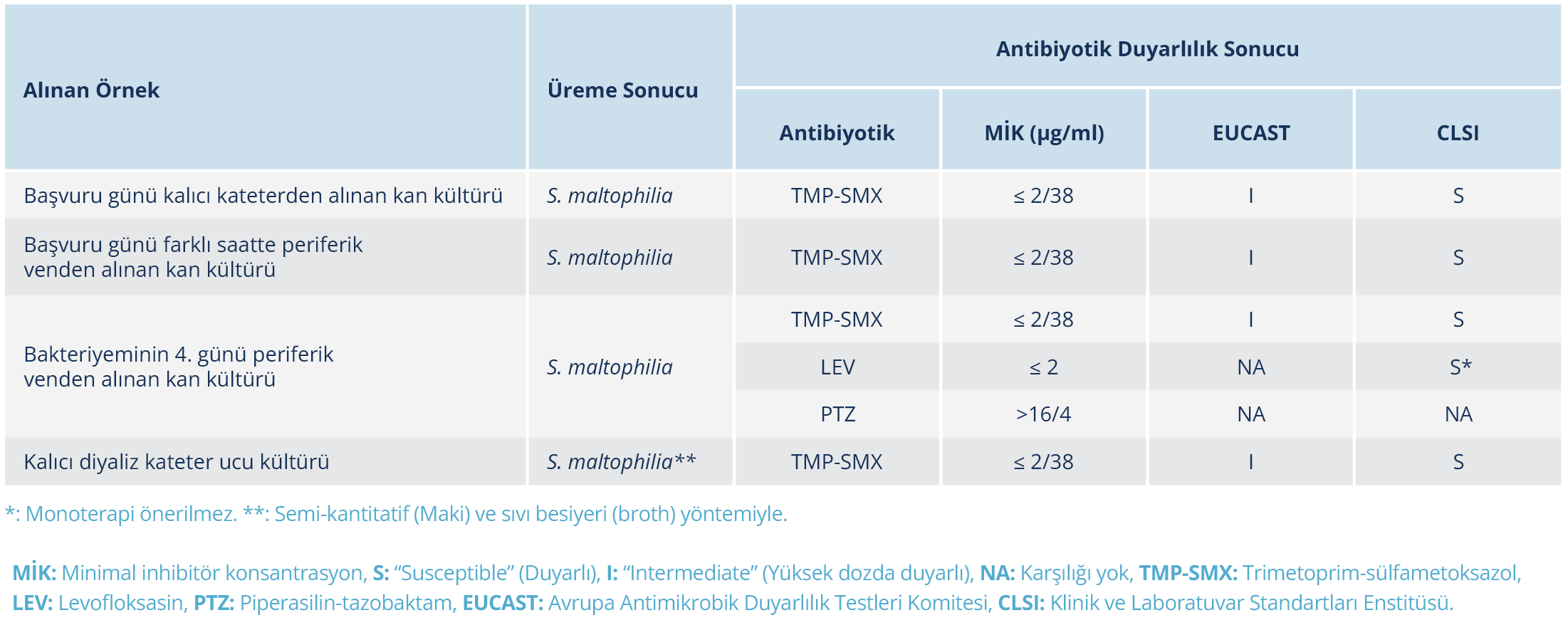
Üç farklı zamanda alınan üç set kan kültüründe aynı etkenin üremesi, kalıcı kateterin geç çekilebilmesi ve aort odağında yeni gelişen bir üfürüm duyulması nedeniyle bakteriyeminin 11. gününde yapılan transtorasik ekokardiyografi (TTE)’de aort kapakta ventrikül tarafında 0.9 × 0.6 cm boyutlarında vejetasyon saptandı (Tablo 1, Resim 1a-1b). Kültür ve TTE sonuçlarıyla iki majör kriteri sağlayan hastaya S. maltophilia endokarditi tanısı kondu.
Antibiyotik duyarlılık sonuçları (Tablo 2), literatür ve kılavuzlar dikkate alınarak piperasilin-tazobaktam kesildi; tedavi levofloksasin (48 saatte bir 750 mg, İV) ve TMP-SMX (320/1600 mg/gün, İV) olarak güncellendi. TMP-SMX’in dokuzuncu, bakteriyeminin 12. gününde ilk kan kültürü negatifliği görüldü. Transtorasik ekokardiyografiden bir hafta sonra yapılan transözofageal ekokardiyografi (TÖE)’de vejetasyonun 0.6 × 0.4 cm boyutunda sürdüğü doğrulandı.
İlerleyen haftalarda, özellikle uzamış TMP-SMX kullanımına bağlı olabilecek hiperpotasemi ve hiponatremi gibi elektrolit bozuklukları, en erken ve uzun süre trombositer seride olmak üzere her üç seride kemik iliği süpresyonu ve şiddetli bulantı-kusma gibi yan etkiler gelişti. Bulantı şikayetine yönelik ondansetron ve metoklopramid ile semptomatik tedavi uygulandı; hiperpotasemi yönetimi için tedaviye polistiren sülfonat kalsiyum tuzu eklendi ve hemodiyaliz sıklığı artırıldı. İç Hastalıkları bölümü tarafından önerilen bu destek yaklaşımları titizlikle uygulandı.
Başvuru anındaki trombositopeni KDİ ile ilişkili olarak değerlendirildi ve uygun antibiyotik tedavisi sonrası ilk haftalarda trombosit değerlerinde yükselme gözlendi. Öte yandan, TMP-SMX tedavisinin özellikle dördüncü haftasından sonra trombosit değerlerinde tekrardan düşüş (100 000/mm³ altı) gözlendi ve diğer serilerde de sitopeni gelişti. Hematoloji bölümü tarafından periferik yayma ile yapılan değerlendirmede, trombosit sayısı hemogram ile uyumlu bulundu ve trombositopeni öncelikle uzamış TMP-SMX kullanımı ile ilişkili olarak değerlendirildi. Hastanın takibinde trombosit transfüzyonu gerektirecek düzeyde bir trombosit düşüklüğü gelişmedi; ancak son tedavi haftasında anemiye yönelik eritrosit transfüzyonları uygulandı.
Trimetoprim-sülfametoksazol dozu, tedavinin son haftasında semptomatik desteğe rağmen devam eden şiddetli bulantı ve sitopeniler nedeniyle 160/800 mg/gün şeklinde azaltıldı. Levofloksasin tedavisine ise aynı dozdan devam edildi. Antibiyogram sonuçlarına dayanılarak duyarlı ve erişilebilir alternatif bir ajan bulunmadığından antibiyotik revizyonu düşünülmedi ve tedavi sürdürüldü.
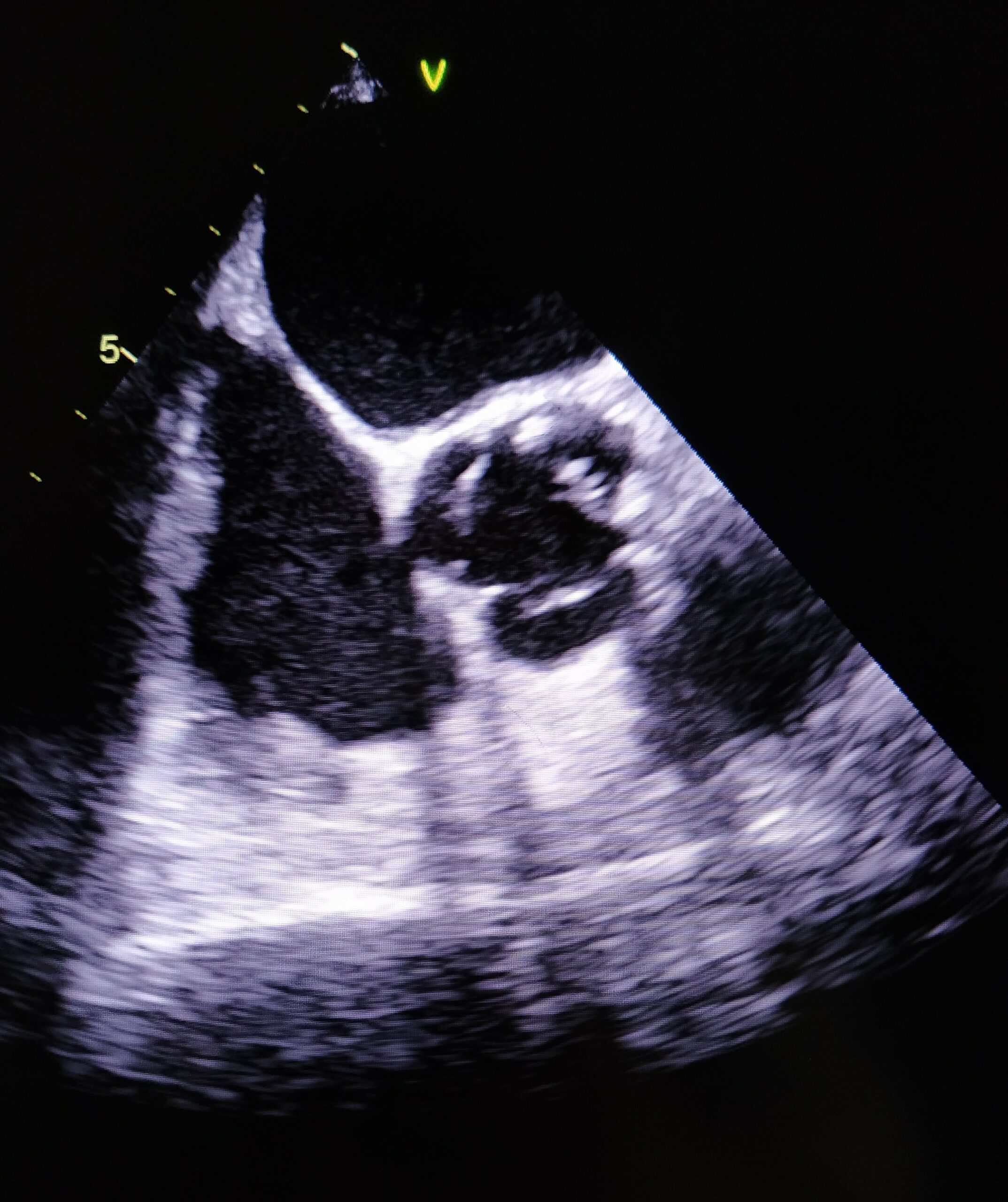
Resim 2. Tedavi Sonrası Yapılan Transözofageal Ekokardiyografide (TÖE) Vejetatif Lezyon Saptanmayan Görüntü
Tedavinin 42. gününde TÖE’de vejetasyonun kaybolduğu saptandı (Tablo 2, Resim 2). Bunun üzerine TMP-SMX 6 haftaya, levofloksasin ise 5 haftaya tamamlanarak kesildi. Elektrolit dengesi düzelen hasta yatışının 53. gününde şifa ile taburcu edildi.
İRDELEME
Stenotrophomonas maltophilia aerobik, hareketli, Gram-negatif bir basildir; hastane ortamında nebülizatörlerde, santral kateterlerde, antiseptiklerde, diyalizat sıvılarında ve su sistemlerinde kolonize olabilmektedir. Gelişmiş biyofilm oluşturma yeteneği ve bazı antibiyotiklere intrensek dirençli olması, onu zor başa çıkılabilen bir tehdit haline getirmektedir (4). Önceleri nadir bir etkenken günümüzde sık karşılaşılan non-fermentatif Gram-negatif fırsatçı patojenlerdendir. Pnömoni, KDİ, üriner sistem infeksiyonu ve nadiren de İE’ye neden olabilir (5). Literatürde diyaliz hastalarında, periton diyalizi alan bir hastada S. maltophilia’ya bağlı peritonit ve olgumuzda olduğu gibi diyaliz kateteri ilişkili KDİ’ler bildirilmiştir (6–8).
İkiyüz elli bir hemodiyaliz hastasının değerlendirildiği bir çalışmada hastaların %17.5’inde KDİ, %3.9’unda ise rekürren KDİ geliştiği; etkenlerin %46.3’ünün Gram-negatif, %31.4’ünün ise dirençli bakteriler olduğu ve kateterden hemodiyalize girmenin KDİ riskini anlamlı şekilde artırdığı bildirilmiştir (2).
Stenotrophomonas maltophilia infeksiyonları için uzamış hastane veya yoğun bakım yatışı, karbapenemler gibi geniş spektrumlu antibiyotiklerin uzun süreli kullanımı, santral venöz kateter varlığı ve yakın zamanlı cerrahi girişim öyküsü bilinen risk faktörlerindendir. Kan dolaşımı infeksiyonu olgularının incelendiği çalışmalarda, uygun ampirik antibiyotik tedavisi, erken dönemde uygun antibiyotik revizyonu yapılması ve infekte santral kateterin çekilmesi azalmış mortalite ile ilişkili bulunmuştur (9,10).
Stenotrophomonas maltophilia İE’nin nadir bir nedenidir; literatürde geçen 50’ye yakın İE olgusu içinde 44 olgunun 28’inin (%62.2) protez kapak, 16’sının (%35.5) ise doğal kapak endokarditi olduğu bildirilmiştir (11–13). Yarıya yakınında yakın zamanda kardiyovasküler girişim öyküsü olup intravenöz madde kullanımı, santral venöz kateter ve yapısal/romatolojik kalp hastalığı kaydedilen diğer predispozan faktörlerdir (11). Santral kateter ve fistül yeri infeksiyonuna bağlı gelişen endokardit olgularının tamamının olgumuzdaki gibi doğal kapak endokarditi olması dikkat çekicidir (11–13).
İnfektif endokardit kılavuzlarında, “tipik” veya güncellenmiş modifiye Duke kriterlerinde “intrakardiyak yabancı cisim varlığında tipik” kabul edilen bakteriler içerisinde S. maltophilia yer almamaktadır. Kan dolaşımı infeksiyonu ile başvuran hastaların kateter giriş yerlerinde belirgin infeksiyon bulgusu ve başlangıçta üfürümü olmayabilir. Bu nedenle klinik şüphe ve takipte dikkatli fizik muayene eksikliğinde İE tanısının gözden kaçması olasıdır. Ateş ve yeni gelişen üfürüm İE’de en sık görülen bulgulardır (3). Olgumuzda da ateş yüksekliği, yeni gelişen üfürüm ve kan kültüründe üremenin devam etmesi, İE açısından tipik olmayan bir etken üremesine rağmen klinik şüphe yarattı ve bizi tanısal sürece götürdü.
İnfektif endokardit rehberlerinde önerilen standart bir antibiyotik rejiminin bulunmaması ve S. maltophilia’nın gelişmiş direnç mekanizmaları, tedavide karşılaşılan önemli güçlüklerdir (14,15). Ayrıca Avrupa Antimikrobiyal Duyarlılık Testi Komitesi (European Committee on Antimicrobial Susceptibility Testing, EUCAST) Rehberi’nde çoğu antibiyotik için referans alınabilecek bir duyarlılık eşiği (breakpoint) olmaması da klinik değerlendirmeyi zorlaştırmaktadır (16). Bu durumda Klinik ve Laboratuvar Standartları Enstitüsü (Clinical and Laboratory Standards Institute, CLSI) Rehberi yol gösterici olabilir (17). Güncel çalışmalarda TMP-SMX duyarlılığı %93, levofloksasin duyarlılığı %88, seftazidim duyarlılığı ise %35 olarak bildirilmiştir (9). Ülkemizden yapılan çok merkezli bir çalışmada ise TMP-SMX direnci %8.8 ve levofloksasin direnci %3.1 olarak bildirilmiş olup çalışmanın yapıldığı yıllar içinde TMP-SMX direncinde istatistiksel olarak anlamlı bir artış saptanmıştır (%2.1’den %10.4’e) (10). Yine ülkemizde yapılan ancak daha eski tarihli bir diğer çalışmada da TMP-SMX direnci %10’unda altında bildirilmiş; seftazidim + moksifloksasin kombinasyonunun in vitro sinerjik etkinliği gösterilerek alternatif seçenekler arasında yer alabileceği vurgulanmıştır (18).
Trimetoprim-sülfametoksazol, minosiklin veya tigesiklin, sefiderokol ve levofloksasin güncel rehberlerde ilk seçeneklerdir; ağır seyirli infeksiyonlarda ise kombinasyon tedavileri önerilmektedir (19). Yanıt alınamayan ve yan etki gelişen olgularda alternatifler seftazidim-avibaktam ve aztreonamdır (20). Kloramfenikol, gentamisin, tikarsilin, seftazidim, piperasilin içeren çeşitli kombinasyonlar daha eski olguların tedavisinde kullanılmış (11) olmakla birlikte günümüzde en sık levofloksasin ve TMP-SMX kullanılmaktadır. Bazı olgularda TMP-SMX’e bağlı gelişen dirençli hiperpotasemi nedeniyle alternatif tedaviler denenmiştir (12,13). Örneğin bir olguda TMP-SMX kesildikten sonra seftazidim ve minosiklin kombinasyonuyla başarılı olunduğu bildirilmiştir (14).
Uzamış TMP-SMX kullanımına bağlı olarak yan etkiler gelişmesi durumunda alternatiflerden olan minosiklin, sefiderokol, aztreonam ülkemizde erişilebilir değildir; seftazidim-avibaktam içinse yoğun bakımda yatış koşulu aranmaktadır. Bu nedenle antibiyotik revizyonu kararı özellikle endokardit gibi ciddi seyirli infeksiyonlarda güçtür. Trimetoprim-sülfametoksazol kullanımı sonrası Stevens-Johnson sendromu, toksik epidermal nekroliz (TEN), eozinofili ve sistemik semptomlarla seyreden ilaç döküntüsü sendromu (drug reaction with eosinophilia and systemic symptoms, DRESS) gibi ciddi seyirli aşırı duyarlılık reaksiyonlarının varlığında antibiyotik tedavisi mutlaka kesilmelidir (21). Fakat bu ciddi yan etkiler genellikle ilk haftalarda daha sık gözlenmektedir (22). Bunların yanı sıra aseptik menenjit, fulminan hepatit, akut interstisiyel nefrit, agranülositoz ve ilaç ilişkili immün trombositopeni ve destek tedaviye yanıtsız elektrolit bozuklukları da antibiyotik tedavisine devam edilemeyecek diğer ciddi advers olaylar arasında sayılabilir (21–23). Olgumuz gibi destek tedaviye yanıt alınan, ciddi advers olay gözlenmeyen ve alternatif seçeneklere erişimin olmadığı koşullarda yakın takiple antibiyotik tedavisine devam edilebilir. Öte yandan bu, hasta bazında ve kâr-zarar oranı gözetilerek verilmesi gereken bir karardır.
Literatürdeki olguların yarıdan fazlasında (24 hasta, %53.3) medikal tedaviye rağmen cerrahi girişim ihtiyacı gelişmesi dikkat çekicidir (11–13). Bu nedenle multidisipliner izlem önemlidir.
Ülkemizden bildirilen dört S. maltophilia endokardit olgusu mevcuttur (24–27). Bunlardan üçü protez kapak cerrahisi sonrası gelişen, biri de olgumuzdaki gibi hemodiyaliz alan bir hastada görülen doğal kapak endokarditidir (24–26). Üçünde antibiyotik tedavisine rağmen cerrahi gerekmiştir (25–27). Olgumuz, ülkemizden bildirilen beşinci; doğal kapakta gelişmesi yönüyle de ikinci S. maltophilia endokarditidir.
Sonuç olarak; S. maltophilia endokarditi tanıda atlanabilen, kısıtlı tedavi seçenekleri olan, uzun antibiyotik tedavi süresi ve yan etkileriyle yönetimi zor ve nadir bir hastalıktır. Kan dolaşımı infeksiyonu hastalarında kateter çekimi ve uygun antibiyotik seçimi hayati önem taşımaktadır. Güncel literatürle birlikte deneyimimiz de TMP-SMX + levofloksasin kombinasyonunun makul bir tedavi seçeneği olduğunu göstermektedir. Alternatif tedavi önerileri ve duyarlılık testlerinde standardizasyon için daha fazla çalışmaya ihtiyaç vardır.
Hasta Onamı
Hastadan bilgilendirilmiş onam formu alınmıştır.
Danışman Değerlendirmesi
Bağımsız dış danışman
Yazar Katkıları
Fikir/Kavram – E.Ö., Y.H., U.Ö.; Tasarım – E.Ö., Y.H.; Denetleme – Y.H.; Malzemeler/Hastalar – E.Ö., Y.H., U.Ö., H.Ş., S.G., C.Ö.; Veri Toplama ve/veya İşleme – E.Ö., Y.H., U.Ö., H.Ş., S.G., C.Ö.; Analiz ve/veya Yorum – E.Ö., Y.H.; Literatür Taraması – E.Ö.; Makale Yazımı – E.Ö.; Eleştirel İnceleme – E.Ö., Y.H., U.Ö., H.Ş., S.G., C.Ö.
Çıkar Çatışması
Yazarlar herhangi bir çıkar çatışması bildirmemiştir.
Finansal Destek
Yazar finansal destek beyan etmemiştir.
Sunulan Bilimsel Etkinlik
Bu çalışma, 13–16 Mart 2023 tarihlerinde Antalya’da düzenlenen 23. Türk Klinik Mikrobiyoloji ve İnfeksiyon Hastalıkları Kongresi’nde bildiri olarak sunulmuştur.
Yapay Zekâ Kullanım Beyanı
Bu çalışmanın hazırlanması, veri analizi veya yazımı aşamalarında herhangi bir yapay zekâ programı kullanılmamıştır.
Referanslar
- Bouza E, Muñoz P, Burillo A. Gram-negative endocarditis: disease presentation, diagnosis and treatment. Curr Opin Infect Dis. 2021;34(6):672–80. [CrossRef]
- Schamroth Pravda M, Maor Y, Brodsky K, Katkov A, Cernes R, Schamroth Pravda N, et al. Blood stream infections in chronic hemodialysis patients – characteristics and outcomes. BMC Nephrol. 2024;25(1):3. [CrossRef]
- Aydın S, Şahin M, Yılmaz E, Mert A. [Infective endocarditis: The evaluation of 64 cases]. FLORA. 2024;29(4):509–15. Turkish. [CrossRef]
- Brooke JS. Stenotrophomonas maltophilia: an emerging global opportunistic pathogen. Clin Microbiol Rev. 2012;25(1):2–41. [CrossRef]
- Hafiz TA, Aldawood E, Albloshi A, Alghamdi SS, Mubaraki MA, Alyami AS, et al. Stenotrophomonas maltophilia epidemiology, resistance characteristics, and clinical outcomes: Understanding of the recent three years’ trends. Microorganisms. 2022;10(12):2506. [CrossRef]
- Tök G, Yapar-Toros G, Altın N, Erdoğan B, Cesur S, Kalı A, et al. [Peritonitis due to Stenotrophomonas maltophilia in a continuous ambulatory peritoneal dialysis patient]. Klimik Derg. 2013;26(1): 40–2. Turkish. [CrossRef]
- James J, Joseph JJ, Sebastian S, Antony E, Vilapurathu JK. Jugular venous catheter related Stenotrophomonas maltophilia bacteremia. Indian J Nephrol. 2021;31(2):205–6. [CrossRef]
- V T, V J, Kv L, Asokan A, George MG, Jayaprakash V. Stenotrophomonas maltophilia in hemodialysis: An opportunistic pathogen or a malevolent foe. Cureus. 2024;16(11):e73277. [CrossRef]
- Kanchanasuwan S, Rongmuang J, Siripaitoon P, Kositpantawong N, Charoenmak B, Hortiwakul T, et al. Clinical characteristics, outcomes, and risk factors for mortality in patients with Stenotrophomonas maltophilia bacteremia. J Clin Med. 2022;11(11):3085. [CrossRef]
- Gezer Y, Tayşi MR, Tarakçı A, Gökçe Ö, Danacı G, Altunışık Toplu S, et al. Evaluation of clinical outcomes and risk factors associated with mortality in patients with Stenotrophomonas maltophilia bloodstream infection: a multicenter study. BMC Infect Dis. 2024;24(1):1387. Erratum in: BMC Infect Dis. 2024;24(1):1396. [CrossRef]
- Subhani S, Patnaik AN, Barik R, Nemani L. Infective endocarditis caused by Stenotrophomonas maltophilia: A report of two cases and review of literature. Indian Heart J. 2016;68 Suppl 2(Suppl 2):S267–70. [CrossRef]
- Kogler W, Davison N, Richardson A, Rollini F, Isache C. Endocarditis caused by Stenotrophomonas maltophilia-A rare presentation of an emerging opportunistic pathogen. IDCases. 2019;17:e00556. [CrossRef]
- Shah S, King M, Rose L. Medical management of endocarditis caused by Stenotrophomonas maltophilia: A case report. J Pharm Pract. 2019;32(6):683–6. [CrossRef]
- Maraolo AE, Licciardi F, Gentile I, Saracino A, Belati A, Bavaro DF. Stenotrophomonas maltophilia infections: A systematic review and meta-analysis of comparative efficacy of available treatments, with critical assessment of novel therapeutic options. Antibiotics (Basel). 2023;12(5):910. [CrossRef]
- Delgado V, Ajmone Marsan N, de Waha S, Bonaros N, Brida M, Burri H, et al; ESC Scientific Document Group. 2023 ESC Guidelines for the management of endocarditis. Eur Heart J. 2023;44(39):3948–4042. Erratum in: Eur Heart J. 2023;44(45):4780. Erratum in: Eur Heart J. 2024;45(1):56. Erratum in: Eur Heart J. 2025;46(11):1082. [CrossRef]
- The European Committee on Antimicrobial Susceptibility Testing (EUCAST). Breakpoint tables for interpretation of MICs and zone diameters. Version 15.0, valid from Jan 01, 2025 [Internet]. Växjö: EUCAST; 2025. [cited September 15, 2025]. Available from: https://www.eucast.org/fileadmin/src/media/PDFs/EUCAST_files/Breakpoint_tables/v_15.0_Breakpoint_Tables.pdf
- Clinical and Laboratory Standards Institute (CLSI). Performance standards for antimicrobial susceptibility testing. CLSI supplement M100. 35th ed. Wayne (PA): CLSI; 2025.
- Sadıç B, Başaran S, Şimşek-Yavuz S, Çağatay A, Özsüt H, Eraksoy H. [Stenotrophomonas maltophilia: Results of antimicrobial susceptibility testing and in vitro activity of the combination of ceftazidime and moxifloxacin]. Klimik Derg. 2019;32(1):29–34. Turkish. [CrossRef]
- Tamma PD, Heil EL, Justo JA, Mathers AJ, Satlin MJ, Bonomo RA. Infectious Diseases Society of America 2024 Guidance on the treatment of antimicrobial-resistant Gram-negative infections. Clin Infect Dis. 2024:ciae403. [CrossRef]
- Sümer Ş, Kurt Azap Ö, Aygün G, Akalın H, Akova M, Köksal İ. [Common problems and solutions in the management of resistant Gram-negative bacterial infections: expert opinion on clinical practice]. FLORA. 2024;29(1):1–24. Turkish. [CrossRef]
- Deva Holding A.Ş. Bactrim® 400/80 mg IV enjektabl çözelti içeren ampul, kısa ürün bilgisi [Internet]. İstanbul: Deva Holding; 2025. [cited September 18, 2025]. Available from: https://www.deva.com.tr/uploads/product_files/qEVqSz1xjIONV6TQK3Bi.pdf
- Preyra R, Eddin LE, Ahmadi F, Jafari A, Muanda FT. Safety of sulfamethoxazole-trimethoprim for the treatment of bacterial infection in outpatient settings: A systematic review and meta-analysis with active comparator disproportionality analysis. Br J Clin Pharmacol. 2025;91(6):1632–48. [CrossRef]
- Ho JM, Juurlink DN. Considerations when prescribing trimethoprim-sulfamethoxazole. CMAJ. 2011;183(16):1851–8. [CrossRef]
- Aydin K, Köksal I, Kaygusuz S, Kaklikkaya I, Caylan R, Ozdemir R. Endocarditis caused by Stenotrophomonas maltophilia. Scand J Infect Dis. 2000;32(4):427–30. [CrossRef]
- Sanioğlu S, Sokullu O, Yavuz SS, Kut MS, Palaz FK, Bilgen FS. Stenotrophomonas maltophilia endocarditis treated with moxifloxacin-ceftazidime combination and annular wrapping technique. Anadolu Kardiyol Derg. 2008;8(1):79–80.
- Ucak A, Goksel OS, Inan K, Tatar T, Ozelçi A, Us M, et al. Prosthetic aortic valve endocarditis due to Stenotrophomonas maltophilia complicated by subannular abscess. Acta Chir Belg. 2008;108(2):258–60. [CrossRef]
- Alat I, Kılıç AT, Çelik E. Replacement of the native mitral valve due to endocarditis caused by Stenotrophomonas maltophilia. Braz J Cardiovasc Surg. 2019;34(5):615–7. [CrossRef]