En Çok Okunanlar
Özet
Diyabetik hastalarda gelişen ayak yaraları ve infeksiyonları tüm dünyada önemli sağlık problemleri arasında yer almaktadır. Türk Klinik Mikrobiyoloji ve İnfeksiyon Hastalıkları Derneği Diyabetik Ayak İnfeksiyonları Çalışma Grubu (DAİÇG), ülkemiz koşullarında diyabetik ayak (DA) yarasının ve DA infeksiyonu (DAİ)’nun tanısı, tedavisi ve önlenmesine yönelik bir Ulusal Uzlaşı Raporu’nu 2015 yılında hazırlamıştır. Söz konusu raporun güncellenmesi için 2023 yılında ilgili ulusal uzmanlık derneklerine iş birliği çağrısında bulunulmuştur. Görevlendirilen temsilcilerin katılımıyla ilgili literatür ve uluslararası kılavuzlar gözden geçirilerek; patogenez, mikrobiyoloji, değerlendirme ve derecelendirme, tedavi, korunma ve kontrol, basıdan kurtarma, ampütasyon sonrası rehabilitasyon konularında yanıt verilmesi gereken sorular saptanmış ve bu sorulara yönelik uzlaşılan yanıtlarla rapor güncellenmiştir. Raporun amacı diyabetik hastalarla ilgilenen tüm sağlık çalışanlarına yardımcı olmaktır ve sorulara verilen yanıtlar şu şekilde özetlenebilir: 1) DA yarasının gelişiminin pek çok nedeni olmakla birlikte en önemli nedenler sensorimotor polinöropati ve periferik arter hastalığı (PAH) gelişimidir. 2) DA yarası olan bir hastada diğer nedenler dışlandıktan sonra yara bölgesinde pürülan akıntı veya eritem, ödem, ısı artışı, ağrı, hassasiyet, endürasyon gibi lokal inflamasyon bulgularından en az ikisi varsa yara infeksiyonu düşünülmelidir. Bu olgularda; yaranın derinliği, genişliği ve infeksiyonun sistemik bulgularının olup olmamasına bağlı olarak hafif, orta veya şiddetli infeksiyon tanımlaması yapılır. 3) DAİ’de etkenler, infeksiyonun akut ya da kronik olmasına ve şiddetine bağlı olarak değişiklik gösterir. Selüliti olan ve daha önce antibiyotik kullanmamış hastalarda gelişen yüzeysel DAİ’lerden daha çok aerop Gram-pozitif koklar (stafilokok, streptokoklar) sorumludur. 4) Derin ve kronik infeksiyonlar ve/veya daha önce antibiyotik tedavisi alan hastalarda gelişen infeksiyonlar genellikle polimikrobiktir (Gram-pozitif kok + Gram-negatif basil). 5) Diyabetik ayak infeksiyonlarının ciddiyetinin değerlendirilmesinde Uluslarası Diyabetik Ayak Çalışma Grubu / Amerikan İnfeksiyon Hastalıkları Derneği (IWGDF/IDSA) sınıflaması kullanılabilir. 6) Bu sınıflamaya göre ağır ve bazı özellikli DAİ olguları hastaneye yatırılarak tedavi edilmelidir. 7) İnflamasyon göstergeleri olan C-reaktif protein (CRP), eritrosit sedimantasyon hızı (ESH) ve prokalsitonin gibi biyobelirteçler, infeksiyonla kolonizasyonun ayırt edilmesinde yararlı olabilir. 8) DAİ şüphesinde antibiyotik başlanmadan önce kültür için uygun doku örneği yara tabanından küretaj veya biyopsi yöntemi ile alınmalıdır. 9)Tanıda görüntüleme yöntemi olarak öncelikle üç yönlü direkt ayak grafisi çekilmelidir; böylelikle infeksiyonun yanı sıra kemik deformiteleri-kırık, radyoopak yabancı cisimler ve yumuşak dokudaki gaz oluşumları da saptanabilir. 10) Manyetik rezonans görüntülemesi (MRG), tedaviye yanıt alınamayan, osteomyelit ya da derin yumuşak doku apsesi düşünülen hastalar için duyarlı ve özgül bir yöntemdir. 11) Osteomyelit tanısında, kemik kültüründe üreme olması ve histopatolojik incelemede pozitif sonuç altın standart olarak kabul edilmektedir. 12)Yara iyileşmesini sağlayabilmek ve ayağı kurtarmak için gerekenler; acil ve agresif debridmanlarla ölü ve infekte dokuların uzaklaştırılması, uygun yara bakımı, ayağın yükten ve basıdan kurtarılması, uygun antibiyotik tedavisi, metabolik kontrol, PAH tanısı-uygun şekilde tedavisi ve ayağın işlevinin kazandırılmasıdır. 13) DAİ ve PAH birlikteliğinde cerrahi uygulamanın planlaması ve zamanlaması için ilgili cerrahi branş ile birlikte revaskülarizasyon kapsamında vasküler cerrahiden de görüş alınmalıdır. DA yaralarında cerrahi yaklaşımı beş ana başlıkta incelemek gerekir: (a) Acil yara müdahalesi; apse drenajı ve/veya debridman. (b) Vasküler patolojiler için yapılan cerrahi girişimler. (c) Yara kapatıcı müdahaleler, rekonstrüksiyon yöntemleri, greft ve flep cerrahisi. (d) Ülseri önleme ve tedavi amaçlı kemik ve ayak patolojilerinin rekonstrüksiyonu (Charcot ayak deformitesi, aşil uzatılması, tenotomi ve gerektiğinde osteotomiler, vb.). (e) Gereğinde uygulanan minör ve majör ampütasyonlar. 14) Debridmanla infekte dokunun tamamen temizlenmesi mümkün olmadığında ve hastanın kalan infeksiyon yüküyle başa çıkamayacağı durumlarda, yatalak veya fonksiyonel olarak işlevsiz bir ekstremitesi olan hastalarda, uygulanacak ortopedi ve plastik cerrahi girişimlerinin uygulanması için gerekli revaskülarizasyonun sağlanamayacağı düşünülen hastalarda, rekonstrüksiyonu neredeyse olanaksız olan olgularda ve diyaliz hastalarında ampütasyon daha doğru bir seçim olabilir. 15) Diyabetik ayak infeksiyonu sonrası rekonstrüksiyonun hedefi, ayak bileğinin nötral pozisyona kadar gelebilmesini ve ayak tabanının yere dengeli olarak basmasını sağlamaktır. 16) Yara iyileşmesini desteklemek ve hızlandırmak, komplikasyon riskini azaltmak, tedavi sırasında hastanın günlük yaşantısına konforlu olarak devam etmesini sağlamak ve yaşam kalitesini artırmak amacı ile yaranın özelliklerine göre seçilen yara bakım ürünleri kullanılabilir. 17) Diyabetik ayak yarası; yapısal ve biyomekanik değişimler sürecinde sıklıkla doğru ayakkabı tercih edilmemesi nedeniyle, kemik yüzeyler çevresinde su toplaması ve nasırlaşma sonucunda ortaya çıkmaktadır. 18) Ayak plantarındaki basıncı azaltmanın en etkili yolu olan ortezler, basıncı mümkün olan en geniş alana dağıtarak görev yapar. 19) Hiperbarik oksijen tedavisi; iskemi, infeksiyon, ödem gibi doku hipoksisine yol açan patolojilerde, bu patolojilerin ana tedavisi olan revaskülarizasyon ve antibiyoterapiye ilave olarak kullanıldığında fayda sağlar. 20) Negatif basınçlı yara kapama sistemlerinin kullanımı, klasik yöntemlere ilave ve yardımcı bir yöntemdir ve iyileşme sürecinde katkı sağlanması için doğru indikasyonla kullanılabilir. 21) İnfeksiyonun kontrol altına alındığı, aktif osteomyeliti olmayan hastalarda Meggitt-Wagner sınıflaması derece 1-3 arasında topikal epidermal büyüme faktörü (EGF), derece 3-4’te de intralezyoner EGF uygulamaları standart tedavilere ek olarak yer alabilir. 22) Diyabetik hastalarda, koruyucu hekimlik uygulamaları ile birlikte ayak yarası gelişiminin engellenmesi için hasta, hasta yakını ve tıbbi ekibin iş birliği içinde olması ve düzenli eğitimi gereklidir. Ayak yarasının geliştiği durumlarda erken tedavi ve infeksiyon gelişiminin önlenmesi için; infeksiyonun geliştiği durumlarda ise orta/şiddetli infeksiyonun tedavi başarısını artırmak için interdisipliner bir yöntemle çalışmak son derece önemlidir.
GİRİŞ
Diyabet prevalansı gerek ülkemizde gerek dünyada artmaya devam etmektedir. Uluslararası Diyabet Federasyonu 2021 yılı itibarı ile dünyada 537 milyon yetişkinin diyabetle yaşadığını bildirmiştir. Ülkemizde ise bu sayı 9 milyonun üzerindedir (1). Bu durum infeksiyon da dahil olmak üzere ayak komplikasyonlarının artışını beraberinde getirmektedir. Diyabetik ayak (DA) yaraları hem hastalar hem de sağlık bakım sistemleri için ciddi sonuçları olan bir sorundur. Diyabetli bir kişinin yaşamının herhangi bir evresinde ayak yarası nedeniyle hastaneye başvurma riski yaklaşık %35 düzeyindedir. Tedavi sonrası olguların %50’sinde yeniden yara oluştuğu bildirilmektedir. Diyabetlilerde ampütasyonların %85’i ayak yarası nedeniyle uygulanmakta ve alt ekstremite ampütasyonu sonrası beş yıllık mortalite %77 düzeyine yükselmektedir. Bu nedenle, diyabette ayak yarasına yol açan faktörlerin bilinmesi ve riskli hastaların yakın takibi son derece önemlidir (2-4). Diyabetik ayak infeksiyonu (DAİ); yara bakımı, antimikrobiyal tedavi ve cerrahi işlemler nedeniyle sık hastane başvurusu gerektiren ve yüksek maliyetlere yol açan diyabetin önlenebilir bir komplikasyonudur. Diyabetle ilişkili olarak hastaneye yatışın en sık sebebi olmasının yanısıra alt ekstremite ampütasyonlarında en yaygın risk faktörü olmaya devam etmektedir (5,6).
Diyabetik ayak yarası ve infeksiyonlarını, diyabetin kontrol altında tutulmasının yanı sıra ayak bakımı ile engellemek mümkün olabilir. Diyabetik hastada ayak yarası gelişimi için risk faktörlerinin yönetimi, hastanın bu süreçteki uyumu, takip sıklığının belirlenmesi ve hastanın önlemlere uyumundaki sürekliliği yara gelişiminin önlenmesinde, gelişen yaraların infekte olmadan erken tedavisinde son derece önemlidir. Diyabetik ayak infeksiyonunun gelişmesi halinde interdisipliner olarak hızlı ve etkin tedavi yaklaşımının uygulanması ampütasyonları azaltmada etkilidir. Unutulmamalıdır ki, DAİ ne kadar etkin tedavi edilirse edilsin gelişimindeki risk faktörleri için uygun önlemler oluşturulup hastanın bu sürece uyumu sağlanmazsa yeni gelişen DA yaraları ve infeksiyonları ile karşılaşılacaktır.
Diyabetlilerde gelişen ayak yaraları ve infeksiyonları tüm dünyada önemli sağlık problemleri arasında kabul edilmektedir. Bu sorunun çözümüne katkı sağlamak için ilişkili ulusal uzmanlık derneklerinin iş birliği ve Sağlık Bakanlığı katılımı ile Türk Klinik Mikrobiyoloji ve İnfeksiyon Hastalıkları Derneği Diyabetik Ayak İnfeksiyonları Çalışma Grubu (DAİÇG) tarafından DA Ulusal Uzlaşı Raporu 2015 yılında hazırlamıştır. Ardından 2023 yılında raporun güncellenmesi amacı ile ilgili ulusal uzmanlık derneklerine iş birliği daveti yapılmış ve görevlendirilen temsilcilerin çalışmaları ile ilgili yeni literatür ve uluslararası kılavuzlar gözden geçirilerek, patogenez, mikrobiyoloji, değerlendirme ve derecelendirme, tedavi, korunma ve kontrol, basıdan kurtarma, ampütasyon düzeyinin belirlenmesi, ampütasyon sonrası rehabilitasyon, podolojik yaklaşım konularında yanıt verilmesi gereken sorular saptanmış ve bu sorulara üzerinde uzlaşılmış yanıtlar verilerek rapor güncellenmiştir. Raporda yer alan bilgilerin, ülkemizdeki diyabetik hastalarla ilgilenen tüm sağlık çalışanlarına yardımcı olması amaçlanmıştır
PATOGENEZ
Soru 1: Diyabetik Ayak Yarası ve İnfeksiyonunun Patogenezi Nasıldır?
Diyabetli bir olguda ayak yarası gelişimi; haberci semptomları, uyarıcı fizik muayene bulguları ve risk faktörleri ile ilişkili, akut ve ani gelişimli olmayan bir komplikasyondur. Diyabete özgü mikro ve makrovasküler hasarlar sonucunda ortaya çıkar. Diabetes mellitus tanısı ile izlenen hastalarda ayak yarası gelişimine yol açan iki majör nedenden biri diyabetik polinöropati, diğeri ise periferik arter hastalığıdır (PAH) (2).
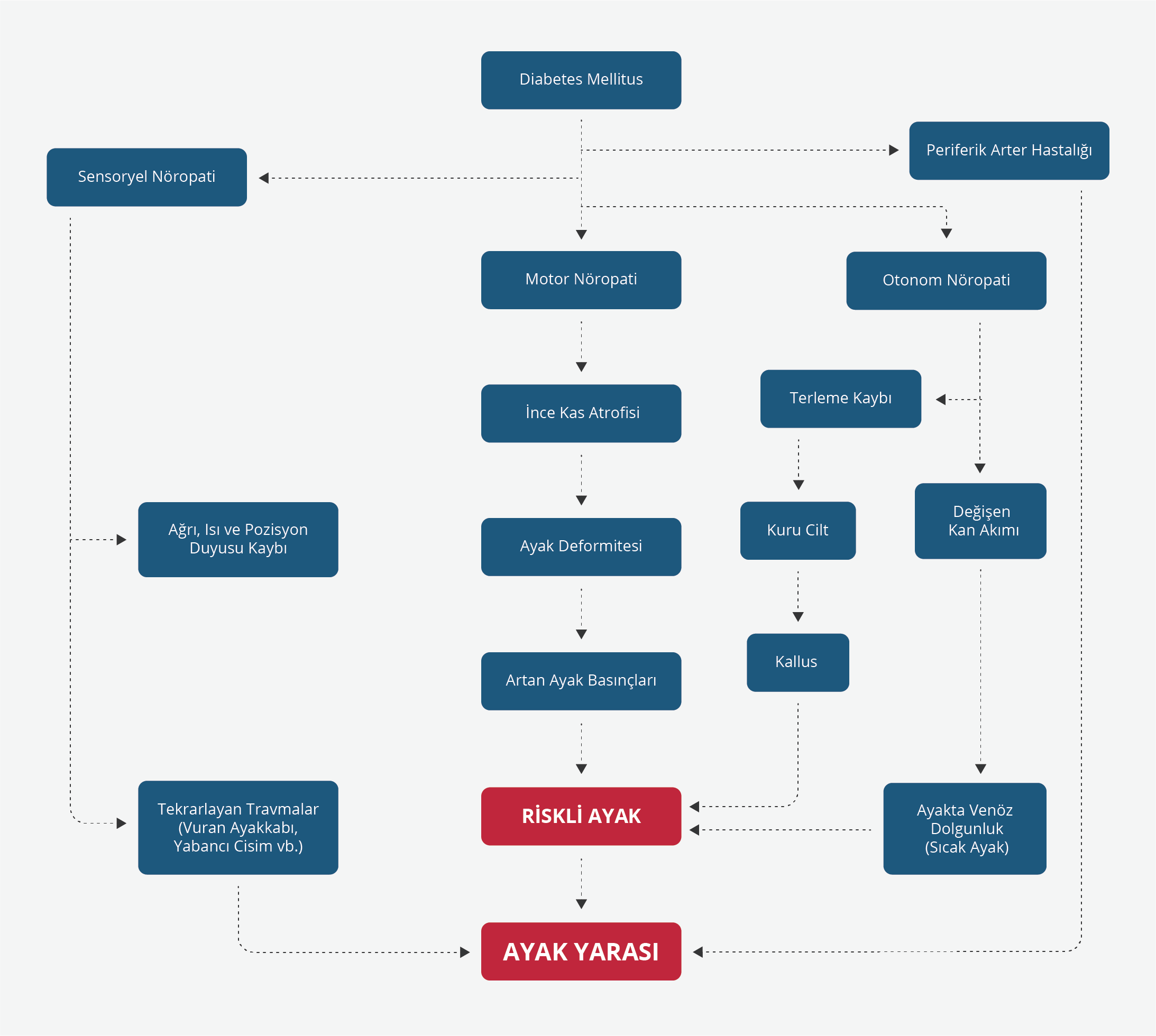
Diyabetik ayak yaralarının en sık nedeni olan sensorimotor polinöropati, simetrik ve distal yerleşimlidir. Her iki ayakta parmak uçlarından başlayan ve proksimale doğru yayılım gösteren paresteziler, yanma, elektrik çarpması, diken batmaları, üşüme gibi pozitif semptomlar duyusal nöropatinin başlangıç bulgularıdır. Keçeleşme, pamuğa basma, hissizlik gibi negatif semptomlar parestezileri izleyen dönemde veya onlara birlikte ortaya çıkar. Zamanla gelişen ağrı duyusu kaybı, sıcağı ve soğuğu hissedememe ayağı travmalara açık hale getirir. Doku bütünlüğünü bozan bir minör travma, örneğin ayakkabı vurması, yanık, böcek sokması gibi durumlar kolayca yara gelişimini tetikler. Hastanın ağrıyı hissetmemesi hekime geç başvurmasına neden olarak tanıyı geciktirir. Şekil 1’de diyabetin komplikasyonlarından ayak ülserine giden yol özetlenmiştir (2).
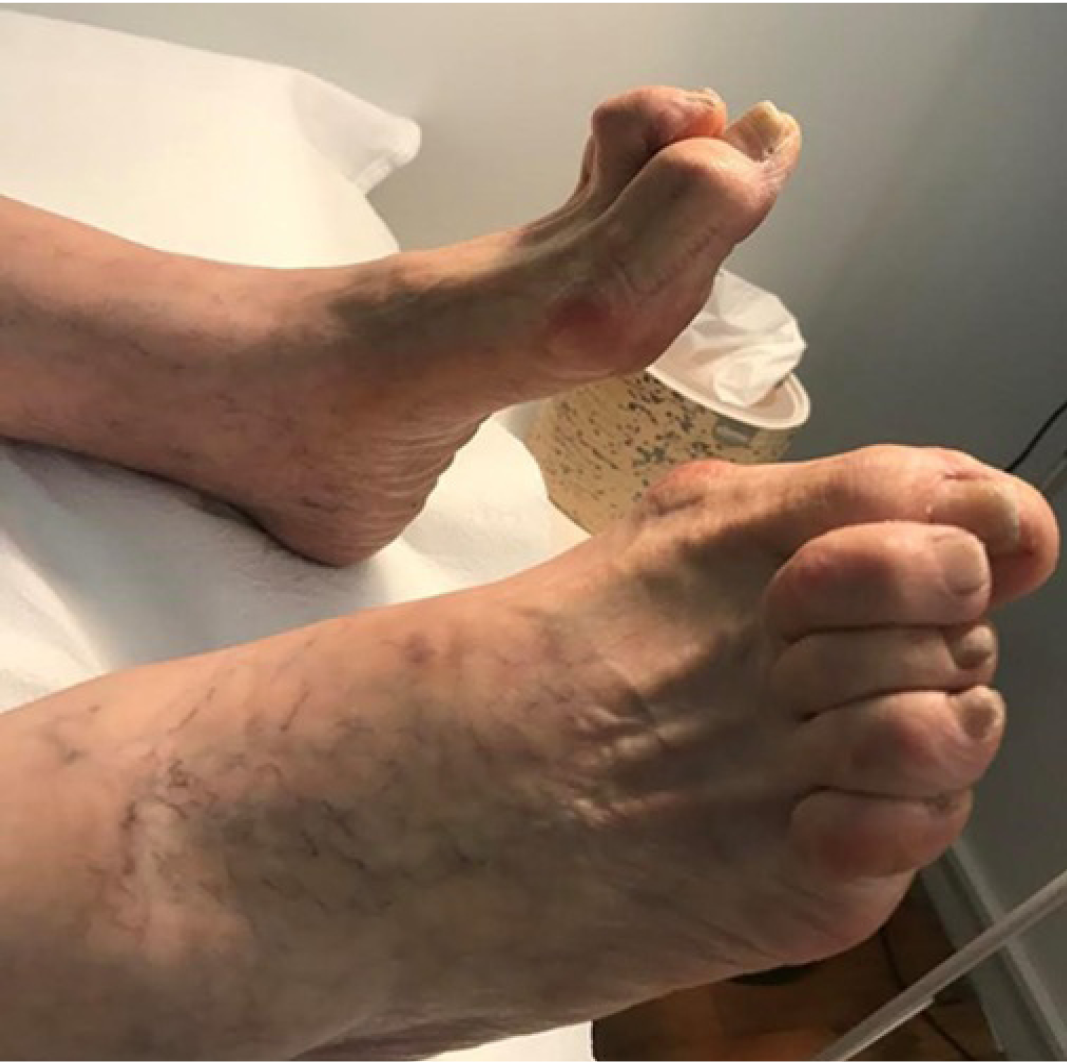
Şekil 2. Tip 2 Diyabetli Bir Hastada Pençe Ayak ve Çekiç Parmak Deformiteleri (Zeynep Oşar Siva’nın izni ve hastanın onamı ile fotoğraf kullanılmıştır.)
Motor nöropati ile yara arasındaki ilişki ise oldukça komplekstir. Motor sinirlerdeki harabiyete bağlı olarak gelişen kas atrofileri, ayakta deformite gelişimine neden olur. Bu şekil bozuklukları yürüme biyomekaniğini etkiler ve yük taşıyan bölgeler değişir. Bunun yanısıra, hiperglisemi; kollajen ileri glikozilasyonu son ürünlerinin (“advanced glycation end products” – AGEs) ortaya çıkmasına, bağ doku yapısında bozulmaya, tendon sertliği ve tendon kısalmalarına yol açarak, eklem sertliği ve deformite oluşumuna katkıda bulunur. Çekiç parmak, pençe ayak ve yüksek ayak arkı bu şekilde ortaya çıkan deformitelerden bazılarıdır (Şekil 2) (7). Sonuçta, değişen ayak anatomisi, biyomekanik travmalara neden olur ve kallus gelişimi tetiklenir. Birinci parmak mediali ve metatars başlarının altı kallus gelişimi açısından riskli bölgelerdir. Kallus gelişimi, yumuşak doku hasarı ve infeksiyonu açısından ciddi bir risk oluşturur. Kallus altındaki yumuşak dokuda zamanla kanama ve iskemiye bağlı hasarlar gelişir ve tablo kronik ayak yarasına ilerler. Ağrı duyusu kaybının da eklendiği bu seyirde, mekanik veya termal travmalara bağlı ülser ve infeksiyonlar kolayca ortaya çıkacaktır.
Otonom nöropati ve yara gelişimindeki rolü, göz ardı edilmemesi gereken bir diğer mikrovasküler diyabet komplikasyonudur. Otonom nöropati terleme bozukluğuna ve anhidroza yol açarak deride kuruluğa, çatlaklara neden olur ve kallus oluşumuna katkıda bulunur. Çatlaklar, deri bütünlüğünü bozarak infeksiyon gelişimini kolaylaştıran yapısal defektlerdir (8).
Charcot ayağı, bir diğer tanımı ile diyabetik nöroartropati de etyopatogenezinde yine nöropatinin rol oynadığı bir nöropatik ayak komplikasyonudur. Primer bozukluk, kutanöz arteriyovenöz kaçaklar ve nöropatik ödemdir. İnflamatuar bir yanıt olarak ortaya çıkar ve osteoklastik aktivite artar. Bu olaylar dizisi, Charcot ayağı olarak bilinen nöroartropatiyle sonlanır. Akut ve kronik nöroartropatinin ayırımı ve infeksiyon ile ayırıcı tanısı, ampütasyon veya kalıcı sakatlık ile sonlanmadan tedavi edilebilmesi açısından büyük önem taşır. Charcot ayağının ağır şekil bozuklukları DA yarası gelişimi açısından ciddi risk ortaya çıkarır (2-4,8,9).
Yara etiyolojisinde rol oynayan bir diğer diyabet komplikasyonu bacak arterlerinde görülen PAH’dır. Diyabetik ayak yarası olguların yaklaşık %50’sinde çeşitli seviyelerde PAH olduğu bildirilmiştir. Diyabete bağlı ateroskleroz ağırlıklı olarak büyük ve orta boy arterleri tutar. Anatomik özelliği diyabetli olmayan popülasyondan farklı olarak distal dağılım gösterir ve multipl seviyelerde kruris arterlerine yerleşerek uzun segmentli tıkanıklıklar oluşturur. Kollateral gelişimi yetersiz, buna karşılık medya kalsinozis prevalansı yüksektir. Bütün bu faktörler diyabetli olgularda endovasküler veya cerrahi revaskülarizasyon açısından teknik zorluklar oluşturur (10). Periferik arter hastalığı ilgili bölümde detaylı olarak ele alınmıştır.
Hiperglisemik ortamın komplikasyonlardan bağımsız olarak infeksiyon eğilimini artırdığı bilinmektedir. Kontrolsüz diyabette hiperglisemi, nötrofillerin fagositer ve bakterisidal işlevlerinde bozulmaya, oksidatif strese ve inflamatuar sitokinlerde artışa yol açar. Hiperglisemi, özellikle lökosit diyapedezini, kemotaksisini, fagositozunu bozar ve intraselüler lizisi inhibe eder. Uzun süreli hiperglisemide ortaya çıkan AGE’ler makrofajlara bağlanarak tümör nekroz faktörü-α (TNF-α) başta olmak üzere dönüştürücü büyüme faktörü-β (“transforming growth factor-β” – TGF-β), interlökin (IL)-6 gibi birçok sitokinin salınmasına ve reaktif oksijen türlerinin (“reactive oxygen species” – ROS) artmasına bağlı olarak düşük düzeyli inflamasyona neden olur. Lökosit fonksiyonlarındaki yetersizliğe, kollajen metabolizmasındaki ileri glikolizasyon son ürünleri aracılıklı bozulmanın da eklenmesi hem infeksiyon ile mücadeleyi güçleştirir hem de yara iyileşmesini geciktirir (2-4,7). Periferik arter hastalığı ayrıca nötrofil fonksiyonlarını olumsuz yönde etkiler, yara ortamından toksik metabolik artıkların uzaklaştırılmasını güçleştirir ve yara iyileşmesini geciktirir. Diğer metabolik dengesizlikler, görme kaybı, hareket kısıtlılığı ve geçirilmiş ampütasyonlar da travmaya yatkınlığı artırır. Temizlik kurallarına ve ayak bakımına uymama ya da aşırı kilo gibi uyumsuz hasta davranışları, kronik hastalık psikolojisi ve depresyonla birleşince iyileşme daha da zorlaşır. Nöropati, iskemi, kontrolsüz hiperglisemi ve eksternal bir travma sonucunda ortaya çıkan yüzeysel yara ve infeksiyonlar kısa zamanda derin yerleşimli apse ve osteomyelite ilerleyebilir (2-4,7).
Diyabetik Ayak Risk Faktörleri
Diyabetik ayak yarası risk faktörlerinin tanımlanması olguların yakın takibi açısından büyük önem taşır. Yara etyopatogenezinde rol oynayan mekanizmaların ışığında, risk oluşturan faktörleri aşağıdaki şekilde sıralayabiliriz (8):
- Kötü glisemik kontrol,
- Periferik nöropati, protektif duyu kaybı (PDK),
- Periferik arter hastalığı,
- Ayak deformiteleri (bunyon, çekiç parmak, Charcot ayağı, vb.),
- Preülseratif nasır veya kallus,
- Geçirilmiş ülser,
- Geçirilmiş ampütasyon,
- Sigara,
- Retinopati,
- Son dönem böbrek yetersizliği.
- Diyabet ayak yarası risk faktörlerinin varlığına göre olguların takip sıklığı belirlenmelidir.
Özetle, diyabette infekte ayak yarası gelişimi; diyabetin kronik komplikasyonları, sensorimotor polinöropati ve PAH nedeniyle ortaya çıkan ciddi bir komplikasyondur. Hiperglisemik ortam infeksiyon riskini artırarak yara iyileşmesini geciktirir. Etyopatogenezin iyi kavranması DA yarasının ve infeksiyonunun önlenmesi, erken tanısı, doğru tedavisi ve dolayısıyla ampütasyonun önlenmesi açısından büyük önem taşır (8).
MİKROBİYOLOJİ
Soru 1: Diyabetik Ayak İnfeksiyonlarında Etken Mikroorganizmalar Nelerdir?
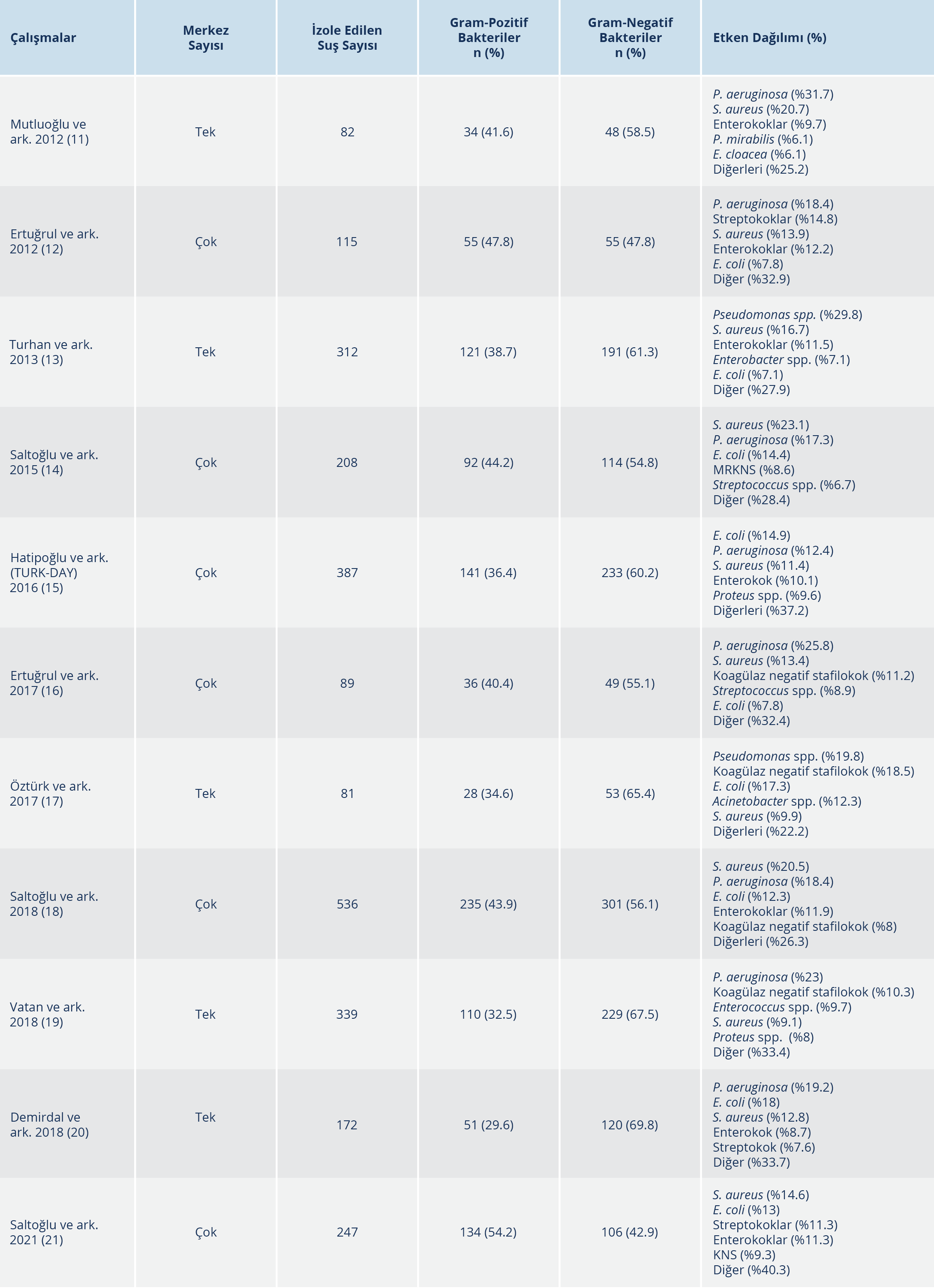
Diyabetik ayak infeksiyonlarının etkenleri, infeksiyonun akut ya da kronik olmasına ve şiddetine bağlı olarak değişiklik gösterir. Türkiye’de çeşitli çalışmalarda belirlenen DAİ etkenleri Tablo 1’de gösterilmiştir (11-21). Selüliti olan ve daha önce antibiyotik kullanmamış hastalarda gelişen yüzeysel DAİ’lerden, daha çok Staphylococcus aureus, Streptococcus agalactiae, Streptococcus pyogenes gibi aerop Gram-pozitif koklar sorumludur. Derin ve kronik infeksiyonlar ve/veya daha önce antibiyotik tedavisi alan hastalarda gelişen infeksiyonlar, genellikle polimikrobiktir. Kronik ya da antibiyotik tedavisini izleyerek gelişen yaraların infeksiyonlarında, etiyolojik etkenler arasında enterokokların da dahil olduğu Gram-pozitif etkenlere ek olarak Enterobacterales takımındaki aerop Gram-negatif basiller ve Pseudomonas aeruginosa da yer alır. Şiddetli yerel inflamasyon, nekroz, gangren ya da kötü kokulu akıntısı olan ve sistemik toksisitenin söz konusu olduğu yaralarda yukarıdaki etiyolojik etkenlerle birlikte anaerop patojenler de yer alırlar. Başlıca anaerop patojenler, anaerop streptokoklar, Bacteroides ve Clostridium türleridir. Diyabetik hastalarda önemli bir sorun olan ayak tırnağındaki ve/veya parmak arasındaki mantar infeksiyonlarına zamanında müdahale edilmesi gerekir. Bunlar bakterilerin girişi için kolaylaştırıcı bir faktör, giriş kapısı olarak rol oynarlar. Bu infeksiyonlara karşı topikal ya da oral antifungal ilaçlar önerilir.
Soru 2: Hangi Durumlarda Dirençli Patojenler Düşünülmelidir?
Diyabetik ayak infeksiyonlarında dirençli patojen varlığı; tedavi başarısızlığı, uzamış hastane yatışları ve maliyet artışı ile doğrudan ilişkili bulunmuştur (12). 2010 yılı sonrasında Türkiye’de yapılmış çok merkezli çalışmalarda S. aureus suşlarında metisilin direnci %20-31, Enterobacteriaceae ailesi içinde genişlemiş spektrumlu β-laktamaz (GSBL) pozitifliği %27-38.5, P. aeruginosa’da çoğul ilaç direnci (ÇİD) pozitifliği %18-21 olarak saptanmıştır (15,19,22).
Diyabetik ayak infeksiyonu gelişmiş hastalarda; 1) önceden hastane yatışı, 2) önceden antibiyotik kullanım öyküsü (özellikle son 30 gün içinde), 3) osteomyelit varlığı, 4) ampütasyon öyküsü, 5) hastane yatışının uzaması, 6) ülserin büyüklüğü, 7) ülserin ileri evre oluşu, 8) kötü glisemik kontrol ve 9) vasküler hastalık varlığı, dirençli mikroorganizma varlığı için risk faktörleri olarak saptanmıştır (23-30). Yine bazı çalışmalarda, biyofilm varlığı ile ÇİD olan mikroorganizma varlığı ilişkili tespit edilmiş olmakla birlikte sebep sonuç ilişkisinin yönü henüz belirlenememiştir (19).
Soru 3: Metisiline Dirençli S. aureus (MRSA) Ne Zaman Etken Olarak Düşünülmelidir?
Hastanın daha önce MRSA ile kolonize olması ya da infeksiyon geçirmesi, bu bakteriyle DAİ gelişmesi açısından önemli bir risk faktörüdür. Aşağıdaki faktörlerin varlığında DAİ olan hastalar MRSA açısından değerlendirilmelidir (11,31-34):
- Şiddetli infeksiyon,
- Altı haftanın üzerinde iyileşmeyen yara varlığı,
- Son bir yıl içerisinde hastaneye yatış,
- Uzun süreli antibiyotik (kinolon gibi) kullanımı öyküsü,
- Osteomyelit,
- Önceki MRSA kolonizasyonu ya da infeksiyonu,
- Yüksek yerel MRSA oranları (orta derece infeksiyon için %30, hafif infeksiyon için %50),
- Kronik böbrek yetmezliği nedeniyle diyalize girmek,
- Bakım merkezinde kalmak.
Soru 4: Pseudomonas Cinsi Bakteriler Ne Zaman Etken Olarak Düşünülmelidir?
Pseudomonas türlerinin izole edilmesi hedefe yönelik tedavinin başlanmasını gerekli kıldığından, bu bakteriler özellikle sorun oluşturmaktadır. Pseudomonas aeruginosa, ülkemizde olduğu gibi hastanın ayak parmak aralarının çoğu kez ıslak kaldığı durumlarda ya da nemli iklimlerde yaşayan hastalarda yaygın olarak karşılaşılan etkenlerden biridir. Yüzeyi aşınmış yaralarda, ayağın nemli kalması durumunda ve bakımsız ayaklarda Pseudomonas infeksiyonu gelişme riski artar. Bununla birlikte daha önce P. aeruginosa’ya maruz kalınması, MRSA’da olduğu gibi riski artırmaz. Ülkemizde son 10 yılda yapılan çok merkezli çalışmalarda söz konusu türler %9-31 oranlarında etken olarak bildirilmiştir (11-21). Son yıllarda yapılmış çalışmalarda bildirilen dirençli Pseudomonas infeksiyonu gelişme oranları da %18-21’e ulaşmıştır (19,25,28).
Soru 5: Genişlemiş Spektrumlu β-laktamaz (GSBL) Oluşturan Bakteriler Ne zaman Etken Olarak Düşünülmelidir?
Dirençli enterik Gram-negatif basiller ve özellikle GSBL oluşturan enterik bakteriler son yıllarda oldukça yaygın olarak görülen patojenlerdir (35). Bu patojenler daha önce hastanede yatan, özellikle sefalosporin ve kinolon sınıfı antibiyotikleri kullanan ve uzun süre bakım merkezlerinde bulunan hastalarda daha yaygındır. Türk Klinik Mikrobiyoloji ve İnfeksiyon Hastalıkları Derneği DAİÇG tarafından yapılan çok merkezli çalışmalarda; DA hastalarından izole edilen Escherichia coli suşlarında GSBL pozitifliği 2015 yılında %33 olarak bildirilirken (14), 2018 yılında bu oran E. coli ve Klebsiella suşlarında %38 ve 2021 de %38.5 olarak saptanmıştır (18,21). Düzenli sağlık hizmetinin aksadığı COVID-19 döneminde yapılmış çok merkezli çalışmada ise bu oran E. coli için %55 ve Klebsiella türleri için %62.5 olarak belirlenmiştir (36).
DEĞERLENDİRME VE DERECELENDİRME
Genel Değerlendirme
Soru 1: Ayağında Yara ile Gelen Diyabetik Bir Hastada Hangi Durumda İnfeksiyon Düşünülmelidir?
Diyabetik ayak yarası olan hastada yara bölgesi değerlendirilirken travma, kırık gibi inflamasyona yol açan diğer sebepler dışlandıktan sonra, yara bölgesinde pürülan akıntı veya eritem, ödem, ısı artışı, ağrı, hassasiyet, endürasyon gibi lokal inflamasyon bulgularından en az ikisi varsa yara infeksiyonu düşünülmelidir. Nöropatik veya vasküler yetmezliği olan hastalarda ağrı duyusu azalabilir veya hiç olmayabilir; bu olgularda yarada iyileşmenin gecikmesi, renk değişikliği, frajilite infeksiyon lehine bulgulardır. Hastada lokal yara infeksiyon bulguları ile birlikte ateş, hipotermi, taşikardi, takipne, hipotansiyon, lökositoz veya lökopeni gibi sistemik inflamatuar yanıt bulgularının en az ikisinin varlığında sistemik infeksiyon düşünülmelidir (37,38).
Soru 2: Diyabetik Ayak İnfeksiyonu Ön Tanısı Konulan Bir Hasta Nasıl Değerlendirilmelidir?
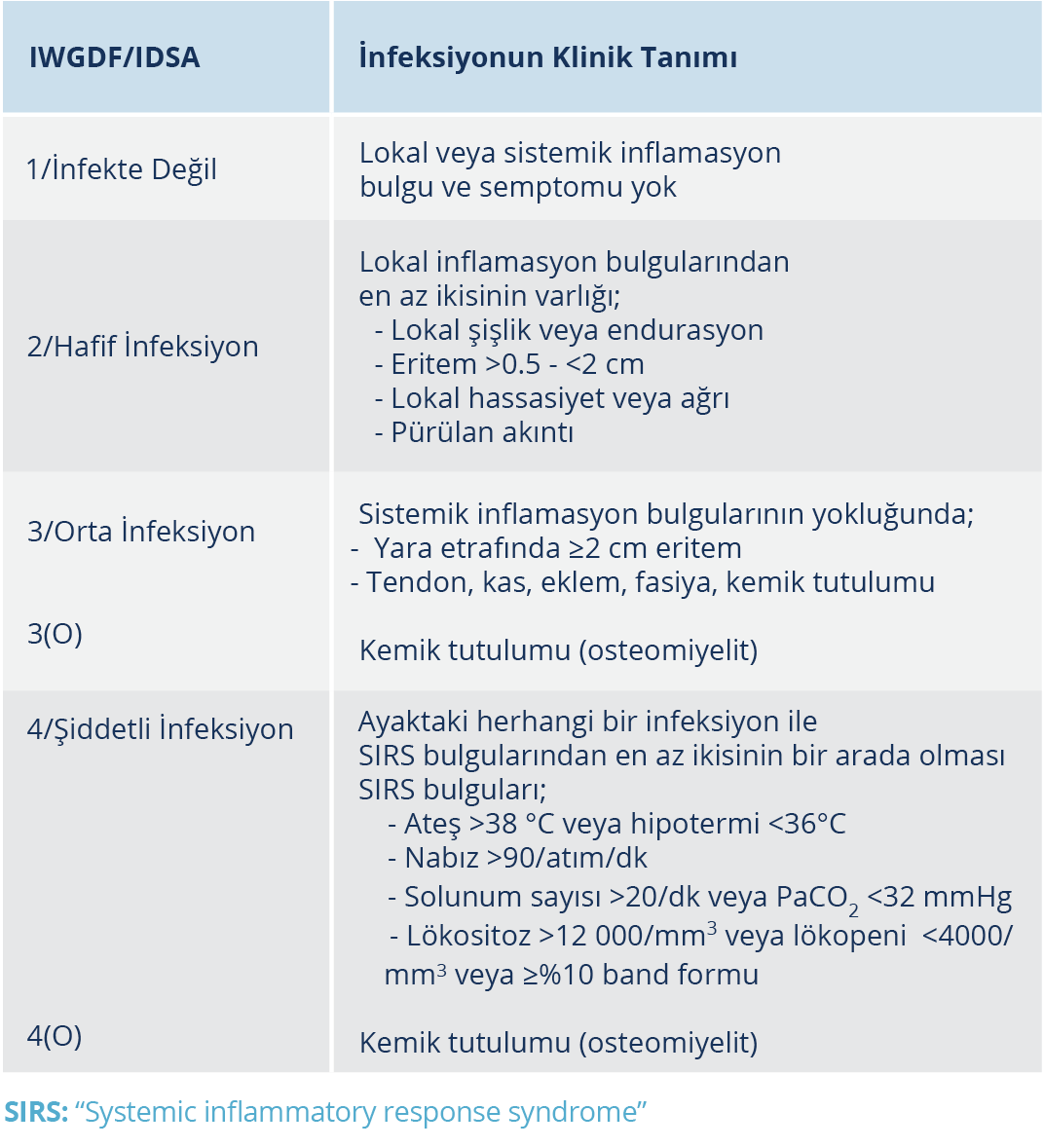
Diyabetik ayak infeksiyonu ön tanısı konulan hastanın ayrıntılı anamnezi alınmalı ve sistemik muayenesi yapılmalıdır. Anamnezde diyabetin tipi, süresi, yaranın başlangıcı, nasıl geliştiği, süresi, daha önce aynı ayakta yara olup olmadığı, ampütasyon, hastane yatış öyküsü, önceki tedaviler sorgulanmalıdır. Muayene sırasında yara bölgesi, tutulan ekstremitenin dolaşım, motor, nöropati değerlendirmesi, diyabetin ek komplikasyonlarının olup olmadığı, yaranın görünümü, boyutu, derinliği, eritem, endürasyon, hassasiyet, ağrı, şişlik, pürülan akıntı, nekroz ve yara bölgesinde yabancı cisim olup olmadığına bakılmalıdır. Yara bölgesinde lokal inflamasyon bulgularına ilave olarak ateş, taşikardi, hipotansiyon gibi sistemik inflamatuar yanıt sendromu (“systemic inflammatory response syndrome”- SIRS) bulgularının varlığı araştırılmalıdır. Lokal infeksiyonlar erken dönemde genelde yüzeyel iken infeksiyonun ilerlemesi ile derin doku, kas, fasiya hatta kemiğe kadar yayılabilir. Yara bölgesinde kızarıklık, şişlik, ısı artışı, ağrı, hassasiyet, >0.5 cm eritem gibi lokal inflamasyon bulgularından en az ikisi veya pürülan akıntı varsa infeksiyon düşünülmeli ve kılavuz önerilerine göre sınıflandırılmalıdır (38-40). Diyabetle ilişkili yumuşak doku infeksiyonlarının tanısı klinik olarak lokal veya sistemik inflamasyonun belirti ve semptomlarının varlığına dayanır. Diyabetik ayak infeksiyonlarının ciddiyetinin değerlendirilmesinde Uluslarası Diyabetik Ayak Çalışma Grubu / Amerikan İnfeksiyon Hastalıkları Derneği (IWGDF/IDSA) sınıflaması kullanılabilir. 2023 yılında güncellenen IWGDF/IDSA Kılavuzu’ndaki infeksiyon sınıflaması Tablo 2’de verilmiştir. Osteomyelit tanı, tedavi ve prognostik sonuçları nedeni ile Evre 3 ve Evre 4 infeksiyon sınıflaması, Evre 3 osteomyelit (O) veya 4 (O) osteomyelit şeklindedir (40).
DERECELENDİRME
Soru 1: Diyabetik Ayak Yarası ve İnfeksiyonlarında Hangi Sınıflama Yeğlenmelidir?
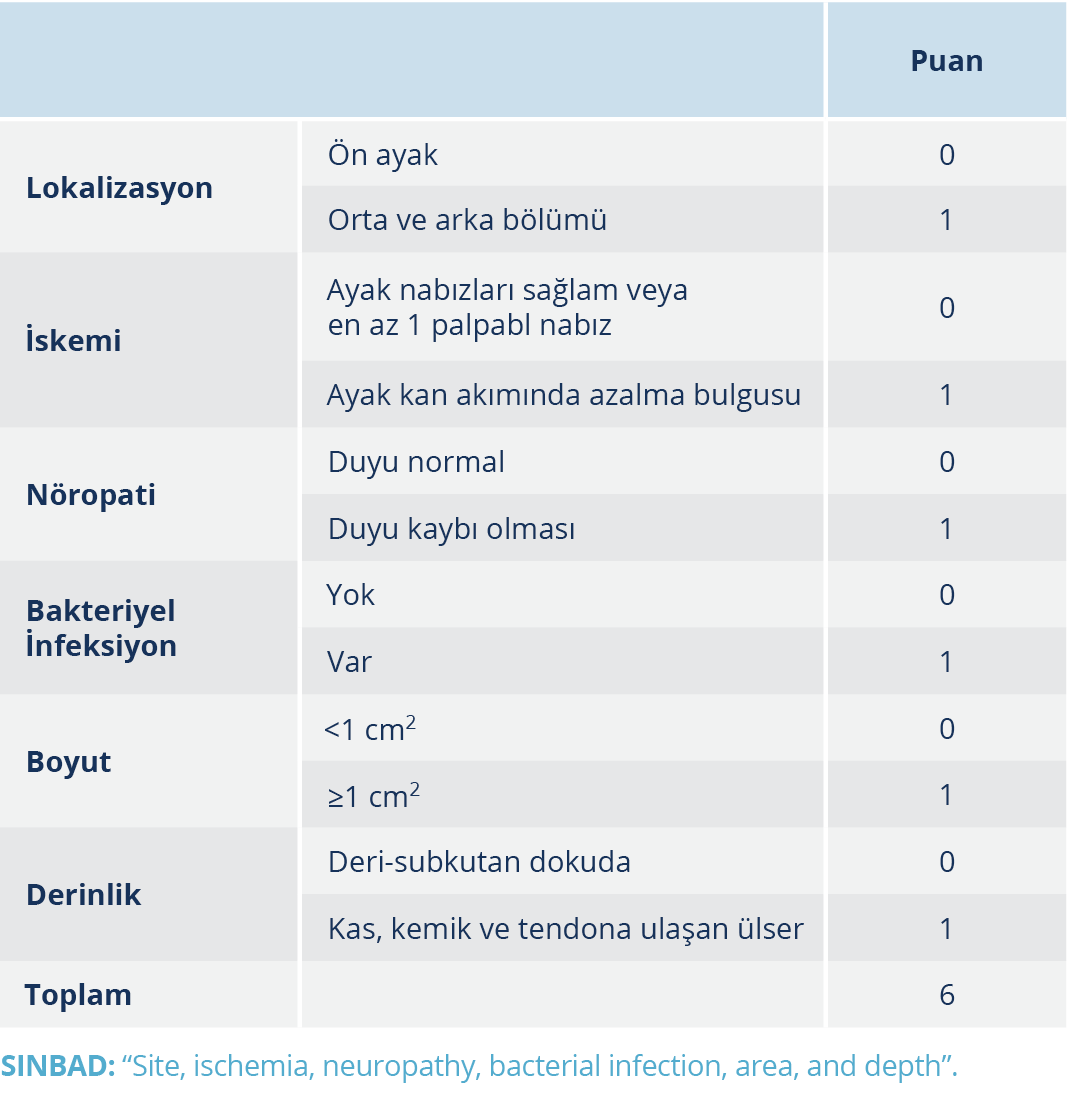
Diyabetik ayak infeksiyonlarının sınıflamaları; ülserin şiddetini derecelendirme, sınıflandırma, riski değerlendirme ve uygun tedavi seçimi için yararlıdır. Diyabetik hastalarda ayaktaki yaraların değerlendirilmesi için yıllar içerisinde farklı sınıflamalar geliştirilmiştir. Bu sınıflamaların bazıları yarayı, infeksiyonu, dolaşımı tek tek değerlendirirken bazılarında yara ile birlikte infeksiyon, nöropati, dolaşım değerlendirilmektedir. Meggitt-Wagner sınıflamasında ülser ve ayaktaki gangren; Texas Üniversitesi sınıflamasında ülser, ülserle beraber infeksiyon, iskemi; “diabetic foot risk assessment” (DIAFORA) sınıflamasında ise ayakla ve ülserle ilgili değişkenler olan nöropati, ayak deformitesi, önceki ülser veya ampütasyon, ülserin sayısı, gangren, infeksiyon ve osteomyelit olup olmadığı değerlendirilmektedir. PEDIS sınıflamasında perfüzyon, yaranın genişlik-derinliği, infeksiyon ve duyu değerlendirilirken, “wound (W), ischemia (I) and foot infection (fI)” – (WIfI) sınıflaması yarayı, iskemi ve infeksiyonu, “site, ischemia, neuropathy, bacterial infection, area, and depth” (SINBAD) sınıflaması ise ülserin yerini, iskemi, nöropati, bakteriyel infeksiyon varlığını ve yaranın derinliğini değerlendirmektedir (41). PEDIS sınıflaması bir önceki uzlaşı raporumuzda önerilen sınıflamadır; söz konusu sınıflama ayağın detaylı değerlendirilmesini sağlamakla birlikte pratikte kullanımı zordur (38). İdeal bir sınıflama sistemi; kolay olmalı, değerlendirmede spesifik bir tetkik ve alet gerektirmemeli, hastanın acilde triajını ve sağlık personeli ile olan iletişimi kolaylaştırmalıdır. Fakat bu özellikleri taşıyan tek bir sınıflama sistemi henüz yoktur. Farklı amaçlar için farklı sınıflamaların kullanımı önerilmektedir. IWGDF’nin 2019 DAİ Tanı-Tedavi Kılavuzu’nda ülserin değerlendirilmesi için bölgesel, ulusal, uluslararası iletişim göz önünde bulundurularak SINBAD sınıflaması önerilmiştir (39). SINBAD sınıflamasında; yaranın boyutu, iskemi, nöropati, bakteriyel infeksiyon olup olmadığı, ülserin yerleşim yeri ve derinliğine göre her bir madde 0 ve 1 arasında puanlanmış ve toplam puan 6 olarak belirlenmiştir (Tablo 3). SINBAD sınıflamasının pratikte kullanımı kolaydır (39,41).
2023’te güncellenmiş olan IWGDF kılavuzunda, ülserin özelliklerinin ve her bir değişkenin varlığı ve yokluğunun değerlendirilmesi amacı ile SINBAD sınıflaması güçlü öneri düşük kanıt düzeyi ile önerilmiştir. Uygun uzmanlık düzeyi ve ek kaynaklar mevcut olduğunda ise ülserin değerlendirilmesi için WIfI sistemi koşullu düşük öneri düzeyi ile önerilmektedir; WIfI sınıflaması ile yara, iskemi ve infeksiyon değerlendirilmektedir (39,41).
Diyabetik ayak ülserli bir hastanın acilde değerlendirilmesinde; kolay bir şekilde ve ekipman ihtiyacı olmadan ülserin boyutunun anlaşılması, infeksiyon ve iskemi olup olmadığının değerlendirilmesi önemlidir. Triajda kullanılacak sınıflama sisteminde; ayak parmak basınç ölçümleri, transkutanöz oksijen basınç ölçümü yapılmadan ayak yarası değerlendirilmeli, PAH şüphesi veya tanısı olduğunda ayak parmak basıncı, transkutanöz oksijen basıncı ölçülebiliyorsa bu ölçümler de yapılmalıdır. SINBAD sınıflaması, hastanın acildeki tiriajını kolaylaştırması, kolay bir şekilde uygulanabilir olması, bir ekipman ihtiyacı olmaması, sağlık profesyonelleri arasında bölgesel, ulusal, uluslararası DA ülserli kişilerin sonuçlarının değerlendirilmesini sağlaması nedeni ile IWGDF kılavuzunda güçlü öneri düşük kanıt düzeyi ile önerilmektedir. Diyabetik ayak ülser ve yara sınıflamaları arasında prognozun değerlendirilebilmesi için kullanılabilecek bir sınıflama yoktur. Periferik arter hastalığı ve iskeminin değerlendirilmesi için WIfI sınıflaması yararlıdır. WIfI sınıflaması transkutanöz oksijen düzeyi, kol bacak indeksi ve bacak sistolik basıncı ölçümlerinin yapılabilmesini sağlayan belli bir uzmanlık gerektirmesi sebebi ile acilde kullanımı kısıtlı olup DA yara sınıflaması için koşullu düşük öneri düzeyi ile önerilmektedir (41).
Bu uzlaşı raporunda DA yara değerlendirmesi için cihaz, ekipman gereksinimi olmadan kolay bir şekilde uygulanabilmesi nedeni ile SINBAD sınıflamasını, infeksiyon durumunu değerlendirmek içinse 2023 IWGDF/IDSA sınıflamasını öneriyoruz (40,41).
DİYABETİK AYAK TANI TESTLERİ
Soru 1: Diyabetik Ayak Yarası Olan Hastada Yara Kültürü Örnekleri Ne Zaman ve Nasıl Alınmalıdır?
Diyabetik ayak ülseri olan hastalarda yarada infeksiyon bulgusu yoksa kültür örneği alınmamalıdır. Yara bölgesinde kızarıklık, şişlik, hassasiyet, ağrı, akıntı gibi lokal infeksiyon bulgusu varsa ve mümkünse antibiyotik başlamadan önce derin doku, aspirasyon veya biyopsi yöntemi ile kültür örneği alınmalıdır. Örnek almadan önce yara bölgesi steril serum fizyolojikle yıkanmalı veya silinmeli, yabancı cisim nekrotik doku varsa uzaklaştırıldıktan sonra örnek alınmalıdır. Pürülan akıntı varsa aspirasyon ile örnek alınması tercih edilmelidir. Kolonizan bakterileri ya da normal deri florasını yansıtabileceğinden sürüntü yöntemi ile kültür örneği alınmamalıdır (38,41,42). Kemik infekte ise ve örnek alınması uygunsa yumuşak doku ve kemikten eş zamanlı kültür için örnek alınmalıdır.
Soru 2: Diyabetik Ayak İnfeksiyonu Olan Hastalarda Ne Zaman Kan Kültürü Alınmalıdır?
Diyabetik ayak infeksiyonu olan hastada lokal yara infeksiyonu bulguları ile birlikte SIRS bulgularından en az ikisi varsa veya septik tabloda organ yetmezlik bulguları varsa kan kültürü de alınmalıdır (38).
Soru 3: Diyabetik Ayak İnfeksiyonu Düşünülen Hastalarda Kan Testlerinin Tanıdaki Yeri Nedir ve Hangi Testler İstenmelidir?
Lökosit sayısı, C-reaktif protein (CRP), eritrosit sedimantasyon hızı (ESH) ve prokalsitonin gibi inflamasyon biyobelirteçleri DAİ tanısında yardımcı testler olarak kullanılmaktadır. Lökositoz veya lökopeni SIRS kriteri olarak şiddetli infeksiyonda yer almakla beraber bazı çalışmalarda lökosit sayısının infeksiyon şiddeti ile korele olmadığı ve DAİ hastalarının yaklaşık yarısında lökosit sayısının normal olduğu bulunmuştur. CRP değerinin, ayakta infeksiyonu olan olgularda infeksiyon olamayanlardan ve diyabetik ayak ülserli hastalarda ülseri olmayan hastalardan daha yüksek olduğu ve şiddetli infeksiyonlarda daha yüksek düzeyleri olduğu gösterilmiştir. Çalışmaların çoğunda ESH infekte DA olgularında infekte olmayanlardan daha yüksek bulunmuştur; ESH infeksiyon dışında anemi, azotemi gibi bazı faktörlerden etkilenmesine rağmen, ≥70 mm/saat ise DA osteomyeliti tanısı açısından %81 duyarlılık ve %80 özgüllük ile kullanılan bir belirteçtir. CRP, ESH ile karşılaştırıldığında infeksiyon varlığında daha erken yükselir ve infeksiyonun iyileşmesi ile daha erken düşer. Prokalsitonin de infekte DA’larda daha yüksek olmakla beraber infeksiyonun şiddeti ile korelasyonunun daha az olduğu bildirilmiştir (38,43-45). 2023 yılı IWGDF/IDSA kılavuzunda; klinik olarak infeksiyon tanısı konulamadığı durumlarda CRP, ESH ve prokalsitoninin tanıda kullanılması önerilmektedir (40).
Soru 4: Diyabetik Ayak İnfeksiyonu Tanısı Alan Hastada Hangi Görüntüleme Yöntemi Ne Zaman Kullanılmalıdır?
Görüntüleme yöntemleri, DAİ tanısında kemik tutulumu, yumuşak doku-fasya tutulumlarının değerlendirilmesi açısından faydalıdır. Öncelikle üç yönlü direkt ayak grafisi çekilmelidir; böylelikle infeksiyonun yanı sıra kemik deformiteleri-kırık, radyoopak yabancı cisimler ve yumuşak dokudaki gaz oluşumları da saptanabilir. Kronik osteomyelit tanısında da yararlı olmakla birlikte akut ostemyelitte erken dönemde direkt grafide bulgu olmayabilir. Erken dönem osteomyeliti, tedaviye yanıt alınamayan osteomyelit ya da derin yumuşak doku apsesi düşünülen hastalarda manyetik rezonans görüntüleme (MRG) daha duyarlı ve daha özgüldür; MRG’nin kontrendike olduğu ya da çekilemediği hastalarda işaretli lökosit sintigrafi ve diğer radyonüklid kemik taramaları yararlıdır. Ultrasonografi (USG), tomografi ve pozitron emisyon tomografi (PET) de son yıllarda DAİ tanısındaki görüntüleme seçenekleri arasında yer almaktadır (38,46,47).
OSTEOMYELİT
Soru 1: Diyabetik Ayak Osteomyeliti Ne zaman Düşünülmeli, Tanısı Nasıl Konmalıdır?
Osteomyelit diyabetik ayak ampütasyonlarının önemli bir nedenidir ve bir ayak infeksiyonunda osteomyelit olması ampütasyon riskini yaklaşık altı kat artırmaktadır (12). Diyabetik ayak osteomyelitinin bu özgül durumu nedeniyle son IWGDF/IDSA kılavuzundaki sınıflamada osteomyelit Evre 3 ve 4’te ayrı bir alt grup olarak tanımlanmıştır (40). Ancak günümüzde hala osteomyelit tanısında tam bir uzlaşı bulunmamaktadır. Diyabetik ayak infeksiyonu olan bir hastada yüksek ateşin olmaması ya da ülser üzerinde inflamasyon bulgularının olmaması infeksiyonu ve osteomyeliti dışlamaz (48). Osteomyelit tanısı için ilk dikkat edilmesi gereken durum hastanın öyküsü ve fizik muayenesidir. Ayak yarası olan diyabetik hastada önceden ayak ülseri öyküsü, daha önce hastanede yatış, uzun süreli diyabetik ayak infeksiyonu, daha önce antibiyotik kullanımı, ampütasyon öyküsü varsa osteomyelit olasılığı akılda tutulmalıdır (48-52). Fizik muayenede yara genişliğinin 2 cm’den büyük olması ve yara derinliğinin 3 mm’den fazla olması osteomyelit riskini artıran göstergelerdir (45,50,53-55). Yapılan çok merkezli bir çalışmada, yara büyüklüğünün 4.5 cm2’nin üzerinde olmasının osteomyelit olasılığını üç kat artırdığı gösterilmiştir (12).
Soru 2: Osteomyelit Tanısında Hangi Laboratuvar Bulguları Yardımcıdır?
Kan Testleri
Laboratuvar göstergeleri içinde osteomyelit için en önemli belirteç ESH’dir (48). Birçok çalışmada ESH’nin 70 mm/saat’in üzerinde olmasının osteomyelit tanısı için iyi bir gösterge olduğu bildirilmiştir (45,50,53,54,56). Özellikle fizik muayenede yara yüzeyi genişliğinin 2 cm2’nin üzerinde olması ile ESH birlikteliği, osteomyelit tanısı için ileri görüntüleme incelemelerinden daha iyi duyarlılık ve özgüllüğe sahiptir (50). ESH’nin bu özelliğine karşın diğer inflamatuar göstergelerden CRP ve prokalsitonin ostemiyelit tanısında yardımcı göstergeler değildir (45,50,54,56).
Görüntüleme Yöntemleri
Diyabetik ayak infeksiyonu yakınması olan hastalarda öykü ve fizik muayenede osteomyelit şüphesi olduğunda ilk istenecek radyolojik inceleme düz ayak filmi olmalıdır. Akut osteomyelit için bu filmlerde görülen klasik üç bulgu, demineralizasyon, periost reaksiyonu ve kemik yıkımıdır; bu bulgular genellikle osteomyelitin 2-3. haftasından sonra kemiğin %40-50 kaybı sonrası düz filmlerde görünür olabilir (48,56). En az iki haftalık antimikrobiyal tedaviye klinik ve laboratuvar yanıtın yetersiz ve osteomyelit şüphesinin yüksek olduğu durumlarda ise akut osteomyelit tanısında kullanılabilecek görüntüleme yöntemi öncelikle MRG ya da çekilemediği durumlarda 3 ve /veya 4 fazlı ve ardından işaretli lökosit ile çekilmiş kemik sintigrafisidir. Manyetik rezonans görüntülemenin sintigrafiye göre en önemli avantajı, osteomyelit için yapılacak cerrahi girişim için yumuşak dokuda cerrahi sınırları daha iyi gösterebilmesidir (48). Bu hastalarda ayrıca dikkat edilmesi gereken bir durum da akut Charcot nöroosteoartropatisi (CN)’nin ostemiyelitle karışmasıdır; CN ile osteomyelit ayırıcı tanısında sintigrafi MRG’ye göre daha iyi sonuç vermektedir (56,57). Akut CN genellikle tarsometatarsal eklemi tutar, deri bütünlüğü bozulmamıştır ve derin dokuda minimal değişiklik vardır; kemikte reaktif ödem ve kaba fragmantasyon görülür (48). Ülkemizde yakın zamanlı olarak gerçekleştirilen iki çalışmada bu hastaların arteriyel dolaşımının durumunu saptamak amacıyla yapılan manyetik rezonans anjiyografi (MRA) işlemi sırasında CN olan hastaların görüntülerinde istatistiksel olarak anlamlı düzeyde venöz kontaminasyon saptandığı ve bunun CN için özgül bir bulgu olabileceği bildirilmiştir (58,59).
Kemik Biyopsisi
Bazı durumlarda osteomyelit tanısı, yalnızca ameliyat sırasında veya perkütan biyopsi ile elde edilen bir kemik örneğinin incelenmesiyle doğrulanabilir. Uluslararası rehberlerin osteomyelit tanısında uzlaştığı tek altın standart kemiğin hem kültüründe üreme olması hem de histopatolojik incelemesinde pozitif sonuçlar elde edilmesidir (60). Ancak kemik biyopsisi her zaman yapılabilecek bir girişim değildir. Karakteristik histolojik bulgular arasında inflamatuar hücre kümeleri (nötrofiller, lenfositler, histiyositler ve plazma hücreleri), trabeküler kemik erozyonu, fibrozis ve reaktif kemik oluşumu dahil kemik iliği değişiklikleri yer alır (56). Osteomyelit tanısında tek başına kemik kültürünün duyarlılığının %92, özgüllüğünün %60 olduğu bildirilmiştir. Kemik kültürünün en büyük avantajı, neden olan patojen(ler)i tanımlamanın tek yöntemi olması, böylece antibiyotik duyarlılıklarının belirlenmesine ve tedavinin doğru hedeflenmesine olanak sağlamasıdır (52,61). Yumuşak dokudan alınan örnekler her zaman kemik infeksiyon etken veya etkenlerini içermeyebilir. Ülkemizde yapılan bir çalışmada 10 hastadan birinde kemik doku kültürü ile yumuşak doku kültür sonuçları arasında farklılık olduğu gösterilmiştir (62). Bu nedenle yapılan debridmanlar sırasında olanaklı ise hem yumuşak dokudan hem de kemik dokudan ayrı örnekler alınmalı ve kemik doku örnekleri hem mikrobiyolojik hem de histopatolojik olarak incelenmelidir. IWGDF/IDSA kılavuzunda DA osteomyeliti şüphesinde tedaviden önce veya sonra intraoperatif veya perkütan olarak yumuşak doku yerine kemik dokudan örnek alınması önerilmektedir (40).
DİYABETİK AYAK İNFEKSİYONUNDA TEDAVİ
Genel İlkeler
Soru 1: Diyabetik Ayak İnfeksiyonunda Tedavi Hedefleri Nelerdir?
Yara iyileşmesini sağlayabilmek ve ayağı kurtarmak için genel tedavi yaklaşımı aşağıda verilmiştir (38):
- Tüm nekrotik dokular ve çevredeki kallusların debride edilmesi, yara temizlenmesi ve uygun yara bakımı,
- Kültür için uygun doku örneği alımı ve uygun antibiyotik tedavisi,
- Metabolik kontrol,
- Ayağın yükten ve basıdan kurtarılması (“off-loading”),
- PAH’ın tanısı ve uygun şekilde tedavisi,
- Ayağın işlevinin kazandırılması (rekonstrüksiyon).
Soru 2: Diyabetik Ayak İnfeksiyonu Olan Hangi Hastalar Hastanede İzlenmelidir?
Şiddetli infeksiyonu ve bazı orta şiddetli infeksiyonu olan hastalar, metabolik ve hemodinamik açıdan stabil olmayan hastalar, ayaktan tedavinin yetersiz kaldığı veya ayaktan tedaviye uygun olmayan hastalar, tanısal testlerin hastanede yatmayı gerektirdiği durumlar, özellikli yara bakımı gerekliliği, ciddi PAH varlığı ve cerrahi işlem gerekliliği, psikolojik veya sosyal nedenlerden dolayı evde bakımı yapılamayan hastalar hastaneye yatırılarak tedavi edilmelidir (40).
Soru 3: Hastaneden Taburcu Edilme Ölçütleri Ne Olmalıdır?
Hastanın taburcu edilmeden önce klinik olarak stabil olması, herhangi bir acil cerrahi müdahale gereksiniminin olmaması, glisemik kontrolünün sağlanmış olması, kullanılacak antibiyotiklerin planlanmış olması, ayağın yükten kurtarılması ve özgül yara bakımının uygulanmış olması gerekir. Bu koşullarda taburcu edilen hastanın ayaktan izlenmesine de devam edilir (38).
Soru 4: Diyabetik Ayak Yumuşak Doku İnfeksiyonu Olan Hastada Mortalite Açısından Risk Faktörleri Nelerdir?
Diyabetik ayak infeksiyonu başlı başına mortaliteyi artırmaktadır. Bununla birlikte, ileri yaş, kontrolsüz diyabet, diyabetik nöropati, kardiyovasküler hastalıklar gibi altta yatan komorbid durumların varlığı ve mikrobiyolojik etkenler de mortalitenin artmasında rol oynayabilir (40). Ülkemizde yürütülen çok merkezli bir çalışmada, mortalite için risk faktörleri olarak tespit edilenler; kronik kalp yetersizliği, kronik diyaliz alımı ve doku kültüründe Klebsiella türlerinin izolasyonudur (18). Major ampütasyon, tekrarlayan infeksiyon ve ölümün dahil edildiği bileşik olumsuz sonuçların değerlendirildiği bazı çalışmalarda da hastalık şiddeti, çoklu antibiyotiğe dirençli Gram-negatif bakteriler, polimikrobiyal infeksiyon varlığı risk faktörleri olarak bildirilmiştir (19,21,22).
Soru 5: Diyabetik Ayak İnfeksiyonu Olan Hastalarda Ne Zaman ve Kimden Konsültasyon İstenmelidir? Diyabetik Ayak Tedavisinde Ekip Çalışmasının Önemi Nedir ve Nasıl olmalıdır?
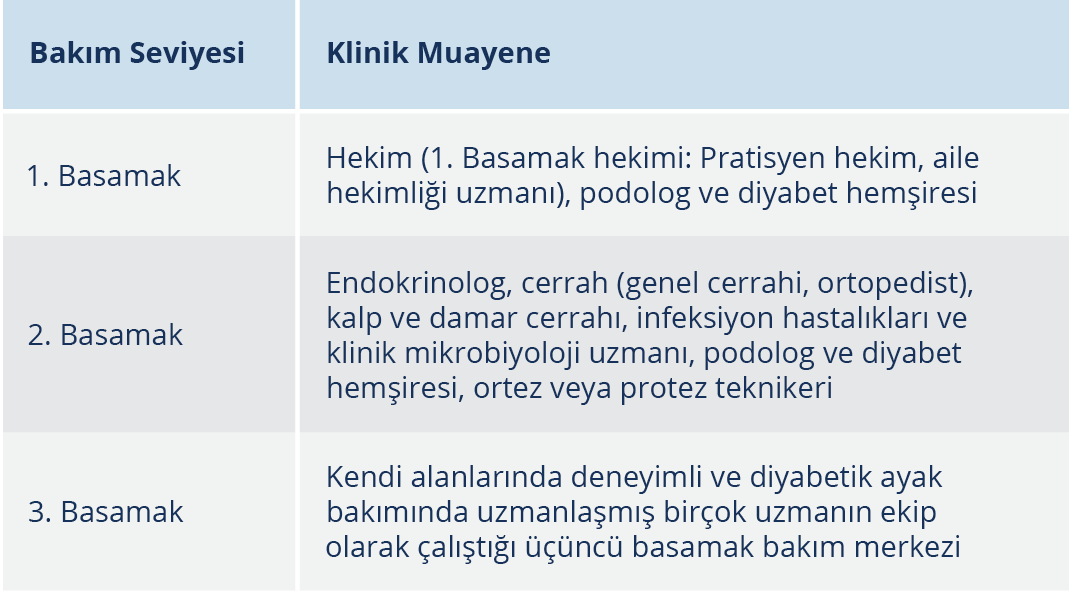
Diyabetik ayak infeksiyonunun gelişiminde rol oynayan faktörlerin çok farklı olması, gelişen lezyonları karmaşık hale getirmekte ve tedavide farklı disiplinlerin katkı sağlamasını gerektirmektedir. Bu nedenle diyabetik hastalarda; ayak yarası ve infeksiyonunun gelişimini önlemek, gelişen yaraların erken tedavisini gerçekleştirebilmek, infeksiyon gelişmesi durumunda tedavideki başarıyı artırmak, infeksiyonla ilişkili morbidite insidansını azaltmak, tedavi yaklaşımlarını daha etkin kılmak, majör ampütasyonları, tedavi maliyetlerini ve hastaların yatış sürelerini azaltmak amacıyla ekip çalışması yapılmasının uygun olacağı düşünülmektedir (38,40,45,63,64). Ülkemizde Sağlık Bakanlığı Tedavi Hizmetleri Genel Müdürlüğünce hazırlanmış olan Diyabet Eylem Planı’nda da bu hastaların etkin tedavisi için ilgili ekip çalışmasının gerekliliği vurgulanmış olup üçüncü basamak hastanelerde DA kurullarının (endokrinoloji ve metabolizma hastalıkları uzmanı, iç hastalıkları uzmanı, infeksiyon hastalıkları ve klinik mikrobiyoloji uzmanı, deri ve zührevi hastalıklar uzmanı, ortopedi ve travmatoloji uzmanı, fiziksel tıp ve rehabilitasyon uzmanı, kalp ve damar cerrahisi uzmanı, plastik rekonstrüktif ve estetik cerrahi uzmanı, radyoloji uzmanı, DA kurulu hemşiresi, fizyoterapist, diyetisyen, vb. içerecek şekilde) kurulmasının hedeflendiği açıkça belirtilmektedir (65, 66). Diyabetik ayak, kronik yaranın en önemli sebepleri arasındadır. Sağlık Bakanlığı Sağlık Hizmetleri Genel Müdürlüğünün hazırlamış olduğu kronik yara bakım hizmetlerinin uygulanmasına dair yayımlanan son genelge ile birinci basamak kronik yara bakımı; sadece deri ve deri altının etkilendiği, yağ ve derin dokuların etkilenmediği yaralar olarak tanımlanmış ve bu hizmetin bir hekim ve hemşirenin görev yaptığı, pansuman odası bulunan sağlık merkezlerinde uygulanabileceği belirtilmiştir. İkinci basamak kronik yara bakımı; yumuşak dokuların etkilendiği, basit cerrahi girişimler (debridman, abse drenajı, minör amputasyolar) ile infeksiyon ve nekrozun kontrol edilmesini takiben yine basit cerrahi işlemlerle veya medikal olarak kapanabilecek yaraların takip ve tedavisinin yapılabildiği hizmetler olarak tanımlanmış ve bu hizmetin ilgili uzman hekim ve ameliyathane şartları bulunan yataklı sağlık tesislerinde verilmesi gerektiği belirtilmiştir. Birinci ve ikinci basamak kronik yara bakım hizmetlerinden en az birinin tüm sağlık merkezlerinde verilmesi gerektiği vurgulanmıştır. Kronik yara bakım ünitelerinin ise gerekli asgari koşullara sahip sağlık merkezlerinde bakanlıkça planlanacağı belirtilmiştir (67). Hastaların interdisipliner olarak değerlendirileceği ekipler bu konuda deneyimli sağlık çalışanlarından oluşmalı, hastayı izlemeli ve ayaktan/yatan hasta için gereken bakımı/konsültasyon hizmetini vermeli ve belirlenen aralıklarla konseyler düzenlemelidir. Ekipte yer alan uzmanlar hastanenin özelliklerine göre değişebilmekle birlikte en az üç dal (infeksiyon hastalıkları ve klinik mikrobiyoloji uzmanı, DA konusunda deneyimli bir cerrah ve endokrinoloji ve metabolizma hastalıkları/iç hastalıkları uzmanı) yer almalıdır. Konsey sorumlu hekimin başkanlığında ilgili uzmanların katılımı ile oluşturulmalıdır. Önemli bir iskemi olduğunun klinik ve tanısal belirtileri varsa, vasküler cerrah, hastayı revaskülarizasyon açısından değerlendirmelidir. Gerektiğinde basınç azaltma yöntemleri için de konsültasyon istenmelidir. Konseyin haftanın belli günlerinde toplanarak hastalara uygulanacak tedavilere karar vermesi ekip çalışmasını daha da pekiştirmesi açısından son derece önemlidir.
ANTİBİYOTİK TEDAVİSİ
Soru 1: Diyabetik Ayak İnfeksiyonlarında Antibiyotik Tedavisi İlkeleri Nasıl Olmalıdır?
Bu kılavuzun amacı, diyabetik ayak infeksiyonlarının ciddiyetinin ve olası patojenlerin değerlendirilmesine dayalı olarak uygun ampirik antibiyotik tedavisinin seçiminde yardımcı olmaktır. Antibiyotik tedavi süresi, doku veya kemik tutulumunun boyutu, cerrahi müdahale gereksinimi ve tedaviye verilen yanıtla ilişkilidir.
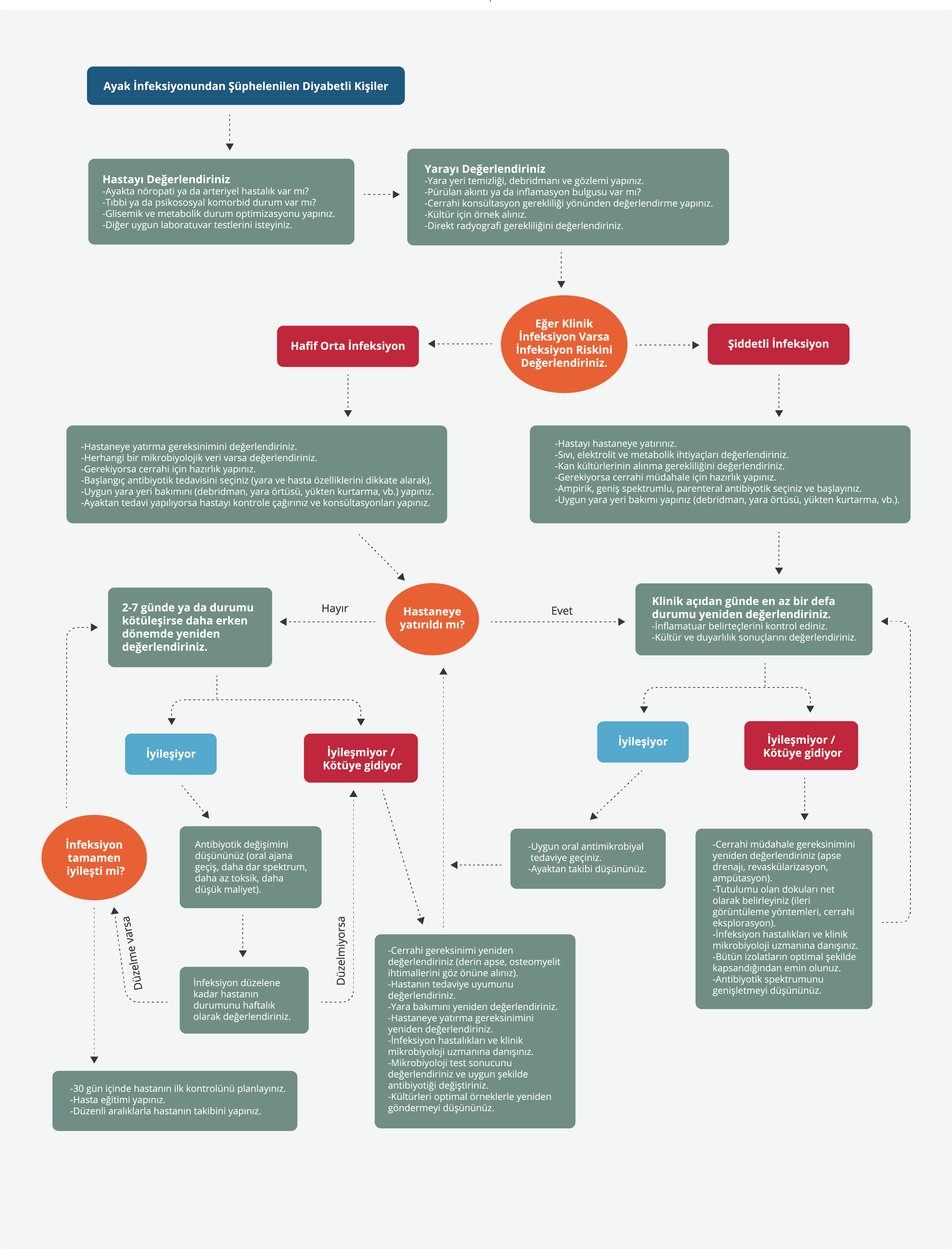
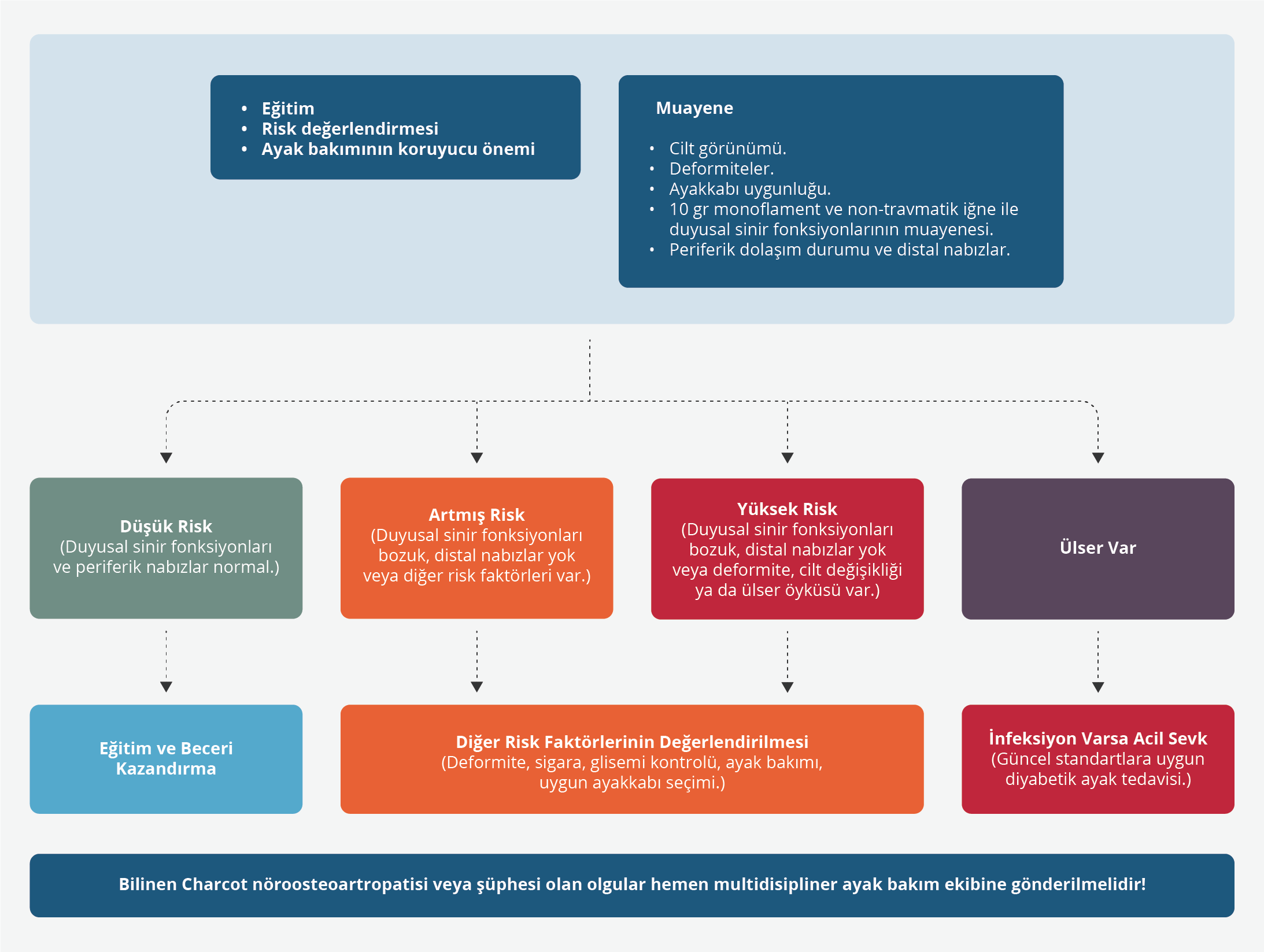
Diyabetik ayak infeksiyonları, diyabetli hastaların önemli morbidite nedenlerinden biri olup artmış ampütasyon veya mortalite riskinden dolayı hemen tedavi edilmesi gerekir (14). Ayak infeksiyonunun tedavisinde, infeksiyon şiddetinin belirlenmesi amacıyla tutulan dokuların derinliği-kapsamı ve sistemik toksisitenin değerlendirilmesi, arteriyel perfüzyonun yeterliliğinin gözden geçirilmesi, olası revaskülarizasyon ihtiyacı dikkate alınır (38,40,45,68). Şekil 3’te ayak infeksiyonundan şüphelenilen diyabetli bireylere yaklaşım özetlenmiştir.
Antibiyotiklerin yaranın iyileşmesini hızlandırdığına dair yayınlanmış bir kanıt bulunmadığından ve gereksiz antibiyotik kullanımı antibiyotik direnci riskini artırdığından, infekte olmayan yaralar için antibiyotik kullanılmamalıdır. Antibiyotik tedavisi lokal ya da sistemik bir diyabetik ayak infeksiyonunda başlanmalıdır. Şiddetli infeksiyon veya yaygın gangren, nekrotizan infeksiyon, derin apse belirtileri (fasyanın altında) veya kompartman sendromuyla komplike orta şiddetli infeksiyon, ciddi alt ekstremite iskemisi olan hastaların tedavisinin başlangıcında acilen ayakla ilgilenen bir cerrahi uzmanına danışılmalıdır. Ampirik antibiyotik seçiminde klinik ve epidemiyolojik veriler dikkate alınmalıdır. Varsa önceki kültür sonuçları, patojenlerin yerel prevalansı, özellikle de antibiyotiklere dirençli bakterilere ilişkin yerel veriler değerlendirilmelidir. Kesin tedavi infekte dokunun kültür sonuçları esas alınarak düzenlenmelidir. Kesin tedavide hastanın klinik tedaviye vermiş olduğu yanıt değerlendirilmeli, bunun yanı sıra uygun alınmış örneklerin antibiyotik duyarlılık sonuçlarına bakılmalı, kesin tedaviye geçildiğinde tedavi süresi yeniden gözden geçirilmelidir. Çeşitli antibiyotik tedavi rejimlerinin sonuçlarını karşılaştıran sınırlı sayıda yayınlanmış veri vardır. Ampirik tedaviye yaranın ciddiyeti ve olası mikroorganizmalar düşünülerek karar verilmelidir; kültür ve duyarlılık sonuçlarına göre daha dar bir kapsama geçilerek tedavi değişikliği yapılması önerilir (69,70).
Soru 2: İnfeksiyon Şiddetine Göre Antibiyotik Seçimi Nasıl Olmalıdır?
Daha önce tedavi edilmemiş bir hastada hafif akut infeksiyona genellikle aerobik Gram-pozitif koklar neden olur; ancak daha derin veya kronik yaralarda etkenler genellikle aerobik Gram-negatif ve zorunlu anaerobik bakterileri içerecek şekilde polimikrobiyaldir.
Antibiyotik seçimi öncesinde hafif infeksiyonu olan hastalarda yara kültürü genellikle gerekli değildir. Yakın zamanda antibiyotik tedavisi almamış ve ılıman bir iklim bölgesinde yaşayan, hafif şiddette diyabetik ayak infeksiyonlu olgularda sadece aerobik Gram-pozitif patojenlere (beta hemolitik streptokoklar ve S. aureus) yönelik ampirik antibiyotik tedavisi başlanmalıdır (38,68).
Orta/ şiddetli diyabetik ayak yumuşak doku infeksiyonunda, tedavi öncesinde ülserden, asepsiye dikkat edilerek kültür için doku örneği (küretaj veya biyopsi) alınmalıdır. Özellikle ÇİD olan patojen riski yüksekse uygun örneğin antibiyotik tedavisi öncesinde alınması ihmal edilmemelidir.
Orta/şiddetli diyabetik ayak infeksiyonlarının çoğu polimikrobiyaldir ve olası patojenler ayak yarasının süresi ve yaranın özelliğine göre değişir. Ülkemizde, birkaç hafta içerisinde antibiyotik tedavisi almış, kronik infekte, ayağı ciddi iskemik, orta / şiddetli diyabetik ayak infeksiyonu olan hastalarda; ampirik tedavinin Gram-pozitif patojenleri kapsayan antibiyotik rejimine ek olarak yaygın olarak izole edilen Gram-negatif patojenlere yönelik antibiyotiklerle başlanılması, nekroz varsa ilave olarak tedavinin olası zorunlu anaerobları da içermesi önerilir (Tablo 4).
Şiddetli infeksiyonda yara kültür sonuçları çıkana kadar ampirik tedavi başlanır; ancak kültür sonuçlarına göre tedavi gözden geçirilmelidir. Ampirik tedavide yalnızca etken olabilecek bakterilerin kapsanması hedeflenmelidir; yeterli doku düzeyi, düşük yan etki ve hasta uyumu gözetilmeli, etkin ilaçlar belirlenmiş dozlarda ve sürede kullanılmalıdır. Diyabet ilişkili böbrek hastalığı; tahmini glomerüler filtrasyon hızı (“estimated glomerular filtration rate” – eGFR) <60 ml/dak/1.73m2 ve/veya kalıcı albüminüri veya proteinüri olarak tanımlanır. Antibiyotik kullanımında doz seçiminde e-GFR mutlaka hesaplanmalı ve hastanın antibiyotik doz ayarlaması yapılmalıdır. Nefrotoksik etkisi nedeni ile vankomisin ve aminoglikozid grubu ajanların seçiminde dikkatli olunmalıdır.
Soru 3: Antipseudomonal Tedavi Ne Zaman Tercih Edilmelidir?
Masere ülserlerde, ayak ıslak kaldığında, diğer su veya nemli ortamlara maruz kalma durumlarında P. aeruginosa riski artar. Birkaç hafta önceki kültürlerinde Pseudomonas izole edilmiş, subtropik/tropik bölgelerde yaşayan, orta /şiddetli infeksiyonu olan olgularda Pseudomonas spp. etken olarak düşünülmelidir. Ülkemizde yapılan çalışmalarda DAİ’lerde etken olarak Pseudomonas spp.’nin izole edilme oranı yüksek olup stafilokoktan sonra ikinci sırada yer alan bakterilerdir. Pseudomanas spp.’de ÇİD oranı da yüksek (%30) bulunmuş olup bu durum tedavi yetersizliği nedeni ile daha yüksek mortalite/ampütasyona neden olmaktadır (14,38).
Soru 4: Diyabetik Ayak İnfeksiyonlarının Ampirik Tedavisinde MRSA Etkili Antibiyotik Ne Zaman Kapsanmalıdır?
Geçmiş bir yıl içinde MRSA infeksiyonu veya bilinen kolonizasyon öyküsü olanlarda, son zamanlarda hastaneye yatış veya uzun süreli bir bakım tesisinde kalanlarda MRSA’ya bağlı infeksiyon gelişme riski yüksektir. Şiddetli diyabetik ayak infeksiyonunda veya hastanın MRSA infeksiyonu için riski söz konusu ise (yakın zamanda hastane yatışı, diyalize girme, önceki stafilokok infeksiyonu ya da kolonizasyonu vb.) kesin kültür ve duyarlılık sonuçları çıkana kadar MRSA’ya etkili antibiyotik düşünülmelidir (45).
Soru 5: Diyabetik Ayak İnfeksiyonlarının Ampirik Tedavisinde Çoğul İlaç Dirençli Bakteri İnfeksiyonlarına Etkili Antibiyotik Eklenmesi Ne Zaman Düşünülmelidir?
Bu bakteriler, aynı ayaktaki yara için daha önce hastaneye yatış öyküsü olan hastaların 1/3’ünde, osteomyeliti olan hastaların ise %25’inde izole edilir. Önceden kolonizasyonu olan hastalarda yaraya yeterince nüfuz edemeyen antibiyotiklerin kullanılması da bu bakterilerle infeksiyon gelişmesine neden olabilmektedir (71). Diyabetik ayak infeksiyonu sürveyansı ile çoğul ilaç dirençli baktreiler (GSBL oluşturan bakteriler, Acinetobacter gibi) tespit edilmeli, kolonize-infekte ayrımı yapıldıktan sonra, antibiyograma uygun tedavi açısından hasta değerlendirilmelidir (22,72).
Soru 6: Diyabetik Ayak İnfeksiyonunda Hangi Antibiyotikler Seçilmelidir?
Diyabetik ayak infeksiyonlarında, yumuşak doku veya kemik infeksiyonunu tedavi etmek için herhangi bir özel antibiyotik rejiminin (spesifik ajan(lar), yol, süre) diğerlerinden daha iyi olduğuna dair kesin bir kanıt yoktur (70). Yapılan çalışmalarda, farklı evrelerdeki DAİ’lerde kullanılan antibiyotik rejimleri arasında klinik sonuçlar açısından önemli fark bulunmamıştır (73-91).
Tedavi seçiminde; olası veya kanıtlanmış patojenler ve bunların antibiyotik duyarlılıkları, infeksiyonun klinik şiddeti, ajanın diyabetik ayak için etkinliğine dair yayınlanmış kanıt, kolateral hasar da dahil olmak üzere olumsuz olay riski, komensal flora, ilaç etkileşimi olasılığı, ajanın kullanılabilirliği ve finansal maliyetler dikkate alınmalıdır.
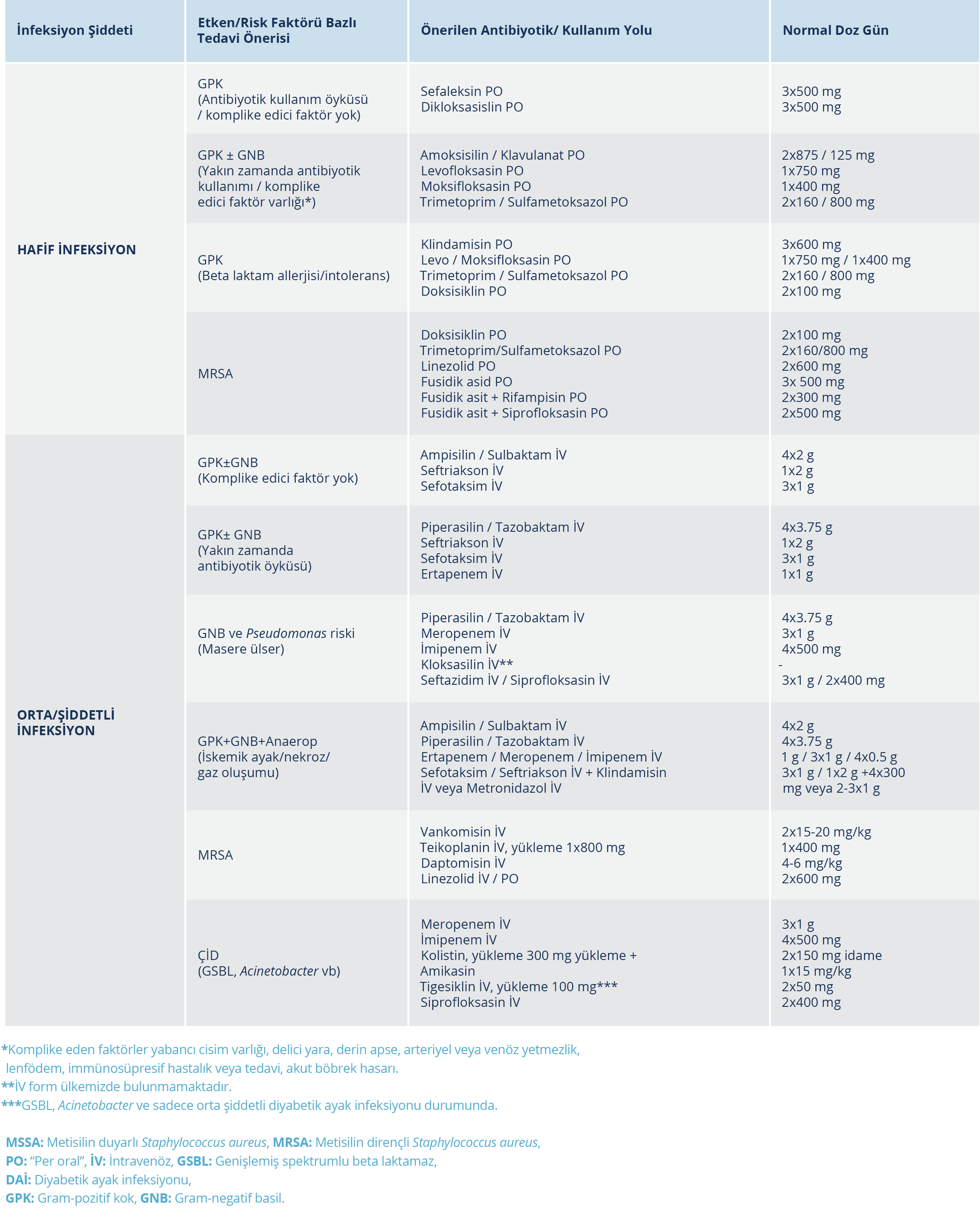
Seçilmesi önerilen bazı ajanlar arasında β-laktam antibiyotikler (penisilinler, sefalosporinler, piperasilin/tazobaktam, karbapenemler), klindamisin, florokinolonlar, MRSA için etkili ajanlar (linezolid, daptomisin, vankomisin, teikoplanin) ve diğer antibiyotikle birlikte metronidazol yer almaktadır (Tablo 4).
Hafif infeksiyon için ilk seçenek olarak oral anti-stafilokokal etkili β-laktam antibiyotikler (sefaleksin, dikloksasilin, amoksisilin-klavulanat v.b) önerilir. β-laktam alerjisi/intoleransı mevcutsa alternatif tedavi olarak klindamisin, kotrimoksazol, doksisiklin, levofloksasin/moksifloksasin önerilir. MRSA riski olan hastalarda oral kotrimoksazol, linezolid ya da fusidik asid+kinolon veya rifampin verilebilir. Duyarlı olduğu gösterilen MRSA suşlarına karşı klindamisin de önerilir.
Sistemik ve yaşamı tehdit eden şiddetli infeksiyonlarda psödomonasa etkili bir penisilin+β-laktamaz inhibitörü (piperasilin- tazobaktam) veya bir karbapenem (imipenem/meropenem gibi) veya psödomonasa etkili bir sefalosporin (sefepim veya seftazidim) + MRSA’ya etkili ajanla (daptomisin, linezolid, teikoplanin ya da vankomisin) tedaviye başlanmalıdır (38,40,86). β-laktam alerjisi varsa tigesiklin + kinolon (siprofloksasin veya levofloksasin) önerilir. Piperasilin-tazobaktam veya karbapenemin sürekli ya da uzamış infüzyonunun şiddetli psödomonas infeksiyonunda standart uygulamaya karşı mortaliteyi azaltmada veya hastanede yatış süresini azaltmada etkili olduğu gözlenmiştir. Karbapenem, piperasilin-tazobaktam veya dördüncü kuşak sefalosporin gibi β-laktamlarla yüksek doz monoterapi β-laktam + aminoglikozid kombinasyonundan daha güvenli ve kombinasyona benzer etkilidir. Penisilin alerjisinde kinolon tedavisi randomize kontrollü çalışmalarla önerilmiştir (45). MRSA infeksiyonu için yüksek risk söz konusuysa, daptomisin, linezolid, teikoplanin veya böbrek işlevleri normalse vankomisin kullanılabilir (92). Bununla birlikte sonuçlar antibiyotik duyarlılık testleri ve yerel epidemiyolojik veriler rehberliğinde değerlendirilmelidir. Genişlemiş spektrumlu β-laktamaz oluşturan enterik bakterilere karşı bir karbapenem seçilebilir ve GSBL oluşturan bakteri riski yüksek olduğunda parenteral günde bir kez kullanım kolaylığı, yumuşak dokuya penetrasyonunun iyi olması ve olumlu klinik deneyim nedeniyle ilk seçenek olarak ertapenem tercih edilir (89).
Son yıllarda ülkemizde bazı merkezlerde DAİ’de Acinetobacter baumanii infeksiyonlarının arttığı dikkati çekmektedir (18,21). Bu infeksiyonlarda etkili antibiyotikler ertapenem hariç diğer karbapenemler, sulbaktam, aminoglikozidler, rifampisin ve tigesiklindir. Aminoglikozidler, sulbaktam ve rifampisin meropenemle kombinasyonda tercih edilebilir. Klinik deneyim sınırlı olmakla birlikte, tigesiklin karbapeneme dirençli suşlara karşı etkilidir. Tigesiklin kullanımında hasta özelliklerine dikkat edilmelidir.
Soru 7: Çoğul İlaç Dirençli Bakteri İnfeksiyonları Nasıl Tedavi Edilmelidir?
Son yıllarda yapılan çalışmalarda, diyabetik ayak infeksiyonları kapsamında ÇİD olan etkenlerde artış görüldüğü bildirilmiştir. Sıklıkla şiddetli infeksiyonu, polimikrobiyal üremesi ve hastaneye yatış öyküsü olan hastalardan çoğul ilaç dirençli bakteriler izole edilmektedir (18,22,94). Bu bakteriler, aynı ayaktaki yara için daha önce hastaneye yatış öyküsü olan hastaların 1/3’ünde, osteomyeliti olan hastaların ise 1/4’ünden izole edilir. Önceden kolonizasyonu olan hastalarda yaraya yeterince nüfuz edemeyen antibiyotiklerin kullanılması da bu bakterilerle infeksiyon gelişmesine neden olabilmektedir (18, 71). Uzun süren tedavi edilemeyen yaralarda, rifampisinle birlikte ya da tek başına intravenöz (İV) kolistin, önceki ilaçlara dirençli suşlara karşı bir seçenek olabilir. Antibiyotik tedavisine ilişkin yukarıdaki yanıtlarda bildirilen antibiyotik seçimlerinde özellikle randomize kontrollü çalışmaların sonuçları göz önünde bulundurulmalıdır (40).
Soru 8: Antibiyotik Kullanım Yolu ve Dozu Ne Olmalıdır?
Klinik olarak infekte olmayan ayak ülserlerinde infeksiyon riskini azaltmak veya ülserin iyileşmesini hızlandırmak amacıyla sistemik veya lokal antibiyotik önerilmez. Topikal antibiyotiklerin hafif DAİ’de kullanılması önerilmemektedir. Hafif DAİ’de oral yolla antibiyotik başlanması tercih edilir. Şiddetli ve çoğu orta derece DAİ’de (kritik organ iskemisi hariç), başlangıçta İV tedavi tercih edilmelidir. İzlem sırasında, sistemik infeksiyon bulguları gerilediğinde ve kültür sonuçları oral seçeneklere uygunsa oral tedaviye geçilebilir (38,68).
Şiddetli veya sistemik infeksiyonu olan tüm hastalara ampirik İV antibiyotik başlanması gereklidir (38). Doz ve dozlama aralığı için, infeksiyonun şiddeti ve infeksiyon bölgesinde yeterli ilaç seviyelerini sağlamak için vasküler yetmezliğin derecesi ve böbrek yetmezliği (kreatinin klirensine göre) dikkate alınmalıdır.
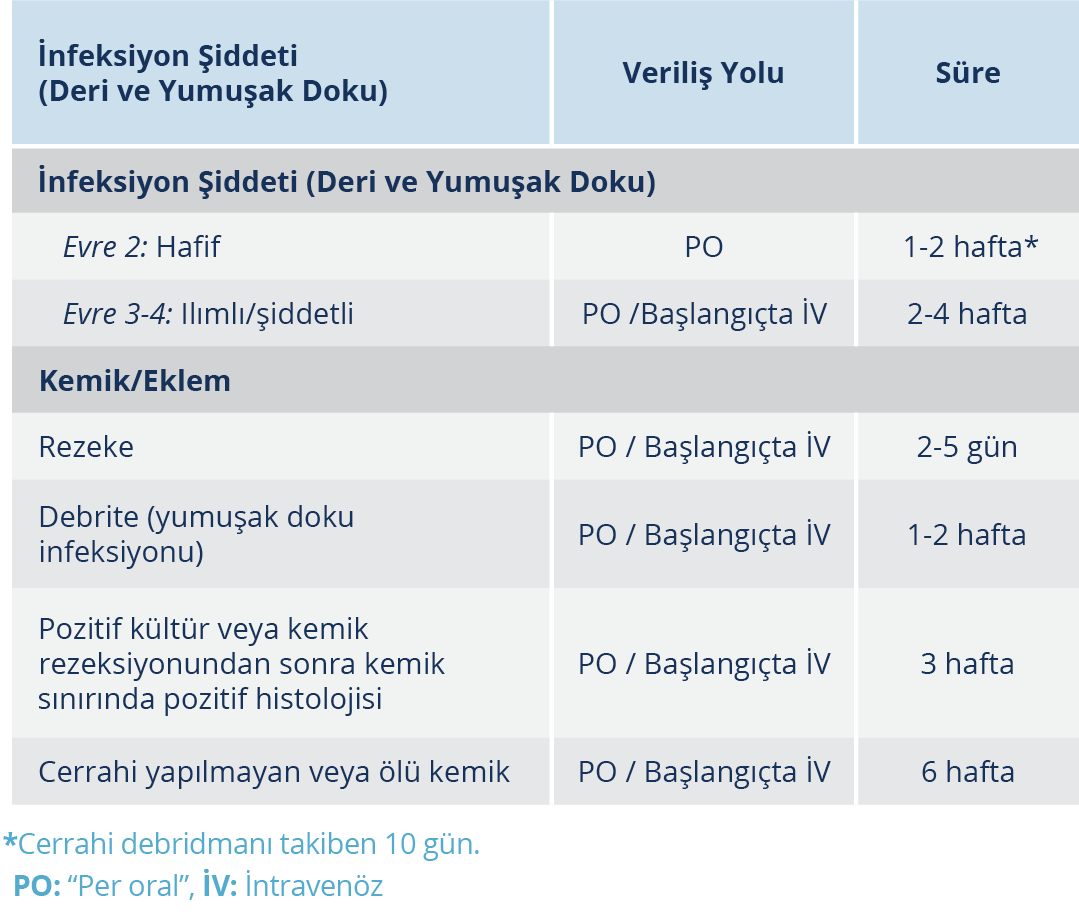
Diyabetik ayak osteomyelit olguları başlangıçta parenteral tedavi gerektirir. Tedavinin 14. gününde kanıtlanmış patojen duyarlı ve hastanın oral alınımını engelleyen bir durum yoksa yüksek biyoyararlanıma sahip olan etkili oral antibiyotik rejimine geçilebilir (95,96). Antibiyotiklerin kullanım yolu ve dozları Tablo 5’te gösterilmiştir.
Soru 9: Diyabetik Ayak Yumuşak Doku İnfeksiyonunda Antibiyotik Tedavi Süresi Ne Olmalıdır?
Antibiyotik tedavisinin süresi, infeksiyonun klinik şiddetine, vasküler durum ve tedaviye verilen yanıta bağlıdır. Tedavi yara iyileşene kadar değil, infeksiyon bulgularının ortadan kalkmasına kadar sürdürülür. Diyabetik ayak deri-yumuşak doku infeksiyonu olan olgularda antibiyotik tedavi süresi 1-2 hafta kadardır (38,40,45,97). Antibiyotik tedavisinin optimal süresini bildirecek yüksek düzeyde kanıt olmamasına rağmen, hafif infeksiyonu olan hastalarda yara bakımı ile birlikte 7 günlük antibiyotik tedavisi genellikle yeterlidir (98). Orta-şiddetli infeksiyonda 2-3 hafta tedavi önerilir. Eğer infeksiyon beklenenden daha yavaş iyileşiyor veya hastada şiddetli PAH varsa, tedavi 3-4 haftaya kadar uzatılabilir. Dört hafta süren uygun tedaviye rağmen iyileşme görülmüyorsa hasta yeniden değerlendirilmeli, alternatif tedaviler ve diğer tanısal test ihtiyacı gözden geçirilmelidir.
Soru 10: Osteomyelitte Tedavi Süresi Ne Olmalıdır?
Medikal tedavinin yeterli olup olmayacağı, cerrahi tedavi gerekliliği tedaviyi yürüten ekip tarafından hastanın tüm koşulları dikkate alınarak tartışılmalıdır. Osteomyelitte antibiyotik tedavisi süresi, cerrahi uygulamanın olup/olmamasına ve ameliyattan sonra kalan etkilenen dokunun boyutuna bağlıdır. Akut osteomyelitte tedavi süresi, en az iki haftası parenteral olarak uygulanmak üzere 4-6 haftadır (38,45). İnfeksiyon ilk 2 ila 4 hafta içerisinde klinik olarak düzelmezse, kültür için kemik örneği almak, cerrahi girişimde bulunmak, rezeksiyon veya alternatif bir antibiyotik rejimi seçilmesi düşünülmelidir.
Yakın zamanlarda diyabetik ayak osteomyeliti olan hastalarda yapılan prospektif randomize bir çalışmada, üç haftalık antibiyotik tedavisi ile altı haftalık antibiyotik tedavisi karşılaştırıldığında benzer sonuçlar elde edildiği bildirilmiştir (99). Cerrahi sonrası infekte kemik çıkarılmış ve geride infekte doku kalmadığı düşünülüyorsa tedavi süresi parenteral 5 güne kadar sınırlanabilir. Yapılan son çalışmalardan birinde, diyabetik ayak osteomyelitinde altı haftadan fazla antibiyotik tedavisi uygulanmaması önerilmiştir (95). Uluslararası diyabetik ayak çalışma grubu, infekte olmuş kemiğin tamamı cerrahi olarak çıkarılmışsa 2-5 gün, yumuşak doku infeksiyonu devam ediyorsa 1-2 hafta daha antibiyotik tedavisi verilmesini önermektedir. Pozitif kültür veya kemik rezeksiyonundan sonra kemik sınırında pozitif histoloji varlığında başlangıçta İV ve ardından “per oral” (PO) olarak üç hafta, cerrahi yapılmayan veya nekrotik kemik varlığında ise başlangıçta İV ve ardında PO olarak altı hafta tedavi önermektedir (Tablo 5) (40). Başka bir çalışmada, rezidüel nekrotik kemik kalırsa, klinik iyileşme için başlangıçta İV ve ardından PO olarak 1-3 hafta daha antibiyotik tedavisi gerektiği vurgulanmıştır (100).
Soru 11: Diyabetik Ayak ve Osteomyeliti Olan Bir Kişide, Remisyona Ulaşmada Tek Başına Antibiyotik Tedavisi, Cerrahi + Antibiyotik Kombine Tedavi Kadar Güvenli ve Etkili midir?
Periferik arter hastalığı, açıkta kemik veya apseleri olmayan hastalar için kombine tedavi ile benzer sonuçlar alınmıştır (101). Tek başına antibiyotik tedavisi, konservatif cerrahi tedavi ile karşılaştırıldığında; iskemi veya nekrotizan yumuşak doku infeksiyonları olmaksızın osteomyelit ile komplike olan nöropatik ön ayak ülseri olan hastalarda iyileşme oranları, iyileşme süresi ve kısa vadeli komplikasyonlar açısından benzer sonuçlara sahiptir (101). Komplike olmayan ön ayak osteomyeliti olan hastalarda diğer yönden cerrahi bir müdahale gerekmiyorsa cerrahi tedavi olmaksızın sadece antibiyotik tedavisi ile izlenebilir. Diyabetik ayak yumuşak doku infeksiyonuna eşlik eden olası osteomyeliti olan bir hastanın acilen cerrahi açıdan değerlendirilmesi, ameliyat sonrasında da medikal bakım ve cerrahi yaklaşım için takip edilmesi önerilir (102).
Soru 12: Antibiyotik Tedavisine Yanıt Alınmadığında Ne Düşünülmelidir?
Ampirik antibiyotik tedavisine yanıt alınamaması, yetersiz odak kontrolü, antibiyotik direnci, iskemi nedeniyle infeksiyon bölgesinde azalmış antibiyotik konsantrasyonu, biyofilm oluşumu veya yetersiz antimikrobiyal kapsamı nedeniyle olabilir (17-19).
Soru 13: Diyabetik Ayak İnfeksiyonu Tedavisinde Yeni Neler Var?
Diyabetik ayak yarasında infeksiyonun tedavisi ve doku onarımının sağlanması anlamında pek çok yeni tedavi-müdahale seçeneği gündemdedir. Bunlardan üzerinde çalışma yapılanlar aşağıda sıralanmıştır.
Cerrahi Müdahaleyi İzleyen Kısaltılmış Tedavi Süreleri
Osteomyelitli DAİ’de, cerrahi debridman sonrası üç haftalık ve altı haftalık antibiyotik tedavi sürelerini karşılaştıran bir çalışmada iki aylık izlemde remisyon oranları benzer (istatistiksel olarak “non-inferior”) bulunmuştur (99). Osteomyelitsiz diyabetik ayak olgularında, cerrahi debridman sonrası 10 gün ve 20 gün süre ile antibiyotik uygulamalarında benzer remisyon oranları bildirilmiştir (103).
Antibiyotik Yüklü Tanecikler / Aracı Materyaller ile Topikal Tedavi
İki ayrı in vitro çalışmada, antibiyotik yüklenmiş tanecikler yoluyla yapılan topikal antibiyotik uygulamalarının, biyofilmlerde mikroorganizma yükünü 5-9 log azalttığı gösterilmiştir (104,105). Başka bir çalışmada antibiyotik yüklü kollajen sünger + sistemik antibiyotik uygulamasının yalnızca sistemik antibiyotik uygulamasına göre daha etkin olduğu saptanmıştır (106).
Fotodinamik Tedavi
Fotodinamik tedavi, vücuda verilen ışığa duyarlı maddenin ışık uygulaması etkisi ile aktive olarak hedef hücrede değişiklik oluşturması olarak tanımlanabilir. Bu tedavi yöntemi ile yaradaki bakteri yükünün azaldığı, Pseudomonas ve MRSA’nın antibiyotik tedavisine duyarlılığının arttığı gösterilmiştir. Ayrıca yara iyileşmesine olumlu etkileri olduğu ve ülser iyileşmesine bu yolla da katkı sağladığı bildirilmiştir (107-111).
Trombositten Zengin Plazma (PRP) Uygulaması
Trombositten zengin plazma (PRP) uygulamasının yara iyileşmesini hızlandırdığı, yaranın infekte olma riskini azalttığı gösterilmiştir (112-114). Ancak PRP uygulamasının tam temas alçılı hastalarda yara iyileşmesine anlamlı katkı sağlamadığı randomize kontrollü bir çalışmada gösterilmiştir (115). Ayrıca Türkiye’de yapılmış bir çalışmada, PRP’nin ÇİD olan bakterilerin üremesini anlamlı derecede inhibe ettiği bildirilmiştir (116).
Biyomühendislik Ürünleri, Nanoteknoloji
Antimikrobiyal peptidler, biyoaktif peptidler olarak da bilinmektedir. Memeli derilerinde bulunan geniş spektrumlu antibakteriyel etkinlikleri olan peptidler (defensinler, katelisidinler, dermisidinler, vb.) yanında nisin, peksiganan gibi moleküller de biyojel haline getirilip yaraya uygulanabilmektedir. Benzer şekilde polimer bazlı nanokompozit hidrojellerle DAİ tedavisi yapılabilmektedir (117-125). Yine ‘biyoyardımcı’ olarak nitelendirilen bazı moleküllerin (immünokin, pirfenidon vs.) yara iyileşmesini sağladığı gösterilmiştir (126-128).
Ultrasonik ve Diğer Debridmanlar
Karbondioksit lazer debridman; nekrotik dokuları içindeki patojenle birlikte buharlaştıran bir yöntemdir (129).
Elektroporasyon ile debridman; hızlı ve ağrısız olarak bakteriyel yükü azaltıp biyofilmi temizlemekte olup odakların ortadan kaldırılmasında bir süredir kullanılmaktadır. Yara için henüz çok yeni bir seçenek olduğu için geliştirilmesi gereklidir (130).
Ultrasonik debridman; özellikle cerrahi debridman yapılamayan hastalarda, bakteriyel yükü azalttığı ve hücre proliferasyonunu artırdığı kanıtlanmıştır. Antikoagülan kullanımı nedeniyle cerrahi debridman yapılamayan, hastaneye gidemeyen hasta için kullanışlı bir seçenek olarak sunulmaktadır. Ancak ağrı dezavantajı vardır ve medikasyon gerektirmektedir (131).
Enzimatik debridman; papain üre ya da kollajenaz kullanılarak yapılan debridman yöntemidir. Cerrahi debridmanın ardından seri uygulamalar şeklinde kullanılması önerilmektedir (132).
Hidrocerrahi ile debridman; iki prospektif randomize kontrollü çalışma, iki retrospektif karşılaştırmalı çalışma, üç prospektif karşılaştırmasız çalışmanın incelendiği metaaanalizde kısa süreli, maliyet etkin ve yara yatağını koruyucu olarak değerlendirilmiştir (133,134).
Faj Tedavisi
Bakteriye özel olmaları, hedefe yönelik kulllanılabilmeleri, mikrobiyotanın korunabilmesi gibi avantajları yanında biyofilme de etkili olduklarını gösteren sınırlı sayıda çalışma mevcuttur. Çoğul ilaç direnci olan bakteri infeksiyonlarında etkinlikleri gösteren bu çalışmalar faj tedavisinin, antibiyotik tedavisine alternatif olma potansiyeli açısından ilgi çekicidir (135,136). Bu konudaki sistemik derlemelerde bakteriyofaj tedavisinin topikal ya da sistemik uygulamasının diyabetik ayak da dahil yüzeyel ya da lokalize infeksiyonlarda güvenli ve yüksek etkin olduğu bildirilmiştir (137,138).
Amniyon/Koryon Uygulamaları
Bu materyallerin yara kapanmasını kısa sürede sağladığı, standart tedaviden daha iyi olduğu gösterilmiştir (139,140). Bir çalışmada PRP’den daha etkin bulunmuştur (141). Standart bakıma eklenmesinin ileri derece maliyet etkin olduğu gösterilmiştir (142-145).
Bitkisel Tıp ve Diğer Biyomateryaller
Çeşitli bitkisel maddeleri ve doğal biyolojik maddeleri içeren (büyüme faktörleri, kitosan, kollajen, hyalüronik asit, aminoasit kombinasyonları, vb.) pek çok topikal jel formunda materyal geliştirilmiştir (146-149).
Kök Hücre Tedavileri
Hem kemik iliği kökenli mononükleer hücreler hem de endotelyal progenitör hücrelerin iskemik dokuda rejeneratif potansiyeli mevcuttur. Mikrodolaşım, granülosit koloni stimüle edici faktör (GCSF) uyarılması, glukoz metabolizmasına olumlu etkileri daha önce gösterilmiştir. Adipöz dokudan elde edilen mezenkimal kök hücrelerin çeşitli doku faktörleri ve kollajen yapımını uyardığı bilinmektedir. Ayrıca bu tür hücrelerin DAİ’de zor iyileşen ülser varlığında anjiyogenezi uyarabildiği de gösterilmiştir (150). Kritik bacak iskemisi olan diyabetik ayak hastalarında 6-12 aylık ampütasyonsuz izlemde; perkütan translüminal anjiyoplasti (PTA) ve kök hücre uygulaması benzer şekilde faydalı bulunmuştur (151). Klinik uygulamaya girmiş olsalar da doz bağımlı olarak anjiyogenezi uyarmaları, nöroiskemiyi ve inflamasyonu düzeltmeleri ve kollajen depolanmasını artırmaları yanında tümör büyümesini de sağlayabilmeleri nedeniyle uygun doz ve uygun kullanım konusu ve güvenlilikleri üzerine çalışmalara ihtiyaç duyulmaktadır (152-153).
Hasta Takibinde Dijital Teknolojilerin Kullanımı ve Teletıp Uygulamaları
Pandemi öncesinde de diyabetik ayak ülserlerinin izleminde teletıp ve dijital teknoloji kullanımının standart hasta izlemi ile benzer sonuçları verebildiği, ampütasyonu önlemede faydalı olduğu gösterilmiştir (154-156). Dijital teknolojilerin yüksek riskli ayağın triyajını sağlama, evde hastayı izleyebilme ve özbakıma destek verme anlamında belirgin fayda sağladığı pandemi döneminde tecrübe edilmiştir (157,158). Türkiye’de de teletıp hizmetleri kullanımına yönelik mevzuat oluşturulmuş durumdadır (159-161).
CERRAHİ TEDAVİ
Cerrahi tedavinin amacı her şeyden önce yarayı kapatmak, yaranın tekrarlamasını engelleyici tedbirleri almak ve mümkünse hastayı ampütasyondan korumaktır.
Soru 1: Diyabetik Ayak Yarasında Cerrahi Yaklaşımın Hedefleri Nelerdir?
Diyabetik ayak yaralarında cerrahi yaklaşımı beş bölümde incelemek gerekir;
- Acil yara müdahalesi; akut septik yaklaşım, apse drenajı ve/veya debridman (infeksiyonlu DA yarasını infeksiyonsuz ayak yarasına çevirmek),
- Vasküler patolojiler için yapılan cerrahi girişimler,
- Yara kapatıcı müdahaleler, rekonstrüksiyon yöntemleri, greft ve flep cerrahisi,
- Ülseri önleme ve tedavi amaçlı kemik ve ayak patolojilerinin rekonstrüksiyonu (Charcot ayak deformitesi, aşil uzatılması, tenotomi ve gerektiğinde osteotomiler, vb.)
- Gereğinde uygulanan minör ve majör ampütasyonlar.
Bu beş yaklaşımı kapsayıcı bir şekilde düşünmek gerekmektedir; bir hasta için sadece birini veya aynı anda birden fazlasını uygulamak gerekebilir.
DEBRİDMAN
Soru 1: Diyabetik Ayakta Neden Debridman Yapılmalıdır?
Diyabetik ayak debridmanı, temelde kronik yaranın akut yara haline getirilmesi prensibine dayanır. Bu yolla birçok fayda sağlanır. Bunların başında yara iyileşme fazları için dokunun uyarılması ve yabancı madde, debris ve biyofilmin uzaklaştırılması gelir (162). Debridman hem hastadan uygun doku kültürü alınmasını sağlar, hem de debride edilmeden önce yara derinliği ve karakteristiği gibi bulgularda yanılsamaya neden olacak dokular uzaklaştırılarak yaranın daha detaylı ve doğru değerlendirilmesini sağlar. Debridman aynı zamanda yara infeksiyonunun kontrolüne yardımcı olur. Seri debridmanın yara iyileşmesini hızlandırdığı da birçok çalışmada gösterilmiştir (162-164). Diyabetik ayak problemi olan hastalarda yara debridmanının erken yapılması önemlidir (165).
Debridman Yöntemleri
Her pansuman değişimi, yara bölgesinden ölü ve devitalize dokuları uzaklaştırmasıyla bir ölçüde debridman işlemidir. Genel olarak debridman yöntemleri beş başlık altında toplanabilir;
Cerrahi/keskin debridman, cerrahi alet, sıklıkla bistüri kullanılarak yapılır. Kanama kontrolü açısından dikkatli olmak gereklidir.
Mekanik debridman, fiziksel enerji kullanılarak uygulanan debridmandır. Lazer, USG ve irrigasyon (“water jet”) yöntemleri kullanılarak uygulanır (166).
Otolitik debridman, vücudun kendi enzimlerinin otoliz yöntemiyle debridman yapmasıdır. Yara üzeri uygun örtülerle örtülerek (hidrojel, hidrokolloid, köpük, alginat, vb.) uygun ortam sağlanır (167).
Biyolojik debridman, larva (Lucilia sericata) tedavisiyle uygulanan debridmandır.
Enzimatik debridman, proteolitik enzimlerin kullanıldığı topikal bir tedavidir (168,169).
Soru 2: Acil Cerrahi Girişim Gerektiren Durumlar Nelerdir?
Kritik DA olgularında gerek iskemi gerekse infeksiyon hastanın hayati tehlikesine ve uzuv kaybına yol açabileceğinden birçok disiplinin beraber çalışması acil tanı ve tedavi için gereklidir (14). İskemi ve infeksiyonun bir arada olması ampütasyon ihtimalini oldukça artırmaktadır (170,171).
Kritik diyabetik ayak olarak tanımlanabilecek olan apse, nekrotizan fasiit ve kapalı bir kompartmanda basınç artışı nedeniyle nekrotik dokuların yara iyileşmesine engel olduğu durumlar acil cerrahi müdahale gerektirmektedir. Kritik diyabetik ayak varlığı diyabetik hastalarda acil durum olarak değerlendirildiklerinden bu hastaların debridmanı, antibiyotik tedavisi, revaskülarizasyonu ve genel durum düzeltilmesi hızlıca yapılmalıdır (170). Yaradaki infeksiyonun sistemik toksisiteye, metabolik instabiliteye yol açabilmesi durumunda da hastaya acil cerrahi müdahale gereklidir (172). Apse drenajı sadece ayağı rahatlatmakla kalmaz hastanın genel durum bozukluğunu, presepsis/sepsis tablosunu da sıklıkla iyileştirir. Bunun yanında akut iskemik hadiseler de diyabetik ayak yaralarında acil girişim ihtiyacı doğurur. Eğer hastada gelişmiş olan infeksiyon tendon ve fasyal planlar arasında yayılmış ise acil cerrahi bir müdahale gereklidir (173).
Soru 3: İnfeksiyonlu ve İskemik Ayaklarda Revaskülarizasyon mu, Yoksa Debridman mı Önce Yapılmalıdır?
Diyabetik ayak ülserlerinde infeksiyon oranı yüksektir ve ampütasyonun en önemli sebebi olduğu bildirilmiştir (40,174). İnfeksiyonlu diyabetik yarası olan hastalarda revaskülarizasyon veya debridman kararı hastanın başvuru zamanındaki yara ve genel sağlık durumuna göre belirlenir. Kuru nekrozu ve yüzeysel bir selüliti olan hastada uygun antibiyoterapi sonrası revaskülarizasyon ve bunun sonrasında debridman planlanması yapılabilir.
Yine akut gelişen bir iskemide debridman için vakit kaybetmemek gerekir. İnfeksiyon tedavisinde antibiyotik uygulaması ile birlikte debridman yapılması, bakteri yükünü önemli ölçüde azaltarak tedavinin etkili olmasına yardımcı olmaktadır. Islak gangren ve infeksiyon varlığında da nekrotik dokuların uzaklaştırılması acil cerrahi girişim gerektirir; vakit kaybedilmeden hastanın debridman ve cerrahi uygulamaya alınması gereklidir (175).
Sonuç olarak; revaskülarizasyonun yara iyileşmesi için önemini vurgularken akut iskemik ve septik hadiseler dışında kollateral gelişiminin debridman ve infeksiyon tedavisine bir süre zaman kazandırabileceği de göz önünde bulundurulmalıdır.
Soru 4: Acil veya Elektif Cerrahi Girişimde Debridman Sınırları Nasıl Belirlenmelidir?
Acil cerrahi girişimlerde yapılan debridmanlarda sağlam/ölü doku ayırımı yapmak, dokunun ödemi ve infeksiyonun neden olduğu değişiklikler nedeniyle elektif debridmana göre daha zordur. Elektif debridman, basit bir pansuman değişimi sırasında bile yapılabilen bir işlem olup ölü dokuların, hipertrofik kallus dokusunun ve yabancı cisimlerin yaradan uzaklaştırılmasını sağlar. Elektif debridmanın amacı; yarayı kronik yaradan akut haline getirerek yara iyileşme aşamalarının bir noktada durmamasını sağlamaktır. Diyabetik ayak ülseri olan hastalarda, vasküler patolojiler sıklıkla eşlik ettiğinden her zaman debridmanla kanamalı dokuya ulaşmak mümkün olmayabilir (174). Bu gibi durumlarda sağlıklı parlak dokuya ulaşmak yeterlidir. Debridman, fasyal planların birbirinden kolay ayrılmadığı ve dokuların bütünlüğünü koruduğu alanlarda durdurulabilir. Turnike kullanımı sağlıklı ve kanamalı dokuyu maskeleyebileceğinden çoğu zaman önerilmez (173). Elbette kanama kontrolü yapılmalı ve gereksiz kanama ile genel durum bozulmasından kaçınılmalıdır.
Lokal veya genel anestezi altında yapılan işlemlerde mutlaka ameliyathane koşullarının sağlanması ve periferik veya lokal olarak verilen anestezi ve analjeziklerin yan etkilerine karşı dikkatli olunması gereklidir. Çoğunlukla nöropatik olan bu hastalarda ağrı duyusunun olmaması debridman koşullarını değiştirmemelidir; vital yapıların ortaya çıkması, kanama gelişmesi gibi ani durumlar karşısında hastaya müdahale edilebilecek cerrahi koşullar mutlaka sağlanmalıdır.
Debridman süreci hem yaranın süregelen durumu hem de hekimin deneyimi ile yakından ilgilidir. Debridman esnasında anatomik yapıların çıkarılmasında tereddüt yaşanması sık görülen bir durumdur. Burada kanamanın gözlenmesi, kokunun ve akıntının azalması, kompartmanlar arasında ölü dokuların ortadan kalkması debridman sınırlarını etkilemektedir. Yara kanasın diye hastayı kan kaybına sokmamak, sağlıklı-ölü doku ayırımı yapmak oldukça önemlidir. Debridman sınırlarını belirlerken seri debridman ihtiyacı olabileceği ve gerektiğinde tekrarlanması gerekliliği de göz önünde bulundurulmalıdır.
Soru 5: Kompartman Sendromu Nedir?
Her bir vücut bölgesi, kasları, sinirleri ve damarları içeren bir kompartmana sahiptir. Ayak içinde de kaynaktan kaynağa farklılık olmakla birlikte 4-7 arasında kompartman bulunmaktadır. Plantar bölgedekilerin dördü; mediyal, santral, lateral plantar kompartmanlar ve derin interossöz kompartmandır. Bu kompartmanlardaki basınç artışı, içerideki yapılar üzerinde baskı yaparak dolaşımı engelleyebilir ve bu durum acil tıbbi müdahale gerektirebilir. Ayrıca, infeksiyonun zamanında tedavi edilmediği durumlarda da o kompartman boyunca ayağın fleksör kaslarına yayılarak, kompartmanın şişmesine ve bir kompartman sendromu gelişmesine neden olur. Bu durum, kan dolaşımını engelleyebilir ve sinir basısına neden olabilir. Şiddetli ağrı ve hassasiyet, belirgin şişlik, renk değişikliği, soğukluk ve uyuşma hissi kompartman sendromunun belirtilerindendir. İnfekte bir kompartmanın sağlıklı dokulara erişinceye kadar cerrahi olarak genişçe açılarak, acilen drenajının ve debridmanının yapılması gerekir.
Soru 6: Debridman Sonrasında Yara İzlemi Nasıl Yapılmalıdır?
Debridman sonrası yaranın ilk görülme zamanını, temel olarak hastaya ait özellikler ve yaradaki infeksiyon bulguları belirler. İnfekte olmayan bir yaranın debridman sonrası 48. saatte görülmesi yeterliyken, infeksiyon varlığında bu süre daha erkene çekilmelidir (172). Yara görünümünde sağlıksız ve ölü dokuların kalıp kalmadığı, yara çevresinde veya içinde infeksiyon bulgularının olup olmadığı ve yara tabanında sağlıklı granülasyon dokusunun var olup olmadığı değerlendirilmelidir. Debridman yeterli ise hastanın yara bakımı ve yara rekonstrüksiyonu temel prensipler çerçevesinde gerçekleştirilir.
Soru 7: Hangi Hastalarda Primer Ampütasyon Uygulanmalıdır?
Akut bir DAİ’de öncelikli amaç hastanın yaşamını kurtarmaktır. Özellikle bir ayağın ampüte edildiği durumlarda, ikinci ayağın korunması açısından ekstra bir çaba sarfedilebilir. Ancak özellikle hastanın revaskülarizasyon için uygun bir aday olarak kabul edilmediği durumlarda primer ampütasyon ile hastanın ağrısının kontrolü ve ortez/protez desteği ile hızlı ve etkili mobilizasyonu sağlanabilir (176).
Debridmanla infekte dokunun tamamen temizlenmesinin mümkün olmadığı, hastanın kalan infeksiyon yüküyle başa çıkamayacağı durumlarda, ıslak gangren olgularında (infeksiyon + iskemi), yaygın kas nekrozu olması durumunda, bu koşulları sağlayan yatalak veya fonksiyonel olarak işlevsiz bir ekstremitesi olan hastalarda, uygulanacak ortopedi ve plastik cerrahi girişimlerinin uygulanması için gerekli revaskülarizasyonun sağlanamayacağına inanılan hastalarda, rekonstrüksiyonu neredeyse olanaksız olgularda veya diyaliz hastalarında ampütasyon daha doğru bir seçim olabilir (38,176,177).
Primer ampütasyon uygulanması veya daha konservatif bir tedavi arasında verilecek karar ise hasta ile iletişim halinde iken, içinde damar cerrahı veya damara yönelik girişimler açısından tecrübeli bir uzmanın da dahil olduğu interdisipliner bir ekip tarafından verilmelidir (177)
REVASKÜLARİZASYON
Soru 1: Diyabetik Ayak İnfeksiyonu ve Periferik Arter Hastalığı Olan Olgularda Vasküler Yapının Özellikleri Nasıldır?
Diyabetik ayak hastalığında; ateroskleroz, diyabetik makroanjiyopati ve diyabetik mikroanjiyopati olmak üzere arteriyel patolojinin üç bileşeni vardır. Diyabet hastalarında aterosklerozun gelişimi, diyabetik olmayanlar ile fizyopatolojik açıdan benzerdir.
Klasik ateroskleroz diyabet hastalarının iliyak, femoral ve popliteal arterlerinde diyabeti olmayan hastalar ile aynı oranda saptanmaktadır. Aterosklerotik hastalık, diyabetlilerde 10 yıl daha erken başlamakta olup distal arterleri daha sık tutmakta, uzun tıkanıklıklarla seyretmekte ve daha hızlı ilerlemektedir; bu nedenle kollateral gelişimi daha zayıftır. Arteriyel yapı tespih tanesi görünümüne benzer çoklu tıkanıklık ve darlıklar ile seyretmektedir (178). Diz altı damarlarını da yaygın tuttuğu ve bu bölgede kollateraller genişlediği için hasta nadir olarak kesik topallamadan (aralıklı klodikasyo) şikâyet eder. Klodikasyo hissedilmemesinin temel olarak iki sebebi vardır. Bunlardan ilki, alt seviyelerdeki bir tıkanıklığın üst seviyedeki bir tıkanıklığa nazaran baldır dolaşımında daha az sıkıntı yaratması; diğeriyse bu hastaların nöropati sebebiyle ağrı duyularındaki azalmadır. Semptomlar genellikle ayak bileği basıncı 80 mmHg’nın altına indiğinde ortaya çıkar.
Diyabetik makroanjiyopatinin temeli klasik olarak medial kalsifikasyondur. Kalsifikasyon sıklığı ve miktarı diyabet süresi ile doğru orantılı olup vibrasyon duyusu kaybı ile seyreden nöropati ile yakından ilişkilidir (179). Medial kalsifikasyonun artmış mortalite ve artmış ampütasyon riski ile ilişkisi gösterilmiştir (180). Medial arteriyel kalsifikasyon, yanlış basınç ölçümlerine yol açabildiği gibi distal arteriyel akım karakterini değiştirip ayağa olan maksimum akımın kısıtlanmasına yol açar (181). Sistol anında arteriyel duvarın genişlemesi kısıtlanmıştır; bu da yüksek basınçlı sistolik akımın azaltılamadan distaldeki ayak mikrodamarlarına iletilmesine yol açar. Arteriyel duvarın genişlemesi ateroskleroz gelişiminde de önemlidir. Arter duvarındaki kurşun boru tarzındaki sertlik yerçekimi ile ilişkili intraluminal basınç artışına yol açarak infrapopliteal dallarda plak gelişimini hızlandırmaktadır. Yapısal duvar bozukluğu dışında artmış arteriyel direnç, artmış akım hızı ve artmış nabız basıncına yol açar. Artmış sistolik basınca bağlı olarak ard yükte artış ve sol ventrikül hipertrofisi gelişir. Diyastol basıncında azalma ve koroner perfüzyon bozukluğu mevcuttur. Diyabet hastalarındaki otonom nöropati vazosempatik refleksi bozarak intraluminal basıncın yüksek kalmasına destek olmaktadır. Normal bir kişide yatar pozisyondan dik pozisyona geçildiğinde cilt damarlarında refleks vazokonstriksiyona bağlı olarak kan akımında %20 azalma meydana gelir. Otonom nöropati nedeniyle bu refleksin kaybı sonucu ayak cilt damarlarına kan akımı yüksek kalmaktadır. Diz altı arterlerindeki sertliğe bağlı akım dalgasındaki düzleşme, eşlik eden vena kominikanteslerde pulsatilitenin kaybına yol açar. Baldır kaslarını besleyen arterlerdeki yetmezliğe bağlı olarak kaslardaki erime ile beraber venlerdeki pulsasyon kaybı alt ekstremitede venöz yetmezliğe bağlı ödeme yol açar (182).
Eritrositler (8 µu) kapillerlere (4-6 µu) nazaran daha büyük çaptadırlar ve kapillerler içinden tek tek geçerler. Kapillerlerden geçişi sağlayabilmeleri için eritrosit membranlarında deformasyon meydana gelir. Diyabette glikozillenmiş eritrosit membranları bu şekil değişikliğini gerçekleştiremez ve lümende tıkanıklığa yol açar. Lökositler damar lümeninde kenarlarda yuvarlanma şeklinde yavaş hareket eden büyük moleküllerdir. Mikrosirkülasyon da gerçek kapiller yerine arteriyovenöz şantları tercih eder. Ayaktaki yüksek basınç nedeniyle hem eritrositler hem de lökositler bu şantlara yönlendirilir. Diyabetik damar tıkanıklığında, kan akımı ve basıncı azaldığı için bu büyük hücreler gerçek kapillerleri tercih eder. Ayakta ısı kaybından sorumlu kutanöz damarlar bu arteriyovenöz şant damarlarıdır. Gerçek kapillerler ise nutrisyonel damarlardır. İnfeksiyon anında dolaşımda ve yara bölgesinde artan lökositler, mikro damarlarda eritrositlerin hareketini engeller. Yavaş hareket eden bu büyük çaplı hücreler gerçek kapillerde obstrüksiyona yol açarlar. Gerçek kapillerlerin tıkanıklığı dokuda gangrene yol açmaktadır. Nabız alınabilen bir ayakta parmak infeksiyonu gangren gelişimi bu olay ile açıklanabilir (183).
Soru 2: Diyabetik Ayak İnfeksiyonu Olan Olgularda Periferik Arter Hastalığı Sıklığı Nedir? Diyabetik Ayak Yarası Olan Hastada Vasküler Cerrah Görüşü Ne Zaman Alınmalıdır?
Dünya nüfusunda, ülkelerin gelir düzeyine göre dağılımlara bakıldığında, orta-yüksek gelirli ülkelerde diyabeti ve ayak ülseri olan hastaların %50’sinde PAH olduğu tahmin edilmektedir (182,184). Düşük-orta gelirli ülkelerdeki diyabet hastalarında PAH için bir oran söylenemese de diyabete bağlı ölümlerin %80’den fazlasının bu ülkelerde görüldüğü bilinmektedir. IWGDF’nin yayınladığı diyabetik ayak yarası tedavi algoritmasında ilk yapılacak uygulamanın ayağı yükten kurtarmak olduğunu, bunu takiben vasküler yapının değerlendirmesi ve gerekli ise revaskülarizasyon uygulanması için vasküler cerrah görüşü alınması önerilmiştir (177).
Soru 3: Diyabetik Ayak Yarası Olan Olgularda Ekstremite İskemisi Nasıl Değerlendirilmelidir?
Diyabetik ayak yarası olan bir hasta potansiyel periferik arter hastası olarak kabul edilmelidir. Hastanın anamnezi ayrıntılı olarak alınmalı ve kardiyovasküler sistem ile ilişkili diğer hastalıklar sorgulanmalıdır (kalp hastalığı, inme, böbrek hastalığı, ani görme kaybı, vb.). Hastada, PAH ile ilişkili kesik topallama, istirahat ağrısı, ayaklarda üşüme gibi semptomlar sorgulanmalıdır. Anamnezin ardından ayrıntılı fizik muayene gelmelidir. Ekstremitede siyanotik renk değişikliği, tüylenmede azalma, derinin incelmesi ve kuruluğu, ayak tırnaklarında kalınlaşma not edilmelidir. Kızarıklık ve ağrıyla birlikte olan ekstremite iskemisi yumuşak doku infeksiyonuyla karıştırılabilir. Parmak ya da ayak ön bölgesinde yeni başlamış bir gangren sıklıkla yumuşak doku infeksiyonuyla birliktedir. Bu durumda eşlik eden iskemi, inflamasyon bulgularını maskeleyebilir. Diyabette otonom nöropati, prekapiller sfinkter işlev bozukluğuna ve arteriyovenöz şantların açılmasına neden olur. Bu nedenle kapiler iskemi olmasına karşın, ekstremite sıcak ve deri kurudur. Venöz göllenme ve ödem vardır. Bu durum klinisyeni yanıltabilir. Nöropatiye bağlı ağrının bulunmaması ciddi alt ekstremite iskemisini ve doku beslenme bozukluğunu maskeleyebilir. Pedal nabızların palpasyonu oda sıcaklığında yapılmalıdır. Ancak nabızların palpe edilmesi iskemiyi dışlamadığı gibi, tam tersine ayak bileği nabızlarının alınamaması da ciddi iskemi anlamına gelmez. Nabızların olmadığı veya az olarak hissedildiği, nabızların palpe edildiği ama kuvvetli PAH şüphesi olan olgularda ayak bileği-kol indeksi (“ankle-brachial index” – AKI) ölçülmelidir. Bu ölçüm yapılırken ayak arterlerindeki akım şekilleri değerlendirilmelidir. Yapılabiliyorsa ayak başparmak-kol indeksi (“toe-brachial index” – ABPKI) de ölçülmelidir. AKI’nın 0.9’un altında olması PAH için kuvvetli bir göstergedir; 0.9’dan büyük değerler ile PAH tanısı dışlanır. AKI’nın 1.3’ten büyük olması mediakalsinozis nedeniyle yalancı negatif değerler olarak kabul edilmektedir (185). ABPKI’nın 0.75’den büyük olması PAH tanısını dışlar (186). Eski yaklaşımda; ayak parmak arterlerinin mediakalsinozisten etkilenmediği düşünülmekte ve bu ölçümün çok daha sağlıklı sonuç verdiğine inanılmaktaydı. Lakin bunu destekleyen yeterli kanıt bulunmamaktadır (187). Birçok yazar ABPKI ve arter akım şekillerinin beraber değerlendirilmesinin doğruya en yakın tanıyı koymada faydalı olduğunu ileri sürmektedir (188,189). 2021 yılında ülkemizin başlıca kalp ve damar cerrahisi derneklerinin ortak olarak yayımladıkları Periferik Arter ve Ven Hastalıkları: Ulusal Tedavi Kılavuzu’nda diyabetik ayak hastalarında iskemi değerlendirmesine yönelik ayak bileği basıncı ve AKI değerlerinin yanında, perfüzyon bilgileri (cilt perfüzyon basıncı veya transkütanöz oksijen basıncı [TcPO2], vb.) aracılığıyla ampütasyon riskinin değerlendirilmesinin düşünülmesi önerilmiştir (190).
Soru 4: Girişimsel Olmayan Periferik Arter Hastalığı Değerlendirme Yöntemleri Nelerdir?
Fizik muayene dışında kalan ve girişimsel olmayan değerlendirme yöntemleri, yatak başı testleri olarak adlandırılan el doppleri ile arteriyel akım formlarının ölçümü, aynı cihaz kullanılmak suretiyle ölçülen ayak bileği sistolik basınç ölçümü, sistolik AKI, parmak sistolik basınç ölçümü, ABPKI, deri perfüzyon basıncı ölçümü, transkutan oksijen basınç ölçümü (TcPO2) ve radyolojik görüntüleme yöntemi olan Doppler USG ölçümüdür. Yatak başı testlerde el doppleri ile yapılan değerlendirmede trifazik akım formunun ölçülmesi, sistolik ayak bileği basıncının ≥50 mmHg, sistolik AKI >0.9, sistolik parmak basınç ölçümünün ≥30 mmHg, ABPKI ≥0.75, doku perfüzyon basıncı değerinin ≥40 mmHg, TcPO2 ≥25mmHg olması perfüzyonun yeterli olduğunun göstergeleri olarak kabul edilir (187). Doku oksijen basınç ölçümleri, iskemi hakkında bilgi sağlamakla birlikte, ödem ve infeksiyondan dolayı güvenilir sonuç vermeyebilir.
Soru 5: Diyabetik Ayak Yarası Olan Olgularda Görüntüleme Yöntemleri Nasıl Seçilmelidir?
Yapılan yatak başı testlerinde el doppleri ile yapılan değerlendirmede akım alınamaması veya monofazik akım formunun ölçülmesi sonucunda AKI değerinin <0.4, ayak bileği basıncının <50 mmHg, ayak başparmak basıncının <30 mmHg ve TcPO2 değerinin <30 mmHg olması halinde ivedi biçimde ileri görüntüleme ve revaskülarizasyon işlemi planlanmalıdır (191). Aciliyet arz etmeyen diyabetik ayak yarası olan hastalarda; uygun infeksiyon, diyabet ve yara tedavilerine ve uygun yükten kurtarmaya rağmen dört haftalık süre içinde yarada kötüye gidiş veya yara alanında <%50 küçülme olması halinde yeniden vasküler değerlendirme yapılmalıdır (176). Daha ileri görüntüleme yöntemleri olarak; Doppler USG, MRA, bilgisayarlı tomografik anjiyografi (BTA), karbondioksit anjiyografi (KA) ve dijital substraksiyon anjiyografi (DSA) bulunmaktadır (189). Tüm bu görüntüleme yöntemlerindeki amaç alt ekstremite arterlerinin anatomik yapısını ortaya koymak, darlık veya tıkanıklık bölgelerini tespit edip revaskülarizasyon yöntemini ve tedavi planını belirlemektir. Doppler USG; uygulama ve erişim kolaylığı olması, hızlı sonuç alınabilmesi, akım formlarının değerlendirilmesi, ucuz olması, girişimsel olmayan bir yöntem olması, kontrast madde kullanımı gerektirmemesi gibi avantajlara sahip bir görüntüleme yöntemidir. Uzun segment ve yoğun kalsifikasyonlar ile bacak ödemi, görüntü kalitesini düşürmekte olup yapan kişinin bilgisi ve tecrübe düzeyi ile doğrudan ilişkili olması yöntemin dezavantajlarındandır. Kontrast madde kullanımı, diyabetik hastalar gibi sistemik arteriyel dolaşım bozukluğu olan, böbrek arterlerinin de sıklıkla hastalıktan etkilendiği, böbrek fonksiyon bozukluğu olan hasta grubunda ve kalp yetmezliği varlığında kontrast nefropatisi gelişimine yol açabilmektedir. Bu nedenle bazı olgularda görüntüleme yönteminin seçiminde ilk belirleyici faktör kontrast madde gereksinimi olmaktadır. Manyetik rezonans anjiyografi ve BTA yöntemlerinin her ikisinde damarsal görüntünün alınabilmesi için periferik damar yolundan, kontrast maddenin uygulanması gerekmektedir. Bilgisayarlı tomografik anjiyografide kontrast madde ilişkili nefropati ve alerjik reaksiyonların yanı sıra, arter duvarındaki yüksek kalsifikasyon yükü, küçük arterlerin değerlendirilmesini zorlaştırmaktadır. Bilgisayarlı tomografik anjiyografi; MRA’ya kıyasla, erişim kolaylığı, işlem süresinin kısalığı ve nispeten daha düşük maliyetinden ötürü batılı ülkelerin aksine ilk başvurulan görüntüleme yöntemidir. Manyetik rezonans anjiyografide kontrast madde olarak gadolinyum kullanılmaktadır. Daha az nefrotoksisiteye sahip bu ajanın kullanımı bir avantaj olmasına rağmen metalik kalp kapağı, kardiyak “pacemaker” ve intravasküler stent gibi metallerin bulunması görüntülemenin yapılmasını engellemekte veya artefakt oluşturup iyi görüntü elde edilememesine yol açmaktadır. Klostrofobik hastalar için göreceli kontrindikasyon mevcuttur. Kreatinin klirensinin <30 ml/dk olduğu ciddi böbrek yetmezliğine sahip hastalarda, gadolinyum nefrojenik sistemik fibrozise yol açabilmektedir. Bu nedenle son dönemde, ultra küçük süperparamanyetik demir oksit gibi, gadolinyum içermeyen yeni ajanlar geliştirilmiştir (192,193).
Nefrotoksik özelliği olmayan bir diğer kontrast madde karbondioksit gazıdır. İntraarteriyel uygulanan karbondioksit gazı ile çekilen anjiyografi (KA) tanısal amaçlı bir invazif görüntüleme yöntemidir. Klinikte kullanılma amacı kompanse böbrek yetmezliği olan hastalarda perkütan balon anjiyografi işlemi öncesi lezyonların yerini belirleme olup işlemde kullanılacak kontrast madde miktarını olabildiğince azaltarak işlem sonrası gelişebilecek nefropatiyi engellemektir.
İyot içerikli kontrast madde kullanılarak çekilen DSA, günümüzde hala altın standart görüntüleme işlemi olarak tanınmaktadır. En kaliteli görüntüyü sağlaması, kan akımı şekillerinin gerçek zamanlı olarak değerlendirilebilmeleri, hızlı sonuç vermesi ve işlem esnasında endovasküler girişim uygulanabilmesi tetkikin avantajları iken, kontrast madde ilişkili yan etkiler ve arteriyel ponksiyonun komplikasyonları da dezavantajları arasındadır.
IWGDF tarafından yayınlanan kılavuzda, diyabetik ülseri olan hastalarda: AKI <0,4, ayak bileği basıncı <50 mmHg, ayak baş parmak basıncı <30 mmHg, TcPO2 <30 mmHg veya USG dopplerde akımların olmadığı veya monofazik olduğu hastalar da acil görüntüleme ve revaskülarizasyon planlanması gereği olduğu belirtilmiştir (177).
Kılavuza göre alt ekstremite için revaskülarizasyon yapılacağı zaman anatomik bilgi; renkli dupleks USG, BTA, MRA, DSA gibi yöntemlerden biriyle alınmalıdır. Görüntüleme yapılırken tüm alt ekstremite arterleri incelenmeli, diz altı ve pedal damarlara özen gösterilmeli, görüntüler anteroposteriyor ve lateral projeksiyonlarda incelenmelidir (177).
Soru 6: Diyabetik Ayak Yarası Tedavisinde İskemiye Yönelik Tıbbi Tedavi İlkeleri Nelerdir?
Perifer arter hastalığı olan bu hastaların tıbbi tedavisi için 2021 tarihinde güncellenen Periferik Arter ve Ven Hastalıkları: Ulusal Tedavi Kılavuzu’nda (190) en iyi tıbbi tedavi üzerinde önemle durulmuştur. En iyi tıbbi tedavi şunları içermelidir:
- Sigara kullanımının bırakılması.
- Beslenme değişiklikleri ve fiziksel aktivite önerileri.
- Hipolipidemik ilaç kullanımı: (a) LDL kolesterol seviyesinin 70 mg/dL altına düşürülmesi veya başlangıç seviyeleri 70-135 mg/dL ise ≥ %50 azalma sağlanması, (b) tercih edilecek ajanın statinler olması, (c) yeni nesil hipolipidemik ajanlar.
- Diyabetik hastalarda kan şekerinin sıkı kontrolü.
- Semptomatik hastalarda antiagregan tedavi.
- Hipertansiyonu olan hastalarda kan basıncının kontrolü.
En iyi tıbbi tedaviye ek olarak; diyabetik ayak ülseri olan hastaların tedavileri yapılırken kronik ekstremite tehdit edici iskemi (KETİ) tedavi ilkeleri uygulanmalıdır. Bu ilkeler, yüksek mortalite riski olan KETİ hastaları için çok önemlidir. Mortalitenin yanı sıra, revaskülarizasyon olasılığı olmayan hastalarda prostasiklin analogu (iloprost) kullanılması güçlü öneriyle yer almakla beraber diğer prostanoidlerin kullanılmaması önerilmiştir. Ayrıca tüm KETİ hastalarında antiagregan tedavi başlanması (ilk tercih edilecek antiagregan olarak klopidogrel), uzun dönem mortalite ve morbiditeyi azaltmak üzere, kanama riski düşük olan KETİ hastalarında aspirin (100 mg) ve düşük doz rivaroksaban (2.5 mg) kullanılması önerilmiştir. Uzun dönem mortalite ve morbiditeyi azaltmak üzere, KETİ hastalarında statin kullanılması önerilir (190).
Soru 7: Periferik Arter Hastalığı Olan Hastaların Yönetimi Nasıl Olmalıdır?
Periferik arter hastalığı olan bir diyabetik ayak yarasında ivedilikle hareket edilmelidir. Yaraların infekte olduğu durumlarda, hastaların uzuv kaybı ve mortalite oranlarının çok yüksek olduğu daima akılda tutulmalıdır (194). Bu hastalarda motto: “Zaman Dokudur!”. Başvuru anında hastanın ayağı ivedi olarak yükten kurtarılmalıdır. Bunun için yaranın üzerine basılmasını engelleyecek bir pansuman, ortez veya total temas alçısı yapılmalı veya özel üretilmiş tabanlık ve “moon walker” ortezler kullanılmalıdır. Yarada infeksiyon yükü çok fazla, ıslak gangren tablosu ağırlıktaysa, vakit kaybetmeden debridman işlemi yapılarak bakteriyel yük azaltılmalıdır. İnfeksiyon yükünü azaltmak için acil cerrahi müdahele hastaları hariç tüm diyabetik ayak yarası ile başvuran hastalarda, Doppler USG ile arterlerde akım paternleri, AKI ve ABPKI ölçümleri yapılmalıdır. Acil müdahele planlanmayan hasta grubunda ise, iskeminin klinik bulgularının olması veya yatakbaşı testlerinde iskemi bulgularının olduğu diyabetik ayak yarası olan hastada elektif revaskülarizasyon işlemi planlanmalıdır.
İskemi değerlendirilmesinde temel kriterler; iskeminin fizik muayene bulgularının yanısıra, yatakbaşı Doppler USG’de infrapopliteal arterlerde akım olmaması veya monofazik akım olması, ayakbileği sistolik basıncının 100 mmHg’nin altında olması veya başparmak basıncının 60 mmHg’nin altında olmasıdır. Bu bulguların bulunduğu hastalarda yapılacak olan revaskülarizasyon işleminin zamanlamasının planlanlanmasında ise IWGDF 2023 Kılavuzu (177) şunları önermektedir:
- Acil cerrahi müdahele planlanmayan ama ayakta infeksiyon bulguları olan, ayağın bir kısmını içeren gangreni olan veya yatakbaşı testlerde ciddi iskemi bulguları olan hastalar (diğer bir deyişle AKI <0.4, ayak bileği basıncı <50 mmHg, ayak baş parmak basıncı <30 mmHg, TcPO2 <30 mmHg veya Doppler USG’de akımların olmadığı veya monofazik olduğu hastalar) acil olarak vasküler cerrah tarafından işlem açısından değerlendirilmelidirler.
- Ayakta apse, derin doku infeksiyonu ve kompartman sendromu olan hastalarda acil drenaj, kompartmanın dekompresyonu ve infeksiyonun kontrolü için yapılacak debridman ve eş zamanlı geniş spektrum antibiyoterapi ile sepsis kontrol altına alındıktan ve hasta klinik olarak stabil hale getirildikten sonra vakit kaybetmeden arteriyel yapı değerlendirilmelidir. Bu değerlendirmede, ileri iskemi bulguları olan hastalara bir-iki gün içinde acil revaskülarizasyon işlemi yapılmalıdır. Kan akımı sağlandığında ve infeksiyon kontrol altına alındığında fonksiyonel bir ayak sağlamak için gerekli nihai cerrahi girişim (yumuşak doku, kemik rekontrüksiyonu, ampütasyon vs) planlanabilinir.
- İlk değerlendirmeler sonrası revaskülarizasyon işlemine gerek görülmeyen hastalarda, uygun infeksiyon tedavisi, diyabet regülasyonu, yara tedavisi ve yükten kurtarmaya rağmen yarada kötüye gidiş görülmesi veya belirgin iyileşme gözlemlenmemesi halinde (4 hafta içinde yara alanında >%50 küçülme) arteriyel dolaşım bir vasküler cerrah tarafından tekrar değerlendirilmelidir (177).
Unutulmamalıdır ki; diyabetik ayak tedavisi multidisipliner bir yaklaşım ve iş birliği gerektirir. Başvuru anında bahsi geçen yükten kurtarma, revaskülarizasyon-cerrahi debridman değerlendirmeleri ile eş zamanlı olarak antibiyoterapinin infeksiyon hastalıkları ve insülin temelli kan şekeri düzenlenmesinin de endokrinoloji/dahiliye uzmanları tarafından yürütülmesi gerekmektedir. Diyabetik ülser tedavisinde PAH yaklaşımı için IWGDF, diyabetik ülser tedavisi yapan bir merkezin PAH teşhis ve tedavisine hızlı erişimi olması gerektiğini ifade etmiştir (177). Periferik Arter ve Ven Hastalıkları: Ulusal Tedavi Kılavuzu, iskeminin değerlendirilmesinde ve revasülarizasyon etkisinin öngörülmesinde yara durumu, iskemi ve infeksiyonun beraber değerlendirildiği WIfI sınıflama sisteminin kullanılmasının önemle üstünde durmuştur (190).
Soru 8: Diyabetik Ayak Yarası Olan Olgularda Revaskülarizasyon Yöntemlerinin Kullanımına Karar Verilmesinde Dikkat Edilecek Hususlar Nelerdir?
Diyabetik ayak yarası olan ve PAH tespit edilmiş bir hastada revaskülarizasyon için açık “bypass” cerrahisi, kapalı endovasküler yöntemler veya hibrid olarak adlandırılan iki yöntem aynı anda kullanılmaktadır. Hangi yöntemin daha üstün olduğuna dair kanıt düzeyi yüksek güncel bir çalışma bulunmamaktadır (186). Bu işlemlerde temel hedef ayağı besleyen infrapopliteal arterlerin hepsine, mümkün değil ise en az birine abdominal aorttan itibaren kesintisiz pulsatil kan akımının sağlanmasıdır. Bunun gerçekleşmediği hallerde en az bir arterde kan akımı sağlanmalı ve mümkünse bu arter yaranın bulunduğu anatomik bölgeyi besleyen arter olmalıdır. İşlem sonrası, objektif yatak başı testleri kullanılarak yapılacak perfüzyon ölçümleri ile işlemin etkinliği test edilmelidir.
Revaskülarizasyon işlemine karar vermeden önce; hastanın yaşı, yaşam beklentisi, mobilize olup olmadığı, debridman veya minör ampütasyonlar sonrasında basma ve yürüme fonksiyonunu gerçekleştirmeye uygun, yeterli doku kalıp kalmayacağı soruları üzerinde ayrıntılı olarak düşünülmelidir. Benzer bir konu ampütasyonun kaçınılmaz olduğu hastalardır. Majör ampütasyon kararı alınan hastalarda ampütasyon seviyesini diz altı seviyesine çekmek için öncelikle bir revaskülarizasyon işlemi planlanabilir. Hastanın revaskülarizasyon işleminden fayda görüp görmeyeceğinin kararını vermek için WIfI sınıflaması kullanılabilir (195). Fonksiyonel kapasitesi kısıtlı, kırılgan yapıda, kısa yaşam beklentisi olan hastalarda cerrahi yönünde karar vermek gerçekçi ve geçerli değildir. “Bypass” yapılacak damarların ileri derece kalsifik olması, “bypass” yapılacak bölgede doku kaybı ve infeksiyon bulunması bu yöntemin tercih edilmemesinde geçerli bir sebeptir. 2021 yılında güncellenen Periferik Arter ve Ven Hastalıkları: Ulusal Tedavi Kılavuzu’nda (190), KETİ kliniğiyle başvuran hastalara revaskülarizasyon açısından yapılan önerilerden bazıları aşağıda özetlenmiştir:
- KETİ kliniğiyle değerlendirilen, WIfI sınıflamasıyla yüksek evre iskemi bulunan ve revaskülarizasyondan fayda görmesi öngörülen hastalarda, ayak kan akımını artıracak mümkün olan en doğrudan revaskülarizasyon ivedilikle önerilir.
- Revaskülarizasyon yapılacak hastalarda yapılabiliyorsa safen ven greft ile “bypass” düşünülmelidir. Revaskülarizasyon yapılacak ve cerrahi açıdan yüksek riskli görülen hastalarda ise endovasküler revaskülarizasyon, işlem riskini azaltmak üzere deneyimli merkezlerde uygulanmalıdır.
- Endovasküler revaskülarizasyon yapılacak hastalarda, ilaçlı balon uygulaması seçici olarak düşünülmelidir.
Soru 9: Diyabetik Ayak Yarası Olan Olgularda Endovasküler Girişimlerin Cerrahi Girişime Oranla Bir Üstünlüğü Var mıdır?
Revaskülarizasyon kararı alınmış hastalarda açık cerrahi veya kapalı endovasküler yöntemden hangisinin kullanılacağının kararı; iskeminin derecesine, arteriyel hastalığın yaygınlığına, yaranın büyüklüğüne, infeksiyon olup olmamasına/varsa derecesine ve işlemi yapacak hekimin/ merkezin tecrübesine bağlıdır. Hangi revaskülarizasyon işleminin daha uzun açık kalmayı sağladığı hususunda görüş birliği bulunmamakla birlikte endovasküler girişim yaklaşımı günlük pratikte ağırlık kazanmaktadır. Genç, aktif hasta grubunda, uzun segment arteriyel tıkanıklık olan hastalarda, iyi kalitede otolog ven grefti olan hastalarda “bypass” cerrahisi tercih sebebi olabilir. Bu anlamda en nesnel veri, yakın tarihli randomize bir çalışma olan BEST-CLI çalışmasıyla elde edilmiştir (195). Söz konusu çalışmada, otolog safen ven greft ile “bypass” yapılan olgularda ekstremite tehdit edici olayların veya ölümün anlamlı olarak azaldığı ancak protez greft kullanımıyla endovasküler yaklaşım arasında anlamlı bir fark olmadığı ortaya koyulmuştur. Diz altı bölgeye müdahale gerektiren olgularda endovasküler ve cerrahi “bypass” sonuçlarını randomize bir yöntemle karşılaştıran BASIL-2 çalışmasında ise endovasküler tedavinin cerrahi tedaviye göre ampütasyon olmadan daha yüksek sağkalım ile sonuçlandığı bildirilmiştir (196). Dolayısıyla endovasküler girişimler, gelişen teknoloji ve randomize çalışmalardan gelen veriler sonucunda daha yaygın olarak gerçekleştirilmektedir. Kullanılan opak maddenin kompanse böbrek yetmezliğine sahip hastalarda kontrast nefropatisine yol açma ihtimali bulunmakla beraber, KA gibi kullanılan kontrast miktarını azaltan yeni yöntemler ile bu hasta grubunda da endovasküler yöntemler tercih edilebilmektedir. Kullanılacak yöntemin seçiminde birçok faktör göz önünde bulundurulmalıdır; örneğin hasta ile ilgili faktörlerde, hastanın genel durumunun ve ko-morbiditelerinin operasyon açısından uygun olup olmadığı, ameliyatın getirdiği peroperatif morbidite ve mortalite, uygun ven kondüiti bulunup bulunmadığı, darlık ve tıkanıklıkların anatomik özellikleri sayılabilir. Bu işlemleri yapacak merkezin alt yapısı, imkânları, ekibin her iki işlem ile ilgili tecrübeleri de diğer önemli faktörlerdir. Bu hastaları tedavi eden merkezlerin söz konusu iki yöntem ile ilgili tecrübe sahibi olmaları beklenmektedir. Hangi işlem yapılacak olursa olsun revaskülarizasyon kararını vermeden önce işlemin başarı oranı ve hastanın bu işlem sonunda kazanç ve kaybı iyi ortaya konmalıdır. Örneğin yaranın iyileşme ihtimalinin zayıf olduğu, tedavi sonrasında fonksiyon görecek yeterli doku kalmayacak ve yürüme fonksiyonunu yerine getiremeyecek bir ayak yarasında veya yaşam beklentisi az, yatağa bağımlı bir hastada ampütasyon en doğru tercih olabilir.
Soru 10: Diyabetik Ayak Yarası Olan Hastada Endovasküler ya da Cerrahi Tedavi Seçimi Kesin Ölçütlere Dayandırılabilir mi?
Safen ven grefti ile kalıcı ve iyi sonuçlar elde edilmekle beraber bu alanda daha fazla veriye ihtiyaç vardır. Günlük pratikte endovasküler tedavi yaygın olarak tercih edilmekle beraber kanıt seviyeleri kesin öneriler yapmak için yeterli değildir. Uluslararası Diyabetik Ayak Çalışma Grubu; endovasküler, cerrahi veya hibrid tedavi seçenekleri arasında hasta bazında tedavi seçimini önermiştir. Ancak otojen safen ven grefti kullanılabilecek olgularda cerrahi “bypass” tercih edilmelidir (177). Periferik arter hastalığının morfolojik dağılımı, otojen greft uygunluğu, eşlik eden morbidite yanında merkezin ve hekimin tecrübesi, imkanlar ve tedavi olanaklarına erişim gibi seçenekler de göz önüne alınarak merkeze göre özelleştirilmiş endovasküler, cerrahi veya hibrit yaklaşımlar tercih edilebilir.
CHARCOT NÖROARTROPATİSİ
Soru 1: Charcot Nöroartropatisinin Varlığı, Diyabetik Ayak İnfeksiyonu Tedavisini Nasıl Etkiler?
Charcot nöroartropatisi, duyusal nöropatisi olan hastalarda kemik ve eklemlerde deformiteye neden olan ilerleyici bir hastalıktır. Nöropatik artropati olarak da anılan bu patoloji ilk olarak sifiliz hastalarında tanımlanmış olmakla birlikte günümüzde en sık diyabetik hastalarda karşımıza çıkmaktadır. Diyabetik hastalardaki prevalansı %0.09-1.4 arasındadır (197). Hastalık klinik olarak dört evrede değerlendirilir. Modifiye Eichenholtz sınıflaması olarak anılan bu evreleme sisteminin her evresi DAİ hastasındaki yaklaşımı etkileyebilir:
Evre 0’da ayak/ayak bileğinin etkilenen bölgesinde kızarıklık, şişlik ve ısı artışı izlenir. Evre 1’de ise mevcut bulgulara ek olarak eklem deformitesi ve instabilite görülür. Evre 0 ve Evre 1 akut dönemi oluşturur ve hastalarda izlenen bulgular aynı zamanda DAİ’de de karşılaşılan bulgulardır. Bu durum yanlış tanı ve tedaviye, tanıda gecikmelere veya daha önce infekte olmayan Charcot ayağının, infekte Charcot ayağına dönüşmesine ve tablonun daha da karmaşık bir hale gelmesine neden olabilir. Akut DAİ ile Charcot ayağı arasında ayırıcı tanının yapılabilmesi için bazı ipuçları şunlardır:
- Ayak infeksiyonu, sıklıkla ayağın yüklenmeye açık bölgelerinden ve sıklıkla tek bir noktadan başlar. Charcot ayağı ise en sık ayak ortasından, normalde yüklenmeyen bölgede başlar.
- DAİ hastası öyküsünde, genellikle hastanın bildiği bir bası yarası, tırnak batması veya yaralanma bulunur; Charcot ayağı olgusunda ise genellikle hiçbir önemli bulgu yoktur.
- DAİ olgusunda infeksiyon parametreleri yüksek olabilirken, Charcot ayağında normal veya normalden biraz yüksektir.
- Nöropatisi olan ve tipik inflamasyon bulguları izlenen bir hastada (kızarıklık, şişlik ve ısı artışı, vb.) her iki ekstremite karşılaştırıldığında 2 °C’den fazla sıcaklık farkı varken radyografik patoloji tespit edilemediyse tanı büyük olasılıkla akut CN’dir (198).
- Son olarak, etkilenen ekstremitenin birkaç dakika elevasyona alınması ile kızarıklığın gerilemesi de infeksiyon ile ayırıcı tanıda akut CN tanısını destekleyen bir diğer bulgudur (197).
Akut Charcot düşünülen bir hastada MRG ile hastalığın erken evrelerinde görülen kemik iliği ödemi gibi bulgular, radyografik bulgular vermeden izlenebilir ancak bu bulgular aynı zamanda osteomyelit ile de karıştırılmasına neden olabilir. Bu hastalarda özellikle ayak ortasında birden fazla kemik tutulumunun olması ve eklem çevresinde ödem izlenmesi, CN lehine değerlendirilen MRG bulgularıdır (199).
Evre 2’de; kızarıklık, şişlik ve ısı artışı gibi klinik bulgular gerilemiştir ancak instabilitenin de artması ile birlikte deformitelerde artış izlenir. Bu durum özellikle nöropatisi olan bir hastada basınç artışı ve oluşan ekzositozlarla birlikte ülserasyonların gelişimine neden olur. Bası kaynaklı ülsere olmuş bir lezyon kolaylıkla DAİ ile karışabileceği gibi sıklıkla osteomyelit ile de komplike olur. İnfekte olmayan bir lezyonu olan hastada yükten sakınma ve tam temas alçılama gibi tedaviler ile yara iyileşmesi sağlanmakla birlikte infeksiyon eklenmiş olgularda acil debridman gerekli olabilir. Bu olgularda da debridman genel kurallara göre yapılmalıdır. Charcot ayağı hastasında infeksiyonun nöropatik eklemlere ulaştığı gözlenirse, debridmanın bu eklemleri de kapsaması gerekli olabilir. Charcot ayağı gelişen hastalarda debridman sonrasında atel yardımıyla immobilizasyon sağlanması uygun olacaktır.
Evre 3 ise rekonstrüksiyon evresidir ve klinik bulgular ortadan kalkmakla birlikte deformite rijid bir hal almıştır. Bu evrede Lisfranc ligamentinin hasar görmesi ile birlikte metatarsal dislokasyon gelişir, ayak arkı çöker ve tipik “beşik ayak” deformitesi ortaya çıkar (200). Bu hastalarda mevcut deformiteye ek olarak infeksiyon nedeniyle yapılan debridmanın yol açtığı hasar da eklendiğinde, rekonstrüksiyonun daha sorunlu ve başarısının da düşük olması beklenir.
REKONSTRÜKSİYON
Soru 1: Rekonstrüksiyon Girişimi Uygulanması İçin Hangi Ölçütlerin Sağlanması Gereklidir?
Diyabetik ayak infeksiyonu sonrası yapılan rekonstrüksiyon girişiminin hedefi, ayak bileğinin nötral pozisyona kadar gelebilmesini ve ayak tabanının yere dengeli olarak basmasını sağlamaktır. Ayak tabanında yük alan bölgelerin travmaya dayanıklı epitel içeren bir doku ile kapatılması gereklidir. Diyabetik ayak infeksiyonu hastasında rekonstrüksiyon denemelerinin başarısız olması, daha kompleks onarımlarla ya da bir üst düzeyde ampütasyonla sonuçlanacaktır. İnfeksiyon; başlangıç bölgesinde (primer odak) ve ayak ve bacakta yayılma yolları boyunca, çeşitli dokularda tahribata (nekroz) yol açar. Ortaya çıkan bu nekrozun zaman içerisinde debridmanlarla uzaklaştırılması gerekir Ayağın, yapılacak debridman ve rekonstrüksiyon için yeterli dolaşıma sahip olduğundan emin olunmalıdır. Dikkatli yapılmış debridman ve pansuman süreci sonunda yara alanı nekrozdan tümüyle arındırılmış olur. Bu nedenle, bir rekonstrüksiyon girişiminden önce bölgedeki infeksiyonun iyileştiğinden emin olunmalı, varsa vücuttaki başka infeksiyon odakları da ortadan kaldırılmalıdır. Rekonstrüksiyon sırasında ilk aşamada nekrotik materyal radikal bir debridmanla yaradan uzaklaştırılmalı ve osteomyelitli kemik dokusu kalmamış olmalıdır. İnfeksiyon parametrelerinin normale veya normale yakın düzeye dönmüş olması istenir. Günümüzde ayak tabanındaki yaraların kapatılması için lokal flepler, bölgesel flepler, serbest flepler ve hücreden arındırılmış dermal matriksler yoğun olarak kullanılmaktadır.
Soru 2: Yaranın Kapatılması Nasıl Sağlanmalıdır?
Diyabetik ayak yaralarının cerrahi tedavisi için tanımlanmış pek çok ameliyat vardır (Tablo 6); DA cerrahisiyle uğraşan her cerrahın bu ameliyatları bilmesi ve yaptığı ameliyatı tanımlaması bilimsel olduğu kadar sağlık sistemimizin işleyişi açısından da bir gerekliliktir. Hemen her cerrahi alan için başta gelen primer kapama yöntemi, rekonstrüktif cerrahinin de en sık başvurduğu yara kapama yöntemidir. Bunun dışında kalan yara kapama yöntemleri olarak kısmi kalınlıklı (“split-thickness”) deri greftleri, tam kat (“full-thickness”) deri greftleri, lokal deri flepleri, fasya ya da kas içeren flepler, serbest flepler sayılabilir.
Soru 3: Ampütasyon Seviyeleri Nasıl Belirlenir, Avantaj ve Dezavantajları Nelerdir?
Ampütasyonun seviyesine ve tekniğine; yaralanmanın derecesi, alt ekstremitedeki vaskülopatinin ciddiyeti, hastanın genel sistemik durumu gibi faktörler ışığında karar verilir (201). Diyabet ilişkili alt ekstremite ampütasyonları majör ve minör ampütasyonlar olarak iki alt kategoride incelenebilir. Minör ampütasyonlar kısıtlı bir doku eksizyonunun yapıldığı ve ayak bileği seviyesinde veya altında olan ampütasyonlar olarak tanımlanırken; majör ampütasyonlar ayak bileği seviyesi üzerinde olan ampütasyonlar olarak tanımlanırlar.
Minör ampütasyonlar içerisinde; dijital ampütasyonlar, ışınsal (ray) ampütasyonlar, transmetatarsal, tarsometatarsal (Lisfranc) ve transtarsal (Chopart) ampütasyonlar bulunmaktadır (202). Dijital ampütasyonlar parmaklardaki derin ülserlerde veya osteomyelit kaynaklı kemik destrüksiyonu olması durumunda uygulanır. Üç veya dört parmağın etkilendiği durumlarda, dijital ampütasyon yerine transmetatarsal ampütasyon uygulaması ile yara yeri problem gelişiminin ve re-ampütasyon riskinin önüne geçmek mümkün olabilir. Etkilenen parmak ve karşılık gelen metatarsal kemiğin osteomyelitinde ise ışınsal (“ray”) ampütasyonlar ile tedavi planlanabilir. Vasküler problemin proksimale uzanması, yaygın infeksiyon varlığı veya sağlıklı ve gergin olmayan bir yumuşak doku örtünümünün sağlanamayacağı durumlarda ise ayak ortasından (Lisfranc veya Chopart) bir ampütasyona ihtiyaç duyulabilir. Boyd ve Prigoff ampütasyonları ise ayak önünün kurtarılamayacağı ancak ayak arkasının görece korunabildiği seçilmiş bir hasta grubunda tercih edilebilir; ancak yüksek komplikasyon oranları nedeniyle diyabetik hastalarda ayak arkası ampütasyonları yerine diz altı ampütasyonu daha çok kullanılmaktadır (203).
Majör ampütasyonlar ise diz altı ve diz üstü ampütasyonları olarak sıralanabilir; minör ampütasyon sonrasında yara iyileşmesi problemi olması, infeksiyonun kontrol edilememesi veya hastanın mobilize olamadığı durumlarda tercih edilebilirler. Periferik arter hastalığı olan ve ayakta dolaşım problemi olan hastalarda tercih edilen seviye diz altı ampütasyonudur. Popliteal arter oklüzyonu olup arteryel rekonstrüksiyonun mümkün olmadığı yaşlı hastalarda, dizde fleksiyon kontraktürü gelişmiş hastalarda ve cerrahi açısından yüksek riskli hastalarda re-ampütasyon riskini azaltmak için diz üstü ampütasyon seçenekleri tercih edilebilir.
Minör ampütasyonlar sonrasında hastaların kısa mesafelerde, desteksiz yürümesi mümkün olabilirken; tekrarlayan debridman, yara yeri problemi ve re-ampütasyon gereksinimi gibi riskler planlama esnasında akılda tutulmalıdır. Majör ampütasyonların yarattığı ciddi morbidite ve cerrahi sonrası artmış mortalite oranları nedeniyle uygun diyabetik hastalarda ekstremite koruyucu cerrahilerin kullanımı tercih edilmelidir.
YARA BAKIMI
Soru 1: Yaranın Pansumanı Nasıl Yapılmalıdır?
Pansumanın amacı, yaranın iyileşmesi için optimal şartları oluşturarak vücudun doğal iyileşme sürecini desteklemek ve yarayı korumaktır. Kronik yara tedavisinde yara iyileşmesini engelleyebilecek olumsuz lokal şartların düzeltilmesi yara yatağı hazırlığı olarak adlandırılmaktadır. TIME konsepti yara yatağı hazırlığının temel prensiplerini tanımlamaktadır; devitalize dokuların yaradan uzaklaştırılmasını, yani debridmanı (“tissue”), infeksiyonun kontrol altına alınmasını (“infection”), optimal nem dengesinin sağlanmasını (“moisture”) ve yara kenarlarının düzeltilmesini ve epitelizasyonun sağlanmasını (“edge” / “epithelization”) içerir (204, 205). Pansumandan önce mutlaka uygun debridmanla; devitalize dokular, nekroz, debris, yabancı cisimler yaradan uzaklaştırılmalı ve seçilecek doğru antiseptikle yara temizliği yapılmalıdır. Ayrıca tüneller belirlenmeli, gerekli yerlerde dekolasyon yapılmalıdır. Aksi takdirde kullanılan yara bakım ürünlerinin yara yatağına ulaşması mümkün olmayacak ve beklenen fayda sağlanamayacaktır. Pansumanlar tüm yara yatağına temas edecek, kaviteleri dolduracak şekilde yapılmalıdır. Bu işlemler sırasında kullanılacak sistemik antibiyotik seçimi için mutlaka doku kültürü alınmalıdır. Yara iyileşmesi için nem dengesi de çok önemlidir. Pansumanlar fazla sıvıyı absorbe ederek ortamdan uzaklaştırmalı ancak dokudan buharlaşma ile nem kaybını engellemelidir. Eski yıllarda kullanılan tampon, gaz ve ıslak-kuru pansumanların yerini günümüzde büyük ölçüde modern yara örtüleri almıştır. Pansumanlarda kullanılabilecek farklı emici özelliğe sahip çok sayıda yara örtüsü bulunmaktadır (206). Kuru yaralar nemlendirilmeli, eksudalı yaralarda ise fazla sıvı uzaklaştırılarak eksuda kontrolü sağlanarak kurutulmalıdır. Kullanılan yara örtüleri aynı zamanda mikroorganizmalar için bir fiziksel bariyer oluşturarak bakteri sayısının kontrolüne katkıda bulunur. İnfekte ve kritik kolonize yaralarda antimikrobiyal yara örtüleri tercih edilebilir. En sık olarak tercih edilenler gümüşlü örtülerdir. Topikal uygulanan antibakteriyal pomadların ise tedavide kullanılmasına yönelik güçlü hiçbir kanıt yoktur. Antimikrobiyal yara örtülerinin kullanımının ortalama iki hafta ile sınırlandırılması ve bu sürenin sonunda yaranın tekrar değerlendirilmesi ve buna göre tedavinin planlanması önerilmektedir (207).
Pansumanlarda kullanılacak yara bakım malzemelerine karar verirken; yaranın tipi (yüzeyel, derin, kaviteli, vb.), yara iyileşmesinin hangi aşamada olduğu, yaranın özellikleri (kuru, nemli, aşırı eksudalı, kötü kokulu, ağrılı, kolay kanayan, vb.), yaranın bakteri yükü (steril, kolonize, infekte, vb.), hastanın özellikleri (yaşlı, gebe, diyabetik, çocuk, vb.), yaranın vücuttaki yeri, tedavinin yapılacağı yerin özellikleri (hastanede, evde, vb.) ve ürün maliyetleri-geri ödeme koşulları gibi pek çok faktör göz önünde bulundurulmalıdır (208). Yara iyileşmesi dinamik bir süreç olup yara tedavisi de öyle olmalıdır. Her pansuman değişimi sırasında yaranın iyileşme aşaması ve ihtiyaçları tekrar değerlendirilerek ürün seçimi güncellenmelidir. Tedavide en uygun diye seçtiğimiz malzeme maserasyona ve alerjik reaksiyona yol açabilir; tercihimizi değiştirmek zorunda kalabiliriz.
Soru 2: Yara Bakım Malzemelerinin Özellikleri Nelerdir?
Yara bakım malzemelerini kullanma amacımız yara iyileşmesini desteklemek ve hızlandırmak, komplikasyon riskini azaltmak, tedavi sırasında hastanın günlük yaşantısına konforlu olarak devam etmesini sağlamak ve yaşam kalitesini artırmaktır. İdeal yara bakım malzemesi hem yaradan sıvı kaybını önlemeli hem de eksuda kontrolü yaparak optimal nem dengesini sağlamalı, maserasyona yol açmamalı, yara ve çevresini mikroorganizmalar, yabancı cisimler ve travmadan korumalı, ısı kaybını önlemeli, kompresyon yaparak ödemi azaltmalı ve hemostaza katkı sağlamalı, ölü boşlukları doldurmalı, koku ve ağrı kontrolünü sağlamalıdır. Kullanılacak yara bakım malzemesi steril ve biyouyumlu olmalı, yara yüzeyinde kalıntı bırakmamalı, alerjiye yol açmamalı, çok sık değişim gerektirmemeli, kolay uygulanabilir ve kolay değiştirilebilir olmalı, hastanın hareketleri ile uyumlu yapıda farklı lokalizasyonlarda kullanabilmek için değişik boyut ve şekil seçenekleri bulunmalı ve son olarak da ekonomik olarak ulaşılabilir durumda olmalıdır. Günümüzde tüm bu beklentilerimizin hepsini karşılayacak, her yaraya uygun tek bir yara bakım malzemesi bulunmamakta fakat farklı özelliklerde çok geniş bir ürün yelpazesi bulunmaktadır. Yani yara tedavisinde mucize ürün yoktur; klinisyen tarafından doğru seçilen ve doğru uygulanan ürünler vardır. Yaraya ait özellikler, hastaya ait özellikler ve ürünün özellikleri göz önünde bulundurularak hangi yara bakım malzemesinin kullanılacağına karar verilmelidir (209). Yara tedavisinde pasif örtüler en sık kullandığımız yara bakım malzemeleridir (206,210). Hidrojeller hidrofilik polimer ve sudan oluşur, içerdiği su miktarına göre değişik viskozitede olabilir. Rehidratasyon yaparak nemli ortam oluştururlar ve tercihan debridman yapılması istenen nekrotik dokularda sık tercih edilirler. Poliüretan yapıdaki transparan filmler ise yarı geçirgen bir özelliğe sahiptir; nemi koruyarak ve bakteriyel kontaminasyonu engelleyerek iyi bir bariyer oluştururlar. Pektin veya karboksimetilselülozdan yapılan hidrokolloidler ve hidrofiberler, poliüretan köpük ve süperabsorban polimer yara örtüleri değişik derecelerde emici özelliğe sahip olup eksuda kontrolü sağlayarak yaradaki nem dengesini korurlar. Uzun yıllardır yara tedavisinde yeri olan, deniz yosunlarının polisakkaritlerinden üretilen aljinatlar ise köpüklerden daha fazla emici özelliğe sahiptir; ciddi eksüdanın kontrolünü sağlarlar. Gevşek lifli yapıları sayesinde özellikle derin ve düzensiz yüzeyli, kaviteli yaralarda kullanılabilir. Polimerik membran nem ile aktive olan bir temizleme sistemine sahiptir; yara yatağını temizler, nemlendirir ve fazla eksudayı absorbe ederek yara yatağında sıvı dağılımını düzenler.
Son yıllarda yara tedavisinde kullandığımız farklı örtüleri tek bir ürün yapısında bir araya getiren kompozit yara örtüleri geliştirilmiştir. Bu çok tabakalı örtülerde genellikle yara yüzeyine yapışmayı engelleyen ve bir arayüz oluşturan yara temas tabakası, nem dengesini sağlayan bir emici tabaka ve bariyer fonksiyonuna sahip bir film tabaka bulunmaktadır. Kompozit yara örtüleri sayesinde çok farklı özelliklerden aynı anda yararlanmak mümkün olmaktadır.
Antimikrobiyal yara örtülerinde en sık kullanılan antiseptikler; gümüş, aktif karbon, poliheksametilen biguanid, klorheksidin ve iyottur. Antiseptikler geniş spektrumlu antimikrobiyal etki ve düşük toksisiteye sahip oldukları ve etkilerine direnç gelişmediği için yara bakım ürünlerinde tercih edilirler. İnfekte yaralar her zaman eksuda ile birliktedir; antimikrobiyal yara örtüleri ile hem eksuda kontrolü hem de hızlı ve sürekli antimikrobiyal etki sağlanabilir (211).
Kollajen çok farklı formlarda yara tedavisinde kullanılmaktadır. Yara iyileşmesinin tüm basamaklarında etkilidir (212). Yarayı nemlendirir, büyüme faktörlerini tutar, fibroblast ve keratinositler için kemotaktik etkilidir; artmış matriks metalloproteazları inaktive eder, kollajen matriks depolanmasını artırır ve hemostatik etki sağlar. Hyalüronik asit de son yıllarda yara tedavisinde yer almıştır; absorbsiyon kapasitesi çok yüksektir, nemlendirici etkiye sahiptir, fibroblast ve keratinositlerin migrasyon ve proliferasyonunu kolaylaştırır, büyüme faktörleri için rezervuar oluşturur (213).
Tedavide gittikçe daha yaygın kullanılan ve aktif pansumanlar olarak kabul edilen negatif basınçlı kapamalar ve gittikçe gelişen deri eşdeğerleri ise ayrı bölümlerde incelenmesi gereken değerli pansuman örtüleri olarak kabul edilmelidir.
Yara tedavisi sırasında çok önemli bir diğer konu da yara çevresinin korunmasıdır. Yara kenarında kuruluk veya maserasyon sıklıkla görülebilmektedir. Polimerize film bariyerler akrilik ya da silikon yapıda transparan bir tabaka oluşturarak yara çevresini korur. Vazelin dimetikon ve çinko içeren bariyer krem ve merhemler de yara çevresine uygulanabilir.
METABOLİK KONTROL
Soru 1: Diyabetik Ayak Yarası Olan Hastalarda Metabolik Kontrol Nasıl Sağlanmalıdır?
Diyabetik ayak yarası olan hastalarda dikkatli anamnez ve fiziki muayene bulgularından da faydalanılarak, hiperglisemi, nöropati, hipertansiyon ve hiperlipidemi odaklı tedaviler planlanmalıdır. Tüm DA yarası olan hastalarda iyi glisemik kontrol sağlanması hedeflenmelidir. Ayaktan tedavi edilecek hastaların DA yarası ve infeksiyonunda glisemik kontrol hedefleri komplikasyonsuz diyabetlilerden farksızdır. Açlık kan şekeri, tokluk kan şekeri, HbA1c, kan basıncı, kan lipidlerinin hedefte tutulması, organ fonksiyonlarının korunması, mikrovasküler ve makrovasküler komplikasyonların önlenmesi tedavinin temel amaçlarıdır. Kan glisemi düzeyleri ve tedaviye uyum her aşamada değerlendirilmelidir (214). Diabetes mellitus tedavisinde görülen metabolik sorunlar; eğitim, tıbbi beslenme tedavisi, vücut ağırlığın kontrolü, gerektiğinde medikal tedavi (oral antidiyabetikler ve/veya enjeksiyon tedavileri) ile yönetilmektedir (214,215).
Soru 2: Glisemik Kontrol Hedefleri Ne Olmalıdır?
İnfeksiyon ve yaranın derecesi dışında uzun diyabet süresi, düşük yaşam beklentisi, ciddi hipoglisemi atakları, azalmış renal fonksiyonlar, eşlik eden mikro ve makrovasküler komplikasyonlar, eşlik eden hastalıklar ya da diyabet kontrolünün uzun süredir kötü olması durumlarında glisemik hedefler esnek tutulmalı ve HbA1c düzeyinin <%8.0 altı yeterli kabul edilmelidir. Yarası yüzeysel olup hastanede yatmayan, komorbiditeleri bulunmayan, hipoglisemiye eğilimli olmayan ve yaşam beklentisi uzun olan, düşük riskli hastalarda HbA1c <%7.0 düzeyinde tutulmalıdır. Açlık kan glukoz düzeyinin 80-130 mg/dl arasında ve ikinci saat postprandiyal (zirve) kan glukoz düzeyinin 180 mg/dl’nin altında olması hedeflenmelidir (2,216).
Hastanede yatmayan ve Meggitt-Wagner sınıflamasına göre derece 3 yarası olan orta riskli hastalarda ek komorbiditeler yoksa kan glukoz düzeyinin açlık veya öğün öncesinde 130 mg/dl’yi aşmaması, tokluk döneminin ikinci saatinde zirve düzeyi 180 mg/dl’nin altında ve HbA1c hedefinin %7-7.5 olması yeterlidir (Tablo 7) (214,215).
Hastaneye yatırılarak insülin tedavisi başlanan, kritik olan veya olmayan hastalarda hedeflenen glisemi düzeylerinin 140-180 mg/dl arasında tutulması önerilmektedir. Hipoglisemi (<70 mg/dl) yaşamayan seçilmiş hastalarda; 110-140 mg/dl veya 100-180 mg/dl gibi daha sıkı hedefler belirlenebilir (215,217).
Kan glisemi düzeyleri hakkında hızlı, doğru ve uygun karar vermek için diyabet teknolojileri (sürekli cilt altı glukoz ölçüm yöntemleri, kapalı sistem insülin infüzyon pompaları, vb.) kullanılabilir. Glisemi değişkenliği (% değişim katsayısı) hedefi ≤%36, okunan sürelerde normal sınırlar 70-180 mg/dl, birinci düzeyde hiperglisemi 181-250 mg/dl, birinci seviye hipoglisemi 54-69 mg/dl ve ikinci düzey hipoglisemi <54 mg/dl olarak tanımlanmıştır. Hipoglisemi riski yüksek olanlarda hedeflenen sürenin >%50’nin üzerinde ve hipoglisemi oranının <%1’in altında olması önerilmektedir (2,216).
Hospitalize DA Yarasında Glisemik Kontrolün Sağlanması
Hospitalize edilen hastanin HbA1c düzeyi ölçülür, önceki diyabet tedavisi hakkında detaylı bilgi sahibi olunur ve diyabet eğitimi tekrarlanır. Bu yaklaşımın, hastaların hastaneden ayrıldıktan sonraki süreçte de diyabet tedavisine uyumunu artırdığı bildirilmiştir. Diyabetik ayak yarası nedeni ile hospitalize edilen ve kritik durumda olmayan diyabetli hastalarda glukoz düzeylerinin 100-180 mg/dl aralığında tutulması hedeflenmelidir. Ardışık yapılan en az iki ölçümde kapiller glukoz ≥180 mg/dl ise insülin başlanmalıdır. Önerilen tedavi protokolü bazal-bolüs insülin tedavisidir (216).
Kritik durumda olan hastalarda 100-250 mg/dl glukoz düzeyleri hedef glisemi değerleri olarak belirlenmiştir. İntravenöz insülin tedavisi en etkin tedavi şeklidir; intravenöz insülin infüzyonu gereken hastalarda insülin dozlarının hesaplanması için yapay zekâ uygulamalarının kullanılmasının, düşük hipoglisemi riski nedeni ile daha iyi bir glisemik kontrol sağladığı gösterilmiştir (218).
Optimal glisemik kontrol infeksiyonun iyileşme sürecini hızlandırır ve hastanede yatış süresini kısaltır. Ancak, iyi glukoz kontrolü hedeflenirken hipoglisemik atak sıklığını artırmamak da amaçlanmalıdır. Kapiller glukozun 100 mg/dl seviyelerine inmesi, hipoglisemi riskinin arttığının habercisi olarak kabul edilmeli ve önlem alınmalıdır.
Glukoz monitorizasyonu; oral alımı olan diyabetlilerde her öğün öncesi ve öğünlerden iki saat sonra kapiller glukoz takibi şeklinde yapılmalıdır. Oral beslenemeyen hastalarda ise her 4-6 saatte bir kapiller glukoz ölçülmelidir. İntravenöz insülin infüzyonu alan olgularda saat başı veya iki saatte bir ölçüm yapılması gereklidir. Sürekli glukoz monitörizasyonu (“continuous glucose monitor” – CGM) cihazları interstisyel dokuda her dört dakikada bir glukoz ölçümü yaparak yakın glisemi takibine olanak veren cihazlardır. Gerçek zamanlı (“real-time”) veya “flash” CGM cihazlarının kullanımı hastanede yatan kritik olmayan hastalarda düşük hipogilisemi riskini düşürür ve iyi glisemik kontrol sağlanmasına olanak sağlar (215).
Soru 3: Hiperglisemi Tedavisi Nasıl Planlanmalıdır?
Tip 1 diyabetlilerde mutlak insülin eksikliği olduğu için bazal-bolüs insülin rejimleri kullanılmaktadır. Tip 2 diyabetli bir hastada infekte olmayan bir ayak ülseri varsa, hastanın almakta olduğu oral antidiyabetik (OAD) tedavi altında iyi glisemik kontrol sağlanmışsa (HbA1c <%7) ve ilaca ait yan etki ya da kontrindikasyon yoksa tedavi değişikliği gerekmez.
Tiazolidinidonlarla ödem riskinde artış yara bölgesi için sorun olabilir. Metformin ve sodyum glukoz ko-transporter-2 inhibitörü (SGLT-2i; empagliflozin, dapagliflozin, vb) kullanmakta olan olgular hemodinamik bozukluk ve böbrek yetmezliği açısından dikkatle değerlendirilmelidir. Yara yerinde ciddi infeksiyon veya sepsis bulguları varsa; metforminle laktik asidoz riskinde, SGLT-2i kullanımında ise öglisemik ketoz riskinde artış olduğu için infeksiyon kontrol edilene dek bu ilaçlara ara verilmelidir.
Diyabetik ayak yaralı tip 2 diyabetli hastaların çoğunda glisemik regülasyonun kötü olması ya da eşlik eden ciddi komplikasyonlar bulunması nedeni ile orta-yüksek riskli ayak yarası olgularında insülin tedavisi tercih edilir. İnsülin tedavisi konvansiyonel veya bazal-bolüs uygulama olarak düzenlenebilir.
Meggitt-Wagner sınıflandırmasına göre derece 2-3 olan derin yaralarda infeksiyon riskini azaltmak için sıkı bir glisemik kontrol sağlanmalıdır. Hastanın almakta olduğu tedavi altında diyabet kontrolü hedef değerlere uygunsa tedavi değişikliği gerekmeyebilir. Ancak verilen tedavi altındaki kan glukoz düzeyleri yüksek seyreden hastalarda bazal bolüs insülin tedavisi planlanmalıdır.
Meggitt-Wagner sınıflaması derece 4 ve 5’te (PEDIS sınıflamasına göre derece 3-4) acil cerrahi girişim gerekebileceğinden bazal-bolüs insülin tedavisi yapılması daha uygundur. Bu hastalar çoğu kez hiperglisemiktir veya diyabetik ketoasidoz, hiperglisemik hiperozmolar durum ya da böbrek yetmezliği gibi ek metabolik sorunlar olabilir. Bu hastalarda hızla metabolik kontrol sağlanmalı ve operasyona hazır hale getirilmelidir. Glisemik kontrol için bazal bolüs insülin tedavisi yeterli olmazsa insülin infüzyonu planlanmalıdır. Kaydırma ölçekli (“sliding scale”) insülin tedavisi başlangıçta kısa süre için işe yarayabilir ancak özellikle oral beslenen hastalarda uzun süreli uygulanmasından kaçınılmalı, çoklu doz insülin tedavisi başlanmalıdır. Yara tedavisi ve diyabet kontrolünün yanı sıra, hipertansiyon, hiperlipidemi ve nöropati tedavisi de dikkatli yapılmalıdır. Ayrıca koroner arter hastalığı açısından hastalar olarak değerlendirilmelidir (214,215,219-221).
Diyabetik ayak yaralı hastalarda periferik anjiyografi gibi kontrast madde kullanılarak yapılacak radyolojik girişimlere gereksinim duyulabilir. Bu gibi işlemlerden 48-72 saat önce metformin ve SGLT-2i tedavileri kesilmelidir; kalp yetersizliği için tedavi indikasyonunun bulunması, kardiyovasküler ve renal koruma için önceliklendirilmiş olması glisemik regülasyondan bağımsız şekilde SGLT-2i grubu ilaçların kullanımını artırmıştır. Şüpheler güçlü olmamakla birlikte kanagliflozinle diyabete ilişkin alt ekstremite ampütasyon riskinde artış bildiren bir çalışmadan ötürü tüm SGLT-2i ilaçlar için risk bildirilmektedir. Bu grupta bulunan ilaçların ürün bilgilerinde alt ekstremite ampütasyonu ve Fournier gangreni riskinde artış olabileceğine ilişkin uyarı bulunmaktadır. Diğer OAD ilaçlar için ayak yarasına özel bir uyarı söz konusu değildir (214).
Preoperatif Glukoz Kontrolü
Elektif cerrahi uygulanacak olgularda mümkünse HbA1c düzeyinin %8’in altında olması sağlanmalıdır. Ameliyattan önceki 4-6 saat içinde glukoz 100-180 mg/dl aralığında olmalıdır. Metformin operasyondan bir gün önce, SGLT-2 inhibitörleri ise 3-4 gün öncesinden kesilmelidir. Gece bazal insülin kullanmakta olan hastalarda, bir önceki gece %25 doz azaltılması önerilmektedir. Müdahale sabahında, herhangi bir OAD verilmemeli, kullanılmakta olan “neutrol protamine hagedorn” (NPH) insülin günlük dozun %50’si, uzun etkili analog insülin toplam dozun %75-80’i şeklinde uygulanmalıdır. Oral alımı kesilen hastada her 2-4 saatte bir glukoz takibi yapılarak gerektiği durumlarda hızlı etkili analog insülin tedaviye eklenmelidir. “Glucagon-like peptide-1 agonist” (GLP-1 RA)’lerinin ameliyat öncesi kullanımına ilişkin yeterli veri bulunmamaktadır.
Ayak yarasının ve infeksiyonun kontrolü sağlanan hastanın diyabet tedavisi, hastaneden çıkarılma sürecinde endokrinoloji uzmanı tarafından yeniden ve detaylı olarak planlanmalıdır. Eğitim hemşiresi ve diyetisyen de diyabet ekibinin içinde yer almalıdır (215).
Soru 4: Diyabetik Ayak Yarası Olan Hastada Diyabetik Nöropati Tanısı Nasıl Konulmalı ve Tedavi Edilmelidir?
Diyabetik ayak yarası nedeniyle takip ve tedavi edilen bir hastada diyabetik nöropati tanısının konulması tekrarlama riski çok yüksek olan yeni ayak ülserlerin önlenmesi açısından büyük önem taşır. Tip 1 diyabetlilerde tanıdan beş yıl sonra, tip 2 diyabetlilerde ise tanı sırasında diyabetik nöropati açısından değerlendirme yapılması gereklidir.
Diyabetik sensorimotor polinöropati tanısı için öncelikle nöropati ile ilişkili pozitif (her iki ayakta yanma, iğne batması, elektrik çarpması, vb.) ve negatif (pamuğa basma, keçeleşme, his kaybı, vb.) semptomların sorgulanması gereklidir. Ancak, nöropati olgularının yaklaşık yarısında hiçbir semptom bulunmamaktadır, bu nedenle tanı için fizik muayene şarttır.
Sensorimotor polinöropatiden en erken etkilenen duyusal ince liflerdir. Bu nedenle hastalar erken dönemlerden itibaren nöropatik ağrı ve paresteziler tanımlar. Kalın duyusal liflerin tutulumu, keçeleşme ve protektif ağrı duyusu kaybı ile sonlanır. İnce ve kalın duyusal liflerin fonksiyonlarını aşağıdaki tanı testleri ile değerlendirmek mümkündür.
- İnce lif fonksiyonları; pinprick ve ısı duyusu.
- Kalın lif fonksiyonları; vibrasyon duyusu ve 10-g monoflaman.
- Protektif duyu; 10-g mononoflaman.
Bu testler, nöropatinin ve protektif duyu kaybının erken tanısına olanak vererek DA yarası geliştirmesi açısından risk taşıyan olguların belirlenmesini sağlar. Elektromiyografi (EMG) gibi ileri elektrofizyolojik tanı testleri ise sadece tanı konulamayan ve ileri tetkik gerektiren olgularda önerilmektedir.
Diyabetik sensorimotor polinöropatı tanısı alan tüm olgularda; kronik alkol kullanımı, B12 vitamini eksikliği, hipotiroidi, renal yetersizlik, maligniteler (bronkojenik karsinom, multipl myelom, vb.), infeksiyonlar (HIV, vb.), kronik inflamatuar demiyelinizan nöropati, kalıtsal nöropatiler, vaskülitler gibi diğer sensorimotor nöropati nedenleri dışlanmalıdır.
Diyabetik Sensorimotor Polinöropati Tedavisi
Diyabetik nöropatinin, nöropatik hasarı geriletmeye yönelik spesifik bir tedavisi ne yazık ki bulunmamaktadır. Tanı konulduğu andan itibaren sağlanan iyi metabolik kontrolün tip 1 diyabetli olgularda nöropati gelişimini önlediği ve progresyonunu geciktirdiği gösterilmiştir. Tip 2 diyabette de erken başlanan iyi glisemik kontrol nöropati progresyonunu yavaşlatabilmektedir. Bazı antidiyabetik ilaçların diğerlerine üstün etkileri olduğu, özellikle insülin direncine etkili oral antidiyabetiklerin olumlu etkisi bulunduğu bildirilmektedir (2,213-216).
Nöropatik Ağrı ve Tedavisi
Nöropatik ağrı, diyabetik nöropatinin yaşam kalitesini en olumsuz etkileyen ve belki de en disfonksiyonel komplikasyonlarından biridir. Mutlaka farmakolojik tedavi gerektirir. Pregabalin, duloksetin ve gabapentin ilk seçenek ajanlar olarak önerilmektedir. Monoterapide veya kombine tedavide, ağrıyı azaltarak yaşam kalitesini yükselttikleri bildirilmiştir (2,215,216,222).
Soru 5: Hipertansiyon Tedavisi Nasıl Planlanmalıdır?
Diyabetik ayak yarası olan hastaların yarısından fazlası hipertansiftir. Diyabetik hastalarda kan basıncı yüksekliği için eşik değeri ≥140/90 mmHg’dir. Eşlik eden hastalık, risk ve yaşa göre hedef kan basıncı değerleri olarak; 18-65 yaş aralığında 120-130/70-80 mmHg, 65-79 yaş aralığında 130-140/70-80 mmHg ve 80 yaş ve üzerinde 130-140/70-80 mmHg aralığı önerilmektedir (223). Hipotansiyondan kaçınılmalıdır. Antihipertansif tedavi alan hastalarda kan basıncının alt sınırının 120/70 mmHg olması güvenlidir (214,223).
Vücut ağırlığının kontrolü, sağlıklı beslenme, sigara ve alkolün bırakılması, düzenli egzersiz ve stres yönetimi kan basıncı hedeflerine ulaşılmasına önemli ölçüde katkıda bulunacaktır (214,223)
Hipertansiyon tedavisinde ilk tercih edilecek ilaç grupları anjiyotensin dönüştürücü enzim inhibitörleri (“angiotensin-converting-enzyme inhibitors” – ACEI) veya anjiyotensin reseptör blokerleri (“angiotensin receptor blockers” – ARBs) olmalıdır. Bu ilaçlar aynı zamanda albüminüriyi de azaltma yönünde olumlu etkilidir. Özellikle ACEI grubu ilaçlar kullanılırken kan kreatinin ve potasyum düzeylerinin yakından kontrolü önerilir. Beta-blokerler ise sadece atriyal fibrilasyon, kalp yetersizliği ve koroner arter hastalığı gibi hastalıklarda ilk seçenek tedavi olarak kullanılabilecek ajanlardır. Hipertansiyonlu hastalarda zaman ilerledikçe kombine ilaç ihtiyacı oluşur. Kan basıncı düzeyi ≥160/100 mmHg olanlarda hipertansiyon tedavisine öncelikle kombinasyon tedavisiyle başlanması önerilmektedir (215,223). Yapılan çalışmalar, bir diyabet hastasında ortalama üç antihipertansif ilaç grubu kullanmak gerektiğini göstermektedir. Kombinasyon tedavisinin ilk basamağında ACEI/ARB + kalsiyum kanal blokeri (KKB) veya ACEI/ARB+diüretik tercih edilmesi önerilir. Kan basıncı kontrol altına alınamazsa, ACEI/ARB+KKB+diüretik kombinasyonuna geçilir. Üçlü kombinasyonla da kontrol edilmezse mineralokortikoid reseptör antagonisti eklenmesi düşünülmelidir (215,223,224).
Soru 6: Hiperlipidemi Tedavisi Nasıl Yapılmalıdır?
Kötü glisemik kontrollü diyabetik hastalarda trigliserid yüksekliği ve HDL-kolesterol düşüklüğüyle seyreden bir dislipidemi vardır. Glisemik kontrol sağlandığı zaman diyabetik dislipidemi nispeten düzelir ancak LDL kolesterolün aterojenik potansiyeli devam eder. Diyabet bir kardiyovasküler hastalık eşdeğeri olarak kabul edilir ve bu nedenle LDL-kolesterol hedefleri normal topluma göre daha düşük olarak belirlenmiştir. Diyabetli bireylerin hedef lipid düzeyleri kardiyovasküler risklerine göre tespit edilir. Çok yüksek riskli hastalar olarak; aterosklerotik kardiyovasküler hastalıkları veya Evre 4 kronik böbrek hastalığı olan hastalar (eGFR <30 ml/dk), 10 yıllık kardiyovasküler nedenli ölüm riski ≥%10 olan hastalar, diyabetik hedef organ hasarlı (mikroalbuminüri, retinopati veya nöropatili) ve erken başlangıçlı >20 yıl üzeri tip 1 diyabetikler sayılabilir. Bu hastalarda LDL-kolesterol %50’den daha fazla ise düşürülmeli ve hedef <55 mg/dl olmalıdır. Bu hedefe ulaşmak için yüksek derecede etkili statinlerin kullanılması uygundur (215,224,225).
Yüksek Riskli Hastalar
On yıllık kardiyovasküler nedenli ölüm riski %5-9, total kolesterol >310 mg/dl, LDL kolesterol >190 mg/dl veya kan basıncı ≥180/110 mmHg veya Evre 3 böbrek hasarı (eGFR 30-59 ml/dk) olanlar, hedef organ hasarı (mikroalbuminüri, retinopati veya nöropati) gelişmemiş, diyabet süresi ≥10 yıl, ya da ilave bir risk faktörü olan diyabetli olgularda LDL-kolesterol %50’den daha fazla düşürülmeli ve hedef <70 mg/dl olmalıdır (214,215,224,225).
Orta Düzeyde Riskli Hastalar
On yıllık kardiyovasküler nedenli ölüm riski %1-4, diyabet süresi <10 yıl ve bir başka risk faktörü bulunmayan genç hastalarda (tip 1 diyabet <35 yaş, tip 2 diyabet <50 yaş) LDL-kolesterol hedefi <100 mg/dl olmalıdır (214, 215, 224, 225).
HDL-kolesterol düzeyi erkekte >40 mg/dl ve kadında >50 mg/dl, trigliserid düzeyi <150 mg/dl olmalıdır. Hiperlipidemi tedavisinde kolesterol yüksekliği ön plandaysa statinler (simvastatin, atorvastatin, rosuvastatin), glisemik kontrol sağlandığı halde trigliserid düzeyi yüksekse fibratlar (fenofibrat, gemfibrozil) tercih edilmelidir (214,215,224, 225).
YÜKTEN KURTARMA
Soru 1: Diyabetik Ayak İnfeksiyonlarında Yükten Kurtarma İndikasyonları Nelerdir?
İnfeksiyonlu bir dokunun yük alması bölgesel kan dolaşımını fizyolojik sınırların altına düşürebileceği gibi inflamasyonun artmasına ve yayılmasına da neden olabilir. İnfeksiyon bulunan tüm yaralar yükten kurtarılmalıdır. Diyabetiklerde yükten kurtarma ile ilgili ilk ve en önemli indikasyon yara oluşumunun engellenmesidir. Plantar basınç dağılımı analizi gibi ülserasyon riskinin önceden belirlenebilmesine olanak veren yöntemlerle, aşırı basınç, yüklenme ve sürtünme altında kaldığı saptanmış olan ayak bölgelerinin yükten kurtarılmasıyla yara oluşumu önlenebilmektedir (226,227).
IWDGF’nin diyabetik ayak ülserlerinde yükten kurtarma konusundaki önerilerine göre, diyabetli ve nöropatik plantar ön ayak veya orta ayak ülseri varlığında, aktivite düzeyi ve ambulatuvar düzeyi dikkate alınarak ülser iyileşmesini desteklemek amacıyla uygun yükten kurtarma uygulamaları endikedir. Statik durumda 10 kg/cm2, dinamik durumda 50 N/cm2 üzerindeki basınçların ülserasyon riskini artırdığı bilinmektedir (40,228). Ayak plantarındaki basıncı azaltmanın en etkili yolu olan ortezler, basıncı mümkün olan en geniş alana dağıtarak görev yapar. En uygun ortez, artmış basınç alanlarındaki basıncı en çok azaltabilecek şekilde tasarlanan ortezdir (229).
İyileşmiş plantar ayak ülserinin tekrarlamasını önlenmeye yönelik olarak, yürüme sırasında plantar basınç artışını giderici terapötik ayakkabılar primer müdahale olarak belirlenmiş olup bu ayakkabıların giyilmesi teşvik edilmektedir (226,230,231). Ek olarak, söz konusu ayakkabılarla birlikte, yükten kurtarma yönünde tasarlanmış tabanlıkların kullanımı da önerilmektedir (232,233). Diyabetli nöropatik plantar topuk ülseri olanlarda ve ülserasyonu ayak plantarında olmayan olgularda ise ülserin tipi ve konumu göz önünde bulundurularak uygun yükten kurtarma uygulamalarının seçilmesi gerekmektedir (234).
Soru 2: İnfeksiyonlu Bir Yaranın Yükten Kurtarılması için Uygulanabilecek Yöntemler Nelerdir?
Diyabetik hastada ön veya orta ayak ülser varlığında, ülserin iyileşmesini desteklemek amacıyla önerilen ilk seçenek, çıkarılabilir olmayan, diz hizasında sonlanan ve ayak-ortez uyumu iyi olan yükten kurtarma uygulamalarıdır. Bu seçenek için uygulamadaki altın standart geleneksel tam temaslı alçı uygulamasıdır (234). Bu uygulama ile ayak önüne binen yükün %30’u doğrudan alt bacak bölgesindeki alçı yapıya transfer edilir; metatars başlarında yüklenen alan, parmaklar etrafına sarılan sünger ile korunur ve topukta taşınan yük artar (235). Ancak tam temaslı alçılar infekte olgular için uygun olmayıp özel olarak ve tam temaslı alçı prensiplerine göre tasarlanmış çıkarılabilir botlar kullanılabilir.
Hastaların bu ortezleri her zaman kullanması yönünde teşvik edilmesi gerekmektedir. Tam temaslı alçıya alternatif olarak, yükten kaldırma ortezlerinin kullanılacağı durumlarda, yara iyileşme hızı ve oranı, plantar basınç dağılımı, ambulatuvar durum, hastanın orteze uyumu, olası yan etkileri, hasta temelli sonuç ölçümleri ve maliyet etkinliği göz önünde bulundurulmalıdır (236). Çünkü yara iyileşme hızı ve süresi, aktiviteye dönüş hızı, çıkarılamayan alçı uygulanan olgulardaki yükten kurtarma amacıyla kullanılan ortezlere göre daha iyi bulunmuştur (237-239).
Diyabetik ön ayak veya orta ayak ülseri olan bir hastada, çıkarılamayan ve diz hizasında olan yükten kurtarma uygulaması kontrendike ise veya tolere edilemiyorsa, eklemlerin korunmasını ve iyileşmesini desteklemek amacıyla, çıkarılabilir ancak bu kez ayak bileği hizasında ve ayak-ortez uyumu iyi olan yükten kurtarma ortezi ikinci seçenek olarak düşük kanıt ve güçlü öneri gücü ile önerilmektedir; hasta her zaman ortezi takmaya teşvik edilmelidir (234,236). Gereklilik durumunda endike olan bu ortezlerin yara iyileşmesinde etkili olduğu ancak iyileştirici etkisinin yetersiz olduğu gösterilmiştir (240,231).
Yükten kurtarma uygulamalarının kontrendike olduğu durumlarda, ülserin iyileşmesini hızlandırmak amaçlanıyorsa, üçüncü seçenek olarak hastaların geleneksel veya standart terapötik ayakkabıları kullanmaları orta kanıt ve güçlü öneri düzeyi ile önerilmektedir. Hastaya, ülserasyona ve koşullara bağlı olarak, uygun şekilde tasarlanmış geleneksel veya standart terapötik ayakkabılarla birlikte köpük tabanlık önerilmesi dördüncü seçenek olarak düşük kanıt düzeyi ve zayıf öneri gücü ile uygulanabilecek bir yöntemdir (232,234). Özel tabanlıklı terapötik ayakkabı kullanımı, tam temaslı alçı uygulamalarıyla karşılaştırıldığında; alçı uygulanan olgularda yara iyileşmelerinin daha iyi olduğu bildirilmiştir (242). Tabanlıklar, potansiyel destrüktif mekanik güçleri azaltır veya ortadan kaldırır; ayak ile ayakkabı arasındaki lokal basınçları azaltır. Ancak tabanlıkların; mutlaka risk haritası belirlenerek hazırlanması, birinin ısıtılınca ayağa göre şekil alan köpük malzeme olmak üzere en az farklı iki dansiteden katlı yapıda üretilmiş olması, 6-12 ayda bir yenilenmesi gerekmektedir (243). Giyilen terapötik ayakkabıların ya da tabanlıkların üretiminde kullanılan materyalin seçimi de önemlidir. Yapılan çalışmalarda, içinde poliüretan (EVA), mikrohücreli lastik (“microcellular rubber”- MCR) ve şekillendirilmiş materyallerin kullanıldığı ayakkabıların, terapötik olmayan ayakkabıya göre plantar basıncı azaltmada daha iyi olduğu; tabanlık üretim materyalleri içerisinde de basıncı azaltmada en etkili materyalin poliüretan olduğu, yün keçe, lateks gibi materyallerin hem basıncın azaltılmasında yeterli etki sağlamadığı ve çabuk deforme olduğu gösterilmiştir (244,245). İnfeksiyonlu ve iskemik hastalarda ön ayak bölgesinden basıncın kaldırılması için metatarsal ped kullanımı önerilebilir. Poliüretan köpükten yapılan metatarsal pedin, basıncın azalmasında optimum rol oynaması için, proksimal metatarsal başlarının altına uygulanması gerekmektedir (246).
Diyabetik hastada topuk ülseri varlığında, ülserin iyileşmesini desteklemek amacıyla diz hizasında sonlanan, topuk üzerindeki plantar basıncı etkili bir şekilde azaltan ve hasta tarafından tolere edilen yükten kurtarma ortezleri düşük kanıt düzeyi ve zayıf öneri gücü ile önerilebilmektedir. Bunlara örnek olarak “toad anti-gravity foot brace” (TAG) verilebilir (247). Diyabetli ve plantar olmayan ayak ülseri olan kişilerde ise ülser iyileşmesini desteklemek amacıyla, ülserasyonun özellikleri ve konumu dikkate alınarak, çıkarılabilir ve ayak bileği hizasında yükten kurtarma ortezleri, ayakkabı modifikasyonları, ayak parmak silikonları, ayak ortezleri kullanımı düşük kanıt düzeyi ancak güçlü öneri düzeyi ile önerilmektedir. Burada ortezlerin hastaya özel tasarlanmış olması ve kullanımının, etkilerinin takip edilmesi önemlidir (248).
Soru 3: Ampütasyon Sonrası Rehabilitasyon Nasıl Olmalıdır?
Ampütasyonun nedeni rehabilitasyon sürecini etkileyen önemli bir faktördür. Diyabete bağlı ampütasyon cerrahisi planlı bir süreç olduğu için hastanın pre-operatif dönemdeki değerlendirmesine ve durumuna göre erken protez uygulaması planlanabilir.
Hastanede geçirilen erken post-operatif dönemde amputenin psikolojik olarak etkilenmesi dikkate alınmalıdır. Post-operatif dönemde fizyoterapi ve rehabilitasyonun amacı; yara iyileşmesinin sağlanması, ağrı kontrolü, ödemin önlenmesi, limitasyon ve kontraktürlerin önlenmesi, genel mobilitenin devam ettirilmesi, denge ve transferlerin geliştirilmesi, protezsiz yürüme eğitimi verilmesi ve günlük yaşam aktivitelerini bağımsız yapabilmesidir. Hastanın bu dönemdeki bilgilendirilmesi kapsamında; güdük bakımı, egzersiz ve mobilizasyonun önemi, yapılacak protez uygulaması detaylı şekilde anlatılmalıdır; güdükte ağrı, insizyon yerinde infeksiyon, sızıntı, ödem, fantom ağrısı, duyusal kayıplar, vasküler yetmezlik gibi güdüğe ilişkin komplikasyonlar görülebilmektedir. Hasta pre-prostetik dönemde; güdüğün durumu, insizyon yeri, kanama, infeksiyon, cilt rengi, nabızlar, ısı, eklem hareket açıklığı ve limitasyonlar, duyusal durum, yatak içi mobilite, denge, koordinasyon ve transfer aktiviteleri açısından potansiyel olarak değerlendirilmelidir (249).
Pre-prostetik dönemde pozisyonlama önem kazanmaktadır. Transtibial amputelerde diz ekleminde fleksiyon kontraktürü, transfemoral amputelerde ise kalça ekleminde fleksiyon-abduksiyon- eksternal rotasyon hareketine doğru gidiş olur. Bu nedenle, diz altı amputelerde diz eklemi ekstansiyonda olacak şekilde pozisyonlanmalı, sırtüstü yatış pozisyonunda dizin bükülmesi önlenmeli ve yatak içinde kuadriceps kası için kuvvetlendirme egzersizi verilmelidir. Diz üstü amputelerde de gün boyu üç kez 30’ar dakika yüzüstü yatmalı, sırtüstü pozisyonda güdük diğer ekstremiteye paralel olacak şekilde desteklenmeli, güdük altına yastık konulmamalı, tekerlekli sandalyede uzun süre oturma engellenmeli, kalça eklemi ekstansor ve adduktor kaslarına kuvvetlendirme egzersizleri verilmelidir. Kısalma eğilimi olan kaslar gerilmelidir. Bu dönemde, dikişlerin alınmasının ardından, güdük şekillenmesi, ödemin azaltılması ve dolaşımın artırılması amacıyla elastik bandaj uygulamaları, erken protezler ya da alçı, plastik ve pnömatik materyallerden yapılan geçici protezler kullanılır. Diyabetik amputelerde, duyusal uyarı kaybı, en önemli problemlerden biridir. Koruyucu duyu kaybı protezin fonksiyonel kullanımını ve rehabilitasyon sürecini olumsuz etkiler. Bu dönemde, hastanın duyusal kayıpları hem güdük açısından hem de sağlam ekstremite açısından objektif testlerle belirlenmeli, protez uygulaması öncesi dokular korunmalıdır (250). Hastaya ambulasyon ve transfer aktiviteleri öğretilmeli, ambulasyonda destek için kullanılacak üst ekstremite segmentleri kuvvetlendirilmelidir. Bu dönemde kullanılacak protez seçimi de belirlenmelidir.
Prostetik dönemde; protez ölçüsü, provalar ve protez ile mobilite çalışmaları yapılır. Bu süreçte, hastanın yaşı, ampütasyon seviyesi, beklenen mobilite düzeyi, güdük şekillenmesi, insizyon yerinin durumu, hastanın uyumu göz önünde bulundurulmalıdır. Protez seçiminde hastanın duyusal kayıpları hesaba katılarak sert soket içi yumuşak kaplamalar tercih edilmelidir. Protezin süspansiyonu için tercih edilen yöntem de diyabetik hasta için uygun olmalıdır. Bu dönem, yoğun egzersiz programı içermelidir. Egzersizlerden oluşan fizyoterapi ve rehabilitasyon programının amacı, eklem hareketini devam ettirmek, kontraktürleri önlemek, güdüğün kan akışını artırmak, güdüğün şekillenmesini sağlamak, agonist-antagonist kas kuvvet dengesini sağlamak, kas atrofilerini önlemek, hastanın motivasyonunu artırmak, protezsiz yürümeyi öğretmek, denge ve transfer aktivitelerini geliştirmek, kardiyo-respiratuvar enduransı korumak, enerji tüketimini azaltmak ve protezle normale yakın yürüme paterni geliştirmektir (251).
Diyabetik amputeler, protez uygulaması sonrasında post-prostetik dönemde de düzenli aralıklarla takip edilerek vasküler ve duyusal durum açısından izlenmelidir. Gerektiğinde protez modifikasyonları yapılmalı, rehabilitasyon yaklaşımları güncellenmelidir.
DİĞER TEDAVİLER
Soru 1: Hiperbarik Oksijen Tedavisi Nedir? Nasıl Etki Eder?
Diyabetik ayak lezyonlarında yalnızca makro ve mikrovasküler sorunlara bağlı olarak değil, aynı zamanda infeksiyon ve ödeme bağlı olarak da doku hipoksisi bulunur. Doku hipoksisi, yara iyileşme süreçlerini durdurur; yara infeksiyonunu ağırlaştırır ve dokuların nekroza ve gangrene gitmesine neden olur. Diyabetik ayak infeksiyonlarının tedavisinde hiperbarik oksijen (HBO)’in fiziksel ve fizyolojik etkilerinden yararlanılabilir. Söz konusu tedavi, uygun şartların sağlandığı bir odada hastanın basınç altında %100 oksijen soluması esasına dayanır. Yüksek basınç altında solunan oksijenin plazmada çözünmesiyle dokulara normalin 20 katına kadar daha fazla oksijen taşınır; ortamda basıncın artması oksijenin difüzyon mesafesini 2-3 kat artırır. Dokulardaki HBO’nun antihipoksik etkisinin yanı sıra periferik vazokonstriksiyon yoluyla antiödem etkisi de gözlenir. Doku hipoksisine bağlı olarak yara iyileşmesinin bozulması, HBO’nun sağladığı oksijen parsiyel basıncıyla restore edilir, hücresel enerji metabolizması düzelir ve kolajen sentezi ve anjiyogenez artar. Anaerop infeksiyon etkenleri, artan oksijen basıncından doğrudan etkilenir; oksijenle öldürme mekanizması ve bazı antibiyotiklerin işlevi için de dokularda belli bir oksijen basıncına gereksinim vardır.
Soru 2: Diyabetik Ayak İnfeksiyonlarında Hiperbarik Oksijen Neden Kullanılır?
Diyabetik ayak infeksiyonlarında HBO’nun yardımcı bir tedavi olarak kullanılmasının sağladığı yararları vurgulayan randomize kontrollü çalışmalar bulunmaktadır. Söz konusu çalışmalarda, HBO’nun DAİ’lerde iyileşme oranlarını artırdığı (252-258), iyileşme süresini kısalttığı (253,259) ve ampütasyon oranlarını düşürmekte olduğu (5,9,10) bildirilmiş olmakla birlikte yakın zamanda HBO’nun diyabetik ayak yaralarını iyileştirmekte etkisiz olduğunu ve ampütasyon oranlarını değiştirmediğini bildiren iki randomize kontrollü çalışma da yayımlanmıştır (262,263). Ancak bu çalışmalar tasarım, değerlendirme yöntemleri ve hasta seçimi açısından yaygın bir şekilde eleştirilmiştir (264-271). Bu konuda yapılan sistematik derleme ve meta-analizlerde, HBO’nun iskemik ve/veya iskemik olmayan DA yaralarında iyileşmeyi artırdığı ve/veya ampütasyon oranlarını azalttığı ortaya konulmakla birlikte çalışmaların sayıca yetersizliğine, çalışma tasarımlarındaki sorunlara, HBO tedavisi olanaklarının kısıtlılığına ve maliyetinin yüksek olduğuna da çeşitli yayınlarda değinilmektedir (272-280). Bununla birlikte ülkemizde HBO olanakları, başka ülkelerdekilerle karşılaştırılamayacak kadar çok sayıda ve yaygın durumdadır; maliyeti düşüktür ve sosyal güvenlik sistemi tarafından karşılanmaktadır.
Soru 3: Diyabetik Ayak Yarasında Hiperbarik Oksijen Nasıl Kullanılır?
Diyabetik ayak yarası indikasyonunda HBO tedavisi 2-3 ATA (“atmosphere absolute”)’lık basınçlarda günde bir kez toplam iki saatlik bir seans boyunca uygulanır. İlk değerlendirme 30. seansta yapılır ve yarar görülmesi halinde 30 seans daha uygulanır. Ağır hipoksi ve infeksiyon koşullarında günde birden fazla seans uygulanabilir. Hiperbarik oksijen tedavisi, DAİ’lerde yardımcı tedavi yöntemi olarak kullanılır. İskemi, infeksiyon, ödem gibi doku hipoksisine yol açan patolojilerde bu patolojilerin ana tedavisi olan revaskülarizasyon ve antibiyoterapiye eklenecek olan HBO tedavisi yararlı olur. Diğer cerrahi ve tıbbi tedavilerle birlikte uygulanmasına bir engel yoktur. Bununla birlikte aynı ortama alınan hastalarda çapraz infeksiyon riski göz önünde bulundurulmalıdır.
Soru 4: Negatif Basınçlı Yara Kapama Tedavisi Nedir? Nasıl Etki Eder?
Negatif basınçlı yara kapama uygulaması; akut ve kronik yaralarda iyileşmeyi hızlandırmak amacıyla yara üzerine kontrollü ve lokalize negatif basınç uygulanan ve invaziv olmayan bir yöntemdir. Bu konuda; ilk çalışmalar Louis Argenta ve Michael Morykwas tarafından Amerika’da 1989’da başlatılmış ve Amerika’da 1995 yılında 300 yarada kullanılmıştır. Bu olgularda granülasyon dokusu oluşma süresinin kısaldığı, yara ebatlarında belirgin küçülme olduğu gösterilmiş ve çalışma sonuçlarının daha iyi değerlendirilmesi için kapsamlı araştırmaların gerekliliği vurgulanmıştır (281).
Negatif basınçlı yara kapama sistemlerinin dört temel etkisi; makrodeformasyon, mikrodeformasyon, yaranın drenajı (yara sıvısının uzaklaştırılması) ve yara çevresinin kontrolüdür. Uygulama ile yara alanında ekstrasellüler sıvı azalır, lenfatik drenaj artar, kapillerler genişler ve kan akımı artar. Emilen sıvı ile birlikte toksinler, bakteriler ve eksuda uzaklaşır. Negatif basınçla; hücresel deformasyon, proliferasyon, migrasyon ve diferansiyasyonda artış gözlenir, iyileşme hızlanır ve hücrelerde eriyebilen mitojenlere karşı hassasiyet artar. Damarlanma; mekanik stimulasyon (mikrodeformasyon), anjiyogenik faktörlerin uzaklaştırılması, proanjiyogenik faktörlerin artışı, kan damarlarında dilatasyon, hipoksi ve ardından vasküler endotelyal “growth” faktör salgılanması ile artar. Bu hücrelerde eriyebilen mitojenlere karşı hassasiyet de artar. Yara yatağındaki fizyolojik ve kimyasal değişiklikler; ödemi azaltmakta, eksudayı uzaklaştırmakta, nemli ortamı korumakta, yara kontraksiyonunu sağlanmakta, yarada küçülmeyi sağlamakta, anjiyogenezi uyarmakta, kanlanmayı artırmakta, granülasyon dokusunun gelişimini artırmakta ve yara iyileşmesini hızlandırmaktadır.
Soru 5: Diyabetik Ayak İnfeksiyonlarında Negatif Basınçlı Yara Tedavisi Neden Kullanılır?
Diyabetik ayak yaralarında postoperatif dönemde negatif basınçlı yara kapama (NBYK) tedavisi, ıslak pansumana göre daha etkili görünmekle birlikte, iyi planlanmış çalışmalara hala ihtiyaç vardır. Konvansiyonel metotlar ile kıyaslandığında NBYK tedavisi mental (p=0.0287) ve fiziksel (p=0.04) olarak daha etkili görülmektedir (282). Negatif basınçlı yara kapama sistemleri yara tedavisinde yaygın olarak kullanılmaktadır; bu yöntemle infekte dokunun uzaklaştırılması sağlanmakta, yara kenarları küçülmekte, kanlanma artmakta, iyileşme hızı artmakta, iyileşme süresi kısalmakta, ampütasyon oranları düşmektedir. Kullanım indikasyonları olarak; akut ve kronik yaralar, diyabetik ayak infeksiyonu, bası yaraları, travmatik yaralar, venöz ülserler, yanık yaraları, mesh greft ve flep uygulaması sayılabilir. Kontrindikasyonlar olarak da malign yaralar, yetersiz yara perfüzyonu (TcO2 <30), yarada vital yapıların varlığı (organ, kan damarları, vasküler greft), tedavi edilmemiş osteomyelit sayılabilir. Nekrotik doku ve eskar varlığında, aktif kanaması olan hastalarda, antikoagülan kullanımında, radyasyon alanlarında ve sütüre damar alanlarında özen gösterilerek kullanılabilir (283-285). Bu uygulama ile yara tabanında yeterince sağlıklı granülasyon dokusu elde edildiğinde, klasik pansuman yöntemine geri dönülebilir ve deri grefti ile kapama ya da flep (cerrahi girişimi) ile kapama yapılabilir.
Soru 6: Diyabetik Ayak İnfeksiyonlarında Negatif Basınçlı Yara Tedavisi Nasıl Kullanılır?
Sistem; yara yatağını doldurmak için ve basıncın yara üzerinde etkin olarak dağıtılabilmesini sağlamak için poliüretan veya polivinil alkolden oluşan süngerler, yarayı kapamak için yapışkanlı yarı geçirgen kapamalar, yara ile cihaz bağlantısını sağlayan ve basıncı düzenleyen bir düzenek ile toplayıcı kap ve negatif basınç oluşturan bir cihazdan oluşmaktadır. Uygulama için yara yatağına uygun boyutta süngerler kesilerek yerleştirilir. Yara alanları yapışkanlı yarı geçirgen drape ile kapatılır. Kapama üzerinden delik açılarak “therapeutic regulated accurate care” (T.R.A.C.) pad yerleştirilerek cihaz ile yaranın bağlantısı sağlanır. Basınç hastaya, yaranın boyutuna, derinliğine, klinik durumuna göre kademeli olarak artırılarak (50-150 mmHg basınç) devamlı veya aralıklı olmak üzere uygulanır. Yaranın durumu, hastanın kliniği ve laboratuvar parametrelerine göre pansumanlar 48-72 saatte bir değiştirilir.
Sonuç olarak; NBYK klasik yöntemleri terk etmek anlamına gelmez, klasik yöntemlere ilave ve yardımcı bir yöntemdir ve iyileşme sürecinde katkı sağlanması için doğru indikasyonla kullanılabilir.
Soru 7: Ozon Uygulamasının Diyabetik Ayak Yaralarının Tedavisindeki Yeri Nedir?
Ozon üç oksijen atomu içeren siklik yapıda bir gazdır. Antibakteriyel ve antioksidan etkinliği çok uzun zamandır bilinmektedir (286,287). Canlı organizmada bu etkisinin ortaya çıkması, dokuda vaskülarizasyon ve ortamdaki serbest radikal yüküne bağlıdır. Olgu sunumları ve hasta serileri dışında DA yaralarında standart tedaviyi destekleyici seçenek olarak kullanımı tartışmalıdır (288). Son yıllarda yapılan daha geniş hasta serilerinde bile uygulamalarda doz, süre ve etkinlik açısından ozonun topikal veya sistemik uygulamalarında iyileşmeye katkısı bulunmamıştır (289). Diyabeti olan hastalarda ozon uygulaması gibi alternatif tedavi yaklaşımlarının standart tedaviyi geciktirebileceği veya engelleyebileceği dikkate alınmalıdır (288).
Soru 8: Büyüme Faktörlerinin Diyabetik Ayak Yaralarının Tedavisindeki Yeri Nedir?
Diayebetik ayakta infeksiyon ve/veya inflamasyon kontrol altına alındığında granülasyonu ve epitelizasyonu hızlandırmak hızla kapanmayı sağlar. Patogenezinde dokuda büyüme faktörlerinin salınımı azalır ve dokudaki proteinaz aktivitesi özellikle epidermal büyüme faktörlerinin (“epidermal growth factors”- EGFs) parçalanmasına sebep olur (290). Sahada yaygın uygulama alanı bulmaya başlayan rekombinant EGF’lerin topikal (jel) ve intralezyoner (enjektable) formları ülkemizde de mevcuttur. Randomize kontrollü çalışmaların meta-analizlerine ve özellikle uzak doğu kökenli rehberlere göre gerek topikal gerekse intralezyoner EGF’lerin DA’da iyileşmeyi desteklediği, özellikle intralezyoner formunun iskemik DA’da ampütasyonu önlediği gösterilmiştir; EGF’lerin DA’da uygulanması yüksek kanıt düzeyi ile önerilmektedir (291,292). Epidermal büyüme faktörlerinin uygulanması sonrasında ilk 45 dakika içerisinde fibroblast benzeri hücre membranında genişleme, kollajen matriks ve fiberde toplanma meydana gelir; 24. saatte ise ekstrasellüler matriks sentezi tamamlanır. Dakikalar içinde başlayan ve EGF reseptörü üzerinden devam eden etki, diğer yara bakım uygulamaları ile kombinasyon yapılabilme kolaylığı sağlar (293). Ülkemizde yapılan klinik çalışmalarda; topikal ve intralezyoner EGF uygulamalarının yara iyileşmesini olumlu etkilediği, tam kapanma, ampütasyonu önleme veya geciktirmede, ekstremiteyi tehdit eden DA’larda tedavi seçeneklerinden biri olarak değerlendirilmesi gerektiği sonucuna varılmıştır (294,295). Hem ülkemizdeki hem de dünyadaki çalışmaların geneline bakıldığında infeksiyonun kontrol altına alındığı, aktif
osteomyeliti olmayan hastalarda Meggitt-Wagner sınıflaması derece 1-3 arasında topikal EGF, derece 3-4’te de intralezyoner EGF uygulamaları standart tedavilere ek olarak yer alabilir.
Soru 9: Kurtçuk Uygulamasının Diyabetik Ayak Yaralarının Tedavisinde Yeri Nedir?
DA yaralarında debridman amacıyla Lucilia sericata sineğinin steril olarak üretilmiş kurtçukları kullanılmaktadır. Kurtçukların kronik yara tedavisinde nekrotik doku debridmanını hızlandırdığı, iyileşme hızını artırdığı, ampütasyon oranını azalttığı ve antibiyotiksiz gün sayısını artırdığı gösterilmiştir. Söz konusu çalışmalara bakıldığında, DA’larda bir debridman yöntemi olarak uygulandığı görülmektedir (296). Öncelikle bu uygulamayı hasta başı yapabilmek için özel bir eğitimden geçmiş olmanın yanında, sadece tıbbi kontrindikasyonlar nedeniyle keskin debridman uygulanamayan hastalarda özel şartlarda uygulanması, ağrı ve kanama riskinin yanında infeksiyon riskinin de olduğunun bilinerek yakın takip uyarısı yer almaktadır (297). Kurtçuk uygulaması DA yaralarında bilimsel ve etkin bir uygulama olmakla birlikte rutin olarak kullanılması için güçlü kanıtları içeren daha fazla sayıda çalışma yapılması gereklidir.
KORUNMA VE KONTROL
Soru 1: Diyabeti Olan Bireylerde Düzenli Ayak Muayenesi ve İncelemesi Nasıl Yapılmalıdır?
Yüksek riskli ayak sorunlarını tanımlamak ve saptamak için diyabeti olan hastalar muayeneye her geldiğinde ayakları, çorapları ve ayakkabıları çıkartılarak kontrol edilmelidir; ayrıca en az yılda bir kez kapsamlı olarak özel ayak muayenesi yapılmalıdır. Ayağın tam olarak değerlendirilebilmesi için vasküler duruma genel olarak bakılmalı ve deriyle kas, iskelet sistemi ayrıntılı olarak muayene edilmelidir. Bu muayene sırasında koruyucu duyu, ayağın yapısı ve biyomekanikleri, damar yapısı ve deri bütünlüğü değerlendirilmelidir. Bir veya daha fazla yüksek riskli durum saptanmış olan hastalar, ek risk faktörlerinin gelişimini kontrol etmek için daha sık muayene edilmeli ve değerlendirilmelidir (Tablo 8). Nöropati gelişen hastaların ayakları her kontrolde mutlaka konunun uzmanı bir sağlık çalışanı tarafından görsel olarak incelenmelidir (226,298-302).
Düşük riskli ayaklarda nörolojik durum değerlendirilmesi yapılırken Semmes-Weistein 5.07 (10 gr’lık) mono filaman kullanılmaktadır (303). Periferik arter hastalığı için ilk tarama yapılırken “claudicatio intermittens” (kesik topallama) öyküsü sorgulanmalı ve ayak arter nabızları değerlendirilmelidir. Deri incelenirken bütünlüğünün değerlendirilmesine önem verilmelidir; özellikle ayak parmak araları ve metatars başları üzerindeki deri daha dikkatli incelenmelidir. Kemik deformiteleri, eklemlerde hareket kısıtlılığı, yürüme bozuklukları ve denge sorunları, muayene sırasında mutlaka değerlendirilmesi gereken noktalardır (302-306).
Soru 2: Diyabeti Olan Bireylerde Düzenli Ayak Muayenesi Bileşenleri Neleri İçermelidir?
Diyabeti olan bireyde düzenli olarak yapılması gereken ayak muayenesinin bileşenleri Tablo 9’da sunulmuştur.
Soru 3: Diyabeti Olan Bireylerde Yıllık Ayak Muayenesi, Risk Değerlendirmesi ve İzlem Nasıl Yapılmalıdır?
Diyabeti olan tüm hastalarda yara ve ampütasyon açısından predispozan faktörlerin (nöropati, vasküler hastalık ve deformiteler) varlığını değerlendirmek için en az yılda bir kez kapsamlı ayak muayenesi yapılmalıdır. Tip 1 diyabetli hastalarda tanıdan beş yıl sonra başlamak üzere, tip 2 diyabetli hastalarda ise tanıdan itibaren nöropati muayenesi yapılmalı ve tarama yılda bir tekrarlanmalıdır (306). On yılı aşkın süredir diyabeti olan hastalarda yara gelişmesi ya da ampütasyon riski artmaktadır (303). Muayenede risk faktörleri saptanan hastalar 1-6 ay gibi daha sık aralarla izlenmelidir (226,302).
Diyabeti olan hastalarda etkin koruyucu ayak bakımı yapabilmek için riskin belirlenmesi gerekir. Diyabetli hastalarda ayak sorunlarına yaklaşım algoritması Şekil 4’te gösterilmiştir (306).
Soru 4: Ayak Bakımı Yönetiminde Uzmanlık Alanları ve Yapılanma Nasıl Olmalıdır?
Tablo 11. Aile Hekimliği Uygulamasında Rutin Diyabet İzlemlerinde Önerilen Diyabetik Ayak Muayenesi Kontrol Listesi (226, 284,302-307)
Koruyucu hekimlik uygulamaları yolu ile yara gelişiminin önlenmesi, diyabetik ayak yaklaşımının merkezinde yer almalıdır. Bu doğrultuda hasta, hasta yakınları ve tıbbi ekibin düzenli olarak eğitimi gereklidir. Yara gelişmiş bir olguda ise hedefler ülserin iyileştirilmesi, hastanın mobilize olabilmesi, yaşam kalitesinin artırılması ve ampütasyonların mümkün olduğunca azaltılmasıdır. Bu amaçlara ulaşılabilmesi için hastanın multidisipliner bir anlayış içinde yakından takip ve tedavisi şarttır. Tablo 10’da ayak bakım yönetiminde bulunması önerilen uzmanlık alanları listelenmiştir. Bu uzmanlık alanlarının hepsi her yerde bulunamasa da ekiplerin oluşturulması için çaba harcanması gereklidir (305,306).
Soru 5: Diyabeti Olan Bireylerin Koruyucu Sağlık Hizmeti (Birinci Basamak) Kapsamındaki Ayak Muayenesi Sonrasında Sevk İndikasyonları Nelerdir?
Aile hekimliğine başvuran her diyabetli bireyin diyabetik ayak sorunlarının erken fark edilmesi amacıyla ayak muayenesinin rutin olarak yapılması gerekmektedir. Aile hekimlerinin ayak değerlendirmesi yaparken Tablo 11’de yer alan başlıkları dikkate alması önerilmektedir.
Birinci basamakta izlenen bir hastanın hangi koşullarda, ne zaman, nereye sevk edileceği önemlidir. 2015 NICE Kılavuzu’ndan uyarlanmış sevk indikasyonları Tablo 12’de sunulmuştur (284).
Soru 6: Diyabeti Olan Birey ve Ailesinin Eğitimi Neleri İçermelidir?
Diyabetik ayak sorunları diyabetin eğitim ile önlenebilir komplikasyonlarıdır. Diyabeti olan birey ve yakınlarına hekim, hemşire ya da diyabet eğitmeni tarafından özel bir ayak bakım eğitimi verilmeli ve periyodik aralıklarla bu eğitim tekrarlanmalıdır. Ayak bakımı eğitimi bireysel ve/veya ailesiyle birlikte yapılmalıdır; mümkünse her görüşmede bireyin bilgisi ve ayak bakımı uygulama becerisi kontrol edilmelidir. Böylece diyabeti olan bireylerin ayaklarını muayene etmek için gerekli bilgiye sahip olup olmadıkları, kendi kararlarını uygulamak için kaynağa ulaşıp ulaşamadıkları, uyguladıkları bakımın etkinliğini değerlendirmek için yeterli deneyimlerinin olup olmadığı anlaşılmış olur (306-312). Eğitim verilen hastaların öğrendikleri bilgileri günlük yaşamlarına entegre etmeleri ve yaşamlarının her aşamasında uygulamaları gerekmektedir. Diyabeti olan bireylere ve yakınlarına öğretilmesi gerekenler Tablo 13’te gösterilmiştir (226,284,302,304,306,309-313).
Diyabetli bireyin, diyabet yönetimini başarılı bir şekilde gerçekleştirebilmesi yeterli bilgi, beceri ve olumlu tutumlara sahip olması ile ilgilidir. Diyabetli bireylere verilecek ayak eğitimde uyum ve davranış değişikliğinin sağlanması önemlidir. Yapılandırılmış ayak bakımı eğitimi; ayak ülserleri ve sonuçlarını, önleyici öz bakım davranışlarını, koruyucu ayakkabının giyilmesini, düzenli ayak kontrollerinin yapılmasını, uygun ayak hijyeninin sağlanmasını ve ayakta problem varsa zamanında profesyonel yardım istemesini içermelidir (284,306-311).
DİYABETİ OLAN BİREYLERDE NASIR PROBLEMİ NASIL VE NEDEN OLUŞUR?
Diyabetik ayaklarda gelişen deformitelere bağlı olarak değişen yük dağılımı, yineleyen biyomekanik travmalara neden olarak, dorsal ve plantarda özellikle de metatars yerleşimli kallus gelişimini tetikler. Kallus gelişimi, yumuşak doku hasarı ve infeksiyonu açısından ciddi bir risk oluşturur. Kallus altındaki yumuşak dokuda kanama ve iskemiye bağlı yaralar gelişebilme riski artar ve önlem alınmaması durumunda kronik ayak yarasına doğru ilerler. Periferik otonom nöropatiyle dokuda nem dengesinin bozulması, kuruyan ciltte çatlaklar oluşması ve deri bütünlüğünün bozulması mikroorganizma girişine yol açabilmektedir (38,313,314). Tüm bu yapısal ve biyomekanik değişimlerin yaşandığı süreçte doğru ayakkabıların tercih edilmemesi kemik yüzeylerinin çevresinde su toplamasına ve nasırlaşma problemine neden olabilmektedir.
Soru 1: Nasır Tedavisinde Uygulanan Metodlar Nelerdir?
Nasırların bulunduğu yere göre farklı tedavi metotları uygulanmalıdır (Tablo 14). Ülkemizde DA nasır debridmanında podologlar görev almaktadır. Nasır tedavisinde; debridman süresince oluşan toz ve partikülleri aspire edebilen, kuru aspirasyonlu anti-bakteriyel toz torbaları ve hepa filtreleri bulunan cihazlar tercih edilmelidir (315,316). Podolojik uygulamalarda kullanılan su püskürtme özellikli ıslak cihazlar fazladan debridman yapma riski nedeniyle diyabet hastalarında tercih edilmemelidir (317).
Soru 2: Diyabetik Ayakta Nasır Debridmanı Esnasında Kullanılan Freze Uçları Nelerdir?
Freze devirleri hastaların deri ve tırnak anatomisine göre ayarlanmaktadır (317). Freze uçlarıyla deride ve tırnakta çalışırken zig-zag çizmek ve fazladan bası uygulamak dokuya zarar verir. Frezeyi olması gerekenden daha uzun süre dokuya maruz bırakmak tırnakta ve deride yanmaya neden olabilir. Bistürinin kesme hareketine bağlı olarak jilet ve trapan-nasır ucu freze uygulamalarına kıyasla dokuda çok az bir karşı direnç söz konusudur. Kesi yüzeyi kontrolü önemlidir (Şekil 5) (318). Freze uçlarının seçiminde, aşındırma özelliğine dikkat ederek, dokuya en az zarar verecek ya da yakma ihtimali düşük olan gruptan freze ucu tercih edilmelidir (Şekil 6) (319). Bunlara örnek uçlar; çizgisiz elmas freze, kırmızı çizgili ya da seramik freze uçlarıdır.
Danışman Değerlendirmesi
Bağımsız dış danışman
Yazar Katkıları
Fikir/Kavram – A.K., N.S.; Tasarım – A.K., N.S.; Denetleme – A.K., N.S., Ö.A., F.A.A., B.E., M.C.O., S.S., A.Ş., D.Y.; Analiz ve/veya Yorum – TÜM YAZARLAR; Literatür Taraması – TÜM YAZARLAR; Makale Yazımı – TÜM YAZARLAR; Eleştirel İnceleme – A.K., N.S., Ö.A., F.A.A., B.E., M.C.O., S.S., A.Ş., D.Y.
Çıkar Çatışması
Yazarlar herhangi bir çıkar çatışması bildirmemiştir.
Finansal Destek
Yazarlar finansal destek beyan etmemiştir.
Referanslar
- About diabetes: Facts and figures [Internet]. Brussels: International Diabetes Federation. [erişim 24 Ekim 2023]. https://idf.org/about-diabetes/diabetes-facts-figures/
- Andrew JM, Boulton AJM, Armstrong DG, et al. Diagnosis and management of diabetic foot complications. ADA Clinical Compendia. 2018;2018(2). [CrossRef]
- Singh N, Armstrong DG, Lipsky BA. Preventing foot ulcers in patients with diabetes. JAMA. 2005;293(2):217-28. [CrossRef]
- Kim PJ, Steinberg JS. Complications of the diabetic foot. Endocrinol Metab Clin North Am. 2013;42(4):833-47. [CrossRef]
- Rodrigues BT, Vangaveti VN, Urkude R, Biros E, Malabu UH. Prevalence and risk factors of lower limb amputations in patients with diabetic foot ulcers: A systematic review and meta-analysis. Diabetes Metab Syndr. 2022;16(2):102397. [CrossRef]
- Bandarian F, Qorbani M, Nasli-Esfahani E, Sanjari M, Rambod C, Larijani B. Epidemiology of diabetes foot amputation and its risk factors in the Middle East Region: A systematic review and meta-analysis. Int J Low Extrem Wounds. 2022:15347346221109057. [CrossRef]
- Huijberts MS, Schaper NC, Schalkwijk CG. Advanced glycation end products and diabetic foot disease. Diabetes Metab Res Rev. 2008;24 Suppl 1:S19-24. [CrossRef]
- ElSayed NA, Aleppo G, Aroda VR, et al, on behalf of the American Diabetes Association. 12. Retinopathy, neuropathy, and foot care: Standards of care in diabetes-2023. Diabetes Care. 2023;46(Suppl 1):203-15. [CrossRef]
- Wukich DK, Schaper NC, Gooday C, Bal A, Bem R, Chhabra A, et al. Guidelines on the diagnosis and treatment of active Charcot neuro-osteoarthropathy in persons with diabetes mellitus (IWGDF 2023). Diabetes Metab Res Rev. 2023:e3646. [CrossRef]
- Forsythe RO, Apelqvist J, Boyko EJ, et al. Effectiveness of revascularisation of the ulcerated foot in patients with diabetes and peripheral artery disease: A systematic review. Diabetes Metab Res Rev. 2020;36 Suppl 1:e3279. [CrossRef]
- Mutluoglu M, Uzun G, Turhan V, Gorenek L, Ay H, Lipsky BA. How reliable are cultures of specimens from superficial swabs compared with those of deep tissue in patients with diabetic foot ulcers? J Diabetes Complications. 2012;26(3):225-9. [CrossRef]
- Ertugrul BM, Oncul O, Tulek N, et al. A prospective, multi-center study: factors related to the management of diabetic foot infections. Eur J Clin Microbiol Infect Dis. 2012;31(9):2345-52. [CrossRef]
- Turhan V, Mutluoglu M, Acar A, et a. Increasing incidence of Gram-negative organisms in bacterial agents isolated from diabetic foot ulcers. J Infect Dev Ctries. 2013;7(10):707-12. [CrossRef]
- Saltoglu N, Yemisen M, Ergonul O, et al; KLIMIK Turkish Society, Diabetic Foot Study Group. Predictors for limb loss among patient with diabetic foot infections: an observational retrospective multicentric study in Turkey. Clin Microbiol Infect. 2015;21(7):659-64. [CrossRef]
- Hatipoglu M, Mutluoglu M, Turhan V, et al. Causative pathogens and antibiotic resistance in diabetic foot infections: A prospective multi-center study. J Diabetes Complications. 2016;30(5):910-6. [CrossRef]
- Ertugrul BM, Lipsky BA, Ture M, Sakarya S. Risk factors for infection with Pseudomonas aeruginosa in diabetic foot infections. J Am Podiatr Med Assoc. 2017;107(6):483-9. [CrossRef]
- Öztürk BŞ, Ertuğrul MB, Çörekli E. [Bacterial agents in diabetic foot ınfections and their biofilm formation rates]. Türk Mikrobiyol Cem Derg. 2017;47(1):33-8. Turkish. [CrossRef]
- Saltoglu N, Ergonul O, Tulek N, et al; Turkish Society of Clinical Microbiology and Infectious Diseases, Diabetic Foot Infections Study Group. Influence of multidrug resistant organisms on the outcome of diabetic foot infection. Int J Infect Dis. 2018;70:10-4. [CrossRef]
- Vatan A, Saltoglu N, Yemisen M, et al; Study Group, Cerrahpasa Diabetic Foot. Association between biofilm and multi/extensive drug resistance in diabetic foot infection. Int J Clin Pract. 2018;72(3):e13060. [CrossRef]
- Demirdal T, Sen P. The significance of neutrophil-lymphocyte ratio, platelet-lymphocyte ratio and lymphocyte-monocyte ratio in predicting peripheral arterial disease, peripheral neuropathy, osteomyelitis and amputation in diabetic foot infection. Diabetes Res Clin Pract. 2018;144:118-25. [CrossRef]
- Saltoglu N, Surme S, Ezirmik E, et al; KLİMİK Society, Diabetic Foot Study Group. The Effects of antimicrobial resistance and the compatibility of initial antibiotic treatment on clinical outcomes in patients with diabetic foot infection. Int J Low Extrem Wounds. 2023;22(2):283-90. [CrossRef]
- Surme S, Saltoglu N, Kurt AF, et al; Cerrahpasa Medical Faculty Diabetic Foot Infections Study Group (DAİÇG). Changing bacterial etiology and antimicrobial resistance profiles as prognostic determinants of diabetic foot ınfections: A ten-year retrospective cohort study. Surg Infect (Larchmt). 2022;23(7):667-74. [CrossRef]
- Liu X, Ren Q, Zhai Y, Kong Y, Chen D, Chang B. Risk factors for multidrug-resistant organisms ınfection in diabetic foot ulcer. Infect Drug Resist. 2022;15:1627-35. [CrossRef]
- Yan X, Song JF, Zhang L, Li X. Analysis of risk factors for multidrug-resistant organisms in diabetic foot infection. BMC Endocr Disord. 2022;22(1):46. [CrossRef]
- Caruso P, Maiorino MI, Macera M, et al. Antibiotic resistance in diabetic foot infection: how it changed with COVID-19 pandemic in a tertiary care center. Diabetes Res Clin Pract. 2021;175:108797. [CrossRef]
- Xia W, He W, Luo T, Tang N. Risk factors for multidrug-resistant bacterial infections in patients with diabetic foot ulcers: a systematic review and meta-analysis. Ann Palliat Med. 2021;10(12):12618-30. [CrossRef]
- Ji X, Jin P, Chu Y, Feng S, Wang P. Clinical characteristics and risk factors of diabetic foot ulcer with multidrug-resistant organism infection. Int J Low Extrem Wounds. 2014;13(1):64-71. [CrossRef]
- Noor S, Borse AG, Ozair M, Raghav A, Parwez I, Ahmad J. Inflammatory markers as risk factors for infection with multidrug-resistant microbes in diabetic foot subjects. Foot (Edinb). 2017;32:44-8. [CrossRef]
- Zubair M, Malik A, Ahmad J. Clinico-microbiological study and antimicrobial drug resistance profile of diabetic foot infections in North India. Foot (Edinb). 2011;21(1):6-14. Erratum in: Foot (Edinb). 2011;21(4):209-10. [CrossRef]
- Zhang J, Chu Y, Wang P, et al. Clinical outcomes of multidrug resistant pseudomonas aeruginosa infection and the relationship with type III secretion system in patients with diabetic foot. Int J Low Extrem Wounds. 2014;13(3):205-10. [CrossRef]
- Lipsky BA. Diagnosing and treating diabetic foot infections. Klimik Derg. 2009;22(1):2-13.
- Argiana V, Kanellos PΤ, Makrilakis K, et al. The effect of consumption of low-glycemic-index and low-glycemic-load desserts on anthropometric parameters and inflammatory markers in patients with type 2 diabetes mellitus. Eur J Nutr. 2015;54(7):1173-80. [CrossRef]
- Stanaway S, Johnson D, Moulik P, Gill G. Methicillin-resistant Staphylococcus aureus (MRSA) isolation from diabetic foot ulcers correlates with nasal MRSA carriage. Diabetes Res Clin Pract. 2007;75(1):47-50. [CrossRef]
- Liu C, Bayer A, Cosgrove SE, et al. Clinical practice guidelines by the infectious diseases society of america for the treatment of methicillin-resistant Staphylococcus aureus infections in adults and children: executive summary. Clin Infect Dis. 2011;52(3):285-92. [CrossRef]
- Nakai H, Hagihara M, Kato H, et al. Prevalence and risk factors of infections caused by extended-spectrum β-lactamase (ESBL)-producing Enterobacteriaceae. J Infect Chemother. 2016;22(5):319-26. [CrossRef]
- Acar A, Saltoğlu N, Tülek N, et al. Impact of the COVID-19 pandemic on diabetic foot patients: A shift in the infectious agent profile towards non fermentative Gram-negative bacilli. J Am Podiatr Med Assoc. (Yayın aşamasında, 5 Ekim 2022 tarihinde kabul edilmiştir.)
- Pitocco D, Spanu T, Di Leo M, et al. Diabetic foot infections: a comprehensive overview. Eur Rev Med Pharmacol Sci. 2019;23(2 Suppl):26-37. [CrossRef]
- Saltoğlu N, Kılıçoğlu Ö, Baktıroğlu S, et al. Diyabetik ayak yarası ve infeksiyonunun tanısı, tedavisi ve önlenmesi: Ulusal uzlaşı raporu. Klimik Derg. 2015;28(Suppl. 1):2-34. [CrossRef]
- Monteiro-Soares M, Russell D, Boyko EJ, Jeffcoate W, Mills JL, Morbach S, Game F; International Working Group on the Diabetic Foot (IWGDF). Guidelines on the classification of diabetic foot ulcers (IWGDF 2019). Diabetes Metab Res Rev. 2020;36 Suppl 1:e3273. [CrossRef]
- Senneville É, Albalawi Z, van Asten SA, et al. IWGDF/IDSA Guidelines on the diagnosis and treatment of diabetes-related foot infections (IWGDF/IDSA 2023). Clin Infect Dis. 2023:ciad527. [CrossRef]
- Monteiro-Soares M, Hamilton EJ, Russell DA, et al. Guidelines on the classification of foot ulcers in people with diabetes (IWGDF 2023 update). Diabetes Metab Res Rev. 2023:e3648. [CrossRef]
- Malone M, Bowling FL, Gannass A, Jude EB, Boulton AJ. Deep wound cultures correlate well with bone biopsy culture in diabetic foot osteomyelitis. Diabetes Metab Res Rev. 2013;29(7):546-50. [CrossRef]
- Senneville É, Lipsky BA, Abbas ZG, et al. Diagnosis of infection in the foot in diabetes: a systematic review. Diabetes Metab Res Rev. 2020;36 Suppl 1:e3281. [CrossRef]
- Zhang WQ, Tang W, Hu SQ, et al. C-reactive protein and diabetic foot ulcer infections: A meta-analysis. J Tissue Viability. 2022;31(3):537-43. [CrossRef]
- Lipsky BA, Berendt AR, Cornia PB, et al; Infectious Diseases Society of America. 2012 Infectious Diseases Society of America clinical practice guideline for the diagnosis and treatment of diabetic foot infections. Clin Infect Dis. 2012;54(12):e132-73. [CrossRef]
- Rubitschung K, Sherwood A, Crisologo AP, et al. Pathophysiology and molecular imaging of diabetic foot infections. Int J Mol Sci. 2021;22(21):11552. [CrossRef]
- Dinh T, Snyder G, Veves A. Current techniques to detect foot infection in the diabetic patient. Int J Low Extrem Wounds. 2010;9(1):24-30. [CrossRef]
- Ertuğrul MB, Baktıroğlu S. Diyabetik ayak ve osteomiyeliti. Klimik Derg. 2005;18(1):8-13.
- Ertuğrul B, Uçkay I, Schöni M, Peter-Riesch B, Lipsky BA. Management of diabetic foot infections in the light of recent literature and new international guidelines. Expert Rev Anti Infect Ther. 2020;18(4):293-305. [CrossRef]
- Ertugrul BM, Savk O, Ozturk B, Cobanoglu M, Oncu S, Sakarya S. The diagnosis of diabetic foot osteomyelitis: examination findings and laboratory values. Med Sci Monit. 2009;15(6):CR307-12.
- Ertugrul BM, Savk O, Ozturk B, Cobanoglu M, Oncu S, Sakarya S. The diagnosis of diabetic foot osteomyelitis: examination findings and laboratory values. Med Sci Monit. 2009;15(6):CR307-12.
- Ertugrul MB, Baktiroglu S, Salman S, et al. The diagnosis of osteomyelitis of the foot in diabetes: microbiological examination vs. magnetic resonance imaging and labelled leucocyte scanning. Diabet Med. 2006;23(6):649-53. [CrossRef]
- Lipsky BA. Osteomyelitis of the foot in diabetic patients. Clin Infect Dis. 1997;25(6):1318-26. [CrossRef]
- Lipsky BA, Peters EJ, Senneville E, et al. Expert opinion on the management of infections in the diabetic foot. Diabetes Metab Res Rev. 2012;28 Suppl 1:163-78. [CrossRef]
- Newman LG, Waller J, Palestro CJ, et al. Unsuspected osteomyelitis in diabetic foot ulcers. Diagnosis and monitoring by leukocyte scanning with indium in 111 oxyquinoline. JAMA. 1991;266(9):1246-51. [CrossRef]
- Hartemann-Heurtier A, Senneville E. Diabetic foot osteomyelitis. Diabetes Metab. 2008;34(2):87-95. [CrossRef]
- Ertugrul BM, Lipsky BA, Savk O. Osteomyelitis or Charcot neuro-osteoarthropathy? Differentiating these disorders in diabetic patients with a foot problem. Diabet Foot Ankle. 2013;4. [CrossRef]
- Çildağ MB, Ertuğrul BM, Köseoğlu ÖF, Çildağ S, Armstrong DG. Angiographic assessment of atherosclerotic load at the lower extremity in patients with diabetic foot and charcot neuro-arthropathy. J Chin Med Assoc. 2018;81(6):565-70. [CrossRef]
- Çildağ MB, Ertuğrul MB, Köseoğlu ÖFK. Charcot neuroarthropathy and a new sign: “Soft Tissue Contamination Sign of Foot or Ankle” on Bolus Chase 3-dimensional magnetic resonance imaging. J Foot Ankle Surg. 2020;59(3):643-4. [CrossRef]
- Glaudemans AW, Uçkay I, Lipsky BA. Challenges in diagnosing infection in the diabetic foot. Diabet Med. 2015;32(6):748-59. [CrossRef]
- Jude EB, Selby PL, Mawer EB, Burgess J, Boulton AJM. Inflammatory and bone turnover markers in Charcot arthropathy and osteomyelitis of the feet in diabetic patients. Diabetologia 2002;45(suppl 2):A341-2.
- Ertugrul MB, Baktiroglu S, Salman S, et al. Pathogens isolated from deep soft tissue and bone in patients with diabetic foot infections. J Am Podiatr Med Assoc. 2008;98(4):290-5. [CrossRef]
- McDermott KM, Srinivas T, Abularrage CJ. Multidisciplinary approach to decreasing major amputation, improving outcomes, and mitigating disparities in diabetic foot and vascular disease. Semin Vasc Surg. 2023;36(1):114-21. [CrossRef]
- Mahmoudi M, Gould LJ. Opportunities and challenges of the management of chronic wounds: A multidisciplinary viewpoint. CWCMR. 2020;(7):27-36. [CrossRef]
- Türkiye Diyabet Önleme ve Kontrol Programı: Eylem Planı (2011-2014). T.C. Sağlık Bakanlığı, Temel Sağlık Hizmetleri Genel Müdürlüğü, Ankara. Yayın no: 816, 2011.
- Türkiye Diyabet Programı 2015-2020. T.C. Sağlık Bakanlığı, Türkiye Halk Sağlığı Kurumu, Ankara. Yayın no: 816, 2014.
- Genelge: Kronik Yara Bakım Hizmetleri, 2022/8 [Internet]. Ankara: T.C. Sağlık Bakanlığı, Sağlık Hizmetleri Genel Müdürlüğü. [erişim 24 Ekim 2023]. https://www.klimik.org.tr/wp-content/uploads/2022/12/Kronik-Yara-Bakim-Hizmetleri.pdf
- Schaper NC, van Netten JJ, Apelqvist J, Bus SA, Hinchliffe RJ, Lipsky BA; IWGDF Editorial Board. Practical Guidelines on the prevention and management of diabetic foot disease (IWGDF 2019 update). Diabetes Metab Res Rev. 2020;36 Suppl 1:e3266. [CrossRef]
- Peters EJG, Lipsky BA, Senneville E, Abbas ZG, Aragón-Sánchez J, Diggle M, et al. Interventions in the management of infection in the foot in diabetes: A systematic review Diab Metab Res Reviews. 2016;21(Suppl 1):145-53.
- Selva Olid A, Solà I, Barajas-Nava LA, Gianneo OD, Bonfill Cosp X, Lipsky BA. Systemic antibiotics for treating diabetic foot infections. Cochrane Database Syst Rev. 2015;2015(9):CD009061. [CrossRef]
- Hartemann-Heurtier A, Robert J, Jacqueminet S, et al. Diabetic foot ulcer and multidrug-resistant organisms: risk factors and impact. Diabet Med. 2004;21(7):710-5. [CrossRef]
- Kandemir O, Akbay E, Sahin E, Milcan A, Gen R. Risk factors for infection of the diabetic foot with multi-antibiotic resistant microorganisms. J Infect. 2007;54(5):439-45. [CrossRef]
- Paul Bouter K, Visseren FL, van Loenhout RM, Bartelink AK, Willem Erkelens D, Diepersloot RJ. Treatment of diabetic foot infection: an open randomised comparison of imipenem/cilastatin and piperacillin/clindamycin combination therapy. Int J Antimicrob Agents. 1996;7(2):143-7. [CrossRef]
- Clay PG, Graham MR, Lindsey CC, Lamp KC, Freeman C, Glaros A. Clinical efficacy, tolerability, and cost savings associated with the use of open-label metronidazole plus ceftriaxone once daily compared with ticarcillin/clavulanate every 6 hours as empiric treatment for diabetic lower-extremity infections in older males. Am J Geriatr Pharmacother. 2004;2(3):181-9. [CrossRef]
- Erstad BL, McIntyre KE. Prospective, randomized comparison of ampicillin/sulbactam and cefoxitin for diabetic foot infections. Vascular Surgery. 1997;31(4):419-26. [CrossRef]
- Giordano P, Song J, Pertel P, Herrington J, Kowalsky S. Sequential intravenous/oral moxifloxacin versus intravenous piperacillin-tazobactam followed by oral amoxicillin-clavulanate for the treatment of complicated skin and skin structure infection. Int J Antimicrob Agents. 2005;26(5):357-65. [CrossRef]
- Graham DR, Lucasti C, Malafaia O, et al. Ertapenem once daily versus piperacillin-tazobactam 4 times per day for treatment of complicated skin and skin-structure infections in adults: results of a prospective, randomized, double-blind multicenter study. Clin Infect Dis. 2002;34(11):1460-8. [CrossRef]
- Graham DR, Talan DA, Nichols RL, et al. Once-daily, high-dose levofloxacin versus ticarcillin-clavulanate alone or followed by amoxicillin-clavulanate for complicated skin and skin-structure infections: a randomized, open-label trial. Clin Infect Dis. 2002;35(4):381-9. [CrossRef]
- Grayson ML, Gibbons GW, Habershaw GM, et al. Use of ampicillin/sulbactam versus imipenem/cilastatin in the treatment of limb-threatening foot infections in diabetic patients. Clin Infect Dis. 1994;18(5):683-93. Erratum in: Clin Infect Dis. 1994;19(4):820. [CrossRef]
- Harkless L, Boghossian J, Pollak R, et al. An open-label, randomized study comparing efficacy and safety of intravenous piperacillin/tazobactam and ampicillin/sulbactam for infected diabetic foot ulcers. Surg Infect (Larchmt). 2005;6(1):27-40. [CrossRef]
- Lauf L, Ozsvár Z, Mitha I, et al. Phase 3 study comparing tigecycline and ertapenem in patients with diabetic foot infections with and without osteomyelitis. Diagn Microbiol Infect Dis. 2014;78(4):469-80. [CrossRef]
- Lipsky BA, Itani K, Norden C; Linezolid Diabetic Foot Infections Study Group. Treating foot infections in diabetic patients: a randomized, multicenter, open-label trial of linezolid versus ampicillin-sulbactam/amoxicillin-clavulanate. Clin Infect Dis. 2004;38(1):17-24. [CrossRef]
- Noel GJ, Bush K, Bagchi P, Ianus J, Strauss RS. A randomized, double-blind trial comparing ceftobiprole medocaril with vancomycin plus ceftazidime for the treatment of patients with complicated skin and skin-structure infections. Clin Infect Dis. 2008;46(5):647-55. [CrossRef]
- Gyssens IC, Dryden M, Kujath P, et al. A randomized trial of the efficacy and safety of sequential intravenous/oral moxifloxacin monotherapy versus intravenous piperacillin/tazobactam followed by oral amoxicillin/clavulanate for complicated skin and skin structure infections. J Antimicrob Chemother. 2011;66(11):2632-42. [CrossRef]
- Schaper NC, Dryden M, Kujath P, et al. Efficacy and safety of IV/PO moxifloxacin and IV piperacillin/tazobactam followed by PO amoxicillin/clavulanic acid in the treatment of diabetic foot infections: results of the RELIEF study. Infection. 2013;41(1):175-86. [CrossRef]
- Saltoglu N, Dalkiran A, Tetiker T, et al. Piperacillin/tazobactam versus imipenem/cilastatin for severe diabetic foot infections: a prospective, randomized clinical trial in a university hospital. Clin Microbiol Infect. 2010;16(8):1252-7. [CrossRef]
- Siami G, Christou N, Eiseman I, Tack KJ; Severe Skin and Soft Tissue Infections Study Group. Clinafloxacin versus piperacillin-tazobactam in treatment of patients with severe skin and soft tissue infections. Antimicrob Agents Chemother. 2001;45(2):525-31. [CrossRef]
- Lipsky BA, Giordano P, Choudhri S, Song J. Treating diabetic foot infections with sequential intravenous to oral moxifloxacin compared with piperacillin-tazobactam/amoxicillin-clavulanate. J Antimicrob Chemother. 2007;60(2):370-6. [CrossRef]
- Lipsky BA, Armstrong DG, Citron DM, Tice AD, Morgenstern DE, Abramson MA. Ertapenem versus piperacillin/tazobactam for diabetic foot infections (SIDESTEP): prospective, randomised, controlled, double-blinded, multicentre trial. Lancet. 2005;366(9498):1695-703. [CrossRef]
- Vick-Fragoso R, Hernández-Oliva G, Cruz-Alcázar J, et al; STIC Study Group. Efficacy and safety of sequential intravenous/oral moxifloxacin vs intravenous/oral amoxicillin/clavulanate for complicated skin and skin structure infections. Infection. 2009;37(5):407-17. [CrossRef]
- Tan JS, Wishnow RM, Talan DA, Duncanson FP, Norden CW; The Piperacillin/Tazobactam Skin and Skin Structure Study Group. Treatment of hospitalized patients with complicated skin and skin structure infections: double-blind, randomized, multicenter study of piperacillin-tazobactam versus ticarcillin-clavulanate. Antimicrob Agents Chemother. 1993;37(8):1580-6. [CrossRef]
- Eckmann C, Dryden M. Treatment of complicated skin and soft-tissue infections caused by resistant bacteria: value of linezolid, tigecycline, daptomycin and vancomycin. Eur J Med Res. 2010;15(12):554-63. [CrossRef]
- Arda B, Uysal S, Taşbakan M, et al. Use of tigecycline for diabetic foot infections. Wounds. 2017;29(11):297-305.
- Utlu Y, Başak O, Bozkurt-Kozan F, Ertuğrul MB. [Causative agents and factors associated with multidrug resistant pathogens in diabetic foot infections]. Klimik Derg. 2019;32(1):84-9. Turkish. [CrossRef]
- Lipsky BA, Uçkay İ. Treating diabetic foot osteomyelitis: A practical state-of-the-art update. Medicina (Kaunas). 2021;57(4):339. [CrossRef]
- Li HK, Rombach I, Zambellas R, et al; OVIVA Trial Collaborators. Oral versus intravenous antibiotics for bone and joint infection. N Engl J Med. 2019;380(5):425-36. [CrossRef]
- Gariani K, Lebowitz D, von Dach E, Kressmann B, Lipsky BA, Uçkay I. Remission in diabetic foot infections: Duration of antibiotic therapy and other possible associated factors. Diabetes Obes Metab. 2019;21(2):244-51. [CrossRef]
- Commons RJ, Charles J, Cheney J, Lynar SA, Malone M, Raby E; Australian Diabetes-related Foot Disease Guidelines & Pathways Project. Australian guideline on management of diabetes-related foot infection: part of the 2021 Australian evidence-based guidelines for diabetes-related foot disease. J Foot Ankle Res. 2022;15(1):47. [CrossRef]
- Gariani K, Pham TT, Kressmann B, et al. Three weeks versus six weeks of antibiotic therapy for diabetic foot osteomyelitis: A prospective, randomized, noninferiority pilot trial. Clin Infect Dis. 2021;73(7):e1539-45. [CrossRef]
- Senneville E, Joulie D, Blondiaux N, Robineau O. Surgical techniques for bone biopsy in diabetic foot infection, and association between results and treatment duration. J Bone Jt Infect. 2020;5(4):198-204. [CrossRef]
- Lázaro-Martínez JL, Aragón-Sánchez J, García-Morales E. Antibiotics versus conservative surgery for treating diabetic foot osteomyelitis: a randomized comparative trial. Diabetes Care. 2014;37(3):789-95. [CrossRef]
- Aragón-Sánchez J, Lipsky BA. Modern management of diabetic foot osteomyelitis. The when, how and why of conservative approaches. Expert Rev Anti Infect Ther. 2018;16(1):35-50. [CrossRef]
- Pham TT, Gariani K, Richard JC, et al. Moderate to severe soft tissue diabetic foot infections: A randomized, controlled, pilot trial of post-debridement antibiotic treatment for 10 versus 20 days. Ann Surg. 2022;276(2):233-8. [CrossRef]
- Crowther GS, Callaghan N, Bayliss M, Noel A, Morley R, Price B. Efficacy of topical vancomycin- and gentamicin-loaded calcium sulfate beads or systemic antibiotics in eradicating polymicrobial biofilms isolated from diabetic foot infections within an in vitro wound model. Antimicrob Agents Chemother. 2021;65(6):e02012-20. [CrossRef]
- Price BL, Morley R, Bowling FL, Lovering AM, Dobson CB. Susceptibility of monomicrobial or polymicrobial biofilms derived from infected diabetic foot ulcers to topical or systemic antibiotics in vitro. PLoS One. 2020;15(2):e0228704. [CrossRef]
- Lipsky BA, Kuss M, Edmonds M, Reyzelman A, Sigal F. Topical application of a gentamicin-collagen sponge combined with systemic antibiotic therapy for the treatment of diabetic foot infections of moderate severity: a randomized, controlled, multicenter clinical trial. J Am Podiatr Med Assoc. 2012;102(3):223-32. Erratum in: J Am Podiatr Med Assoc. 2012;102(4):323. [CrossRef]
- Li X, Huang W, Zheng X, et al. Synergistic in vitro effects of indocyanine green and ethylenediamine tetraacetate-mediated antimicrobial photodynamic therapy combined with antibiotics for resistant bacterial biofilms in diabetic foot infection. Photodiagnosis Photodyn Ther. 2019;25:300-8. [CrossRef]
- Brocco E, Curci V, Da Ros R, et al. Photodynamic topical antimicrobial therapy for infected diabetic foot ulcers in patients with diabetes: A case series. Int J Low Extrem Wounds. 2022;21(2):137-40. [CrossRef]
- Mannucci E, Genovese S, Monami M, et al. Photodynamic topical antimicrobial therapy for infected foot ulcers in patients with diabetes: a randomized, double-blind, placebo-controlled study–the D.A.N.T.E (Diabetic ulcer Antimicrobial New Topical treatment Evaluation) study. Acta Diabetol. 2014;51(3):435-40. [CrossRef]
- Morley S, Griffiths J, Philips G, et al. Phase IIa randomized, placebo-controlled study of antimicrobial photodynamic therapy in bacterially colonized, chronic leg ulcers and diabetic foot ulcers: a new approach to antimicrobial therapy. Br J Dermatol. 2013;168(3):617-24. [CrossRef]
- Tardivo JP, Adami F, Correa JA, Pinhal MA, Baptista MS. A clinical trial testing the efficacy of PDT in preventing amputation in diabetic patients. Photodiagnosis Photodyn Ther. 2014;11(3):342-50. [CrossRef]
- Ahmed M, Reffat SA, Hassan A, Eskander F. Platelet-rich plasma for the treatment of clean diabetic foot ulcers. Ann Vasc Surg. 2017;38:206-11. [CrossRef]
- Hossam EM, Alserr AHK, Antonopoulos CN, Zaki A, Eldaly W. Autologous platelet rich plasma promotes the healing of non-ischemic diabetic foot ulcers. A Randomized Controlled Trial. Ann Vasc Surg. 2022;82:165-71. [CrossRef]
- Gupta A, Channaveera C, Sethi S, Ranga S, Anand V. Efficacy of intralesional platelet-rich plasma in diabetic foot ulcer. J Am Podiatr Med Assoc. 2021;111(3):Article_7. [CrossRef]
- Ma C, Hernandez MA, Kirkpatrick VE, Liang LJ, Nouvong AL, Gordon II. Topical platelet-derived growth factor vs placebo therapy of diabetic foot ulcers offloaded with windowed casts: a randomized, controlled trial. Wounds. 2015;27(4):83-91.
- Çetinkaya RA, Yenilmez E, Petrone P, et al. Platelet-rich plasma as an additional therapeutic option for infected wounds with multi-drug resistant bacteria: in vitro antibacterial activity study. Eur J Trauma Emerg Surg. 2019;45(3):555-65. [CrossRef]
- Da Silva J, Leal EC, Carvalho E. Bioactive antimicrobial peptides as therapeutic agents for infected diabetic foot ulcers. Biomolecules. 2021;11(12):1894. [CrossRef]
- Villalba-Rodríguez AM, Martínez-González S, Sosa-Hernández JE, Parra-Saldívar R, Bilal M, Iqbal HMN. Nanoclay/polymer-based hydrogels and enzyme-loaded nanostructures for wound healing applications. Gels. 2021;7(2):59. [CrossRef]
- Balcucho J, Narváez DM, Castro-Mayorga JL. Antimicrobial and biocompatible polycaprolactone and copper oxide nanoparticle wound dressings against methicillin-resistant Staphylococcus aureus. Nanomaterials (Basel). 2020;10(9):1692. [CrossRef]
- Gomes D, Santos R, S Soares R, et al. Pexiganan in combination with nisin to control polymicrobial diabetic foot infections. Antibiotics (Basel). 2020;9(3):128. [CrossRef]
- Loera-Valencia R, Neira RE, Urbina BP, Camacho A, Galindo RB. Evaluation of the therapeutic efficacy of dressings with ZnO nanoparticles in the treatment of diabetic foot ulcers. Biomed Pharmacother. 2022;155:113708. [CrossRef]
- Teobaldi I, Stoico V, Perrone F, et al. Effect of a topical gel based on adelmidrol + trans-traumatic acid in the treatment of diabetic foot ulcers: an open-label study. J Am Podiatr Med Assoc. 2022;112(1):20-143. [CrossRef]
- Najafian Y, Khorasani ZM, Najafi MN, Hamedi SS, Mahjour M, Feyzabadi Z. Efficacy of aloe vera/ plantago major gel in diabetic foot ulcer: a randomized double-blind clinical trial. Curr Drug Discov Technol. 2019;16(2):223-31. [CrossRef]
- Grek CL, Prasad GM, Viswanathan V, Armstrong DG, Gourdie RG, Ghatnekar GS. Topical administration of a connexin43-based peptide augments healing of chronic neuropathic diabetic foot ulcers: a multicenter, randomized trial. Wound Repair Regen. 2015;23(2):203-12. [CrossRef]
- Lobmann R, Augustin M, Lawall H, et al. Cost-effectiveness of TLC-sucrose octasulfate versus control dressings in the treatment of diabetic foot ulcers. J Wound Care. 2019;28(12):808-16. [CrossRef]
- Yingsakmongkol N. Clinical outcomes of WF10 adjunct to standard treatment of diabetic foot ulcers. J Wound Care. 2013;22(3):130-6. [CrossRef]
- Gasca-Lozano LE, Lucano-Landeros S, Ruiz-Mercado H, et al. Pirfenidone accelerates wound healing in chronic diabetic foot ulcers: a randomized, double-blind controlled trial. J Diabetes Res. 2017;2017:3159798. [CrossRef]
- Edmonds M, Lázaro-Martínez JL, Alfayate-García JM, et al. Sucrose octasulfate dressing versus control dressing in patients with neuroischaemic diabetic foot ulcers (Explorer): an international, multicentre, double-blind, randomised, controlled trial. Lancet Diabetes Endocrinol. 2018;6(3):186-96. [CrossRef]
- Monami M, Scatena A, Zannoni S, et al. A randomized, open-label, controlled trial to evaluate the antimicrobial and surgical effect of CO2 laser treatment in diabetic infected foot ulcers: DULCIS (diabetic ulcer, CO2 laser, and infections) study. J Endocrinol Invest. 2017;40(9):985-9. [CrossRef]
- Das B, Berthiaume F. Irreversible electroporation as an alternative to wound debridement surgery. Surg Technol Int. 2021;39:67-73. [CrossRef]
- Lázaro-Martínez JL, Álvaro-Afonso FJ, Sevillano-Fernández D, García-Álvarez Y, Sanz-Corbalan I, García-Morales E. Cellular proliferation, dermal repair, and microbiological effectiveness of ultrasound-assisted wound debridement (UAW) versus standard wound treatment in complicated diabetic foot ulcers (DFU): an open-label randomized controlled trial. J Clin Med. 2020;9(12):4032. [CrossRef]
- Ramundo J, Gray M. Enzymatic wound debridement. J Wound Ostomy Continence Nurs. 2008;35(3):273-80. [CrossRef]
- Shimada K, Ojima Y, Ida Y, Matsumura H. Efficacy of Versajet hydrosurgery system in chronic wounds: A systematic review. Int Wound J. 2021;18(3):269-78. [CrossRef]
- Hong CC, Nather A, Lee JK, Mao HT. Hydrosurgery is effective for debridement of diabetic foot wounds. Ann Acad Med Singap. 2014;43(8):395-9.
- Taha OA, Connerton PL, Connerton IF, El-Shibiny A. Bacteriophage ZCKP1: a potential treatment for Klebsiella pneumoniae isolated from diabetic foot patients. Front Microbiol. 2018;9:2127. [CrossRef]
- Huon JF, Montassier E, Leroy AG, et al. Phages versus antibiotics to treat infected diabetic wounds in a mouse model: a microbiological and microbiotic evaluation. mSystems. 2020;5(6):e00542-20. [CrossRef]
- Steele A, Stacey HJ, de Soir S, Jones JD. The safety and efficacy of phage therapy for superficial bacterial infections: a systematic review. Antibiotics (Basel). 2020;9(11):754. [CrossRef]
- Morozova VV, Vlassov VV, Tikunova NV. Applications of bacteriophages in the treatment of localized infections in humans. Front Microbiol. 2018;9:1696. [CrossRef]
- Lavery L, Fulmer J, Shebetka KA, et al. Open-label Extension phase of a chronic diabetic foot ulcer multicenter, controlled, randomized clinical trial using cryopreserved placental membrane. Wounds. 2018;30(9):283-9.
- Snyder RJ, Shimozaki K, Tallis A, et al. A Prospective, randomized, multicenter, controlled evaluation of the use of dehydrated amniotic membrane allograft compared to standard of care for the closure of chronic diabetic foot ulcer. Wounds. 2016;28(3):70-7.
- Mohammadi Tofigh A, Tajik M. Comparing the standard surgical dressing with dehydrated amnion and platelet-derived growth factor dressings in the healing rate of diabetic foot ulcer: A randomized clinical trial. Diabetes Res Clin Pract. 2022;185:109775. [CrossRef]
- Carter MJ. Dehydrated human amnion and chorion allograft versus standard of care alone in treatment of Wagner 1 diabetic foot ulcers: a trial-based health economics study. J Med Econ. 2020;23(11):1273-83. [CrossRef]
- Frykberg RG, Gibbons GW, Walters JL, Wukich DK, Milstein FC. A prospective, multicentre, open-label, single-arm clinical trial for treatment of chronic complex diabetic foot wounds with exposed tendon and/or bone: positive clinical outcomes of viable cryopreserved human placental membrane. Int Wound J. 2017;14(3):569-77. [CrossRef]
- Zelen CM, Serena TE, Denoziere G, Fetterolf DE. A prospective randomised comparative parallel study of amniotic membrane wound graft in the management of diabetic foot ulcers. Int Wound J. 2013;10(5):502-7. [CrossRef]
- Lavery LA, Fulmer J, Shebetka KA, et al; Grafix Diabetic Foot Ulcer Study Group. The efficacy and safety of Grafix(®) for the treatment of chronic diabetic foot ulcers: results of a multi-centre, controlled, randomised, blinded, clinical trial. Int Wound J. 2014;11(5):554-60. [CrossRef]
- Buzzi M, de Freitas F, Winter M. A Prospective, descriptive study to assess the clinical benefits of using calendula officinalis hydroglycolic extract for the topical treatment of diabetic foot ulcers. Ostomy Wound Manage. 2016;62(3):8-24. [CrossRef]
- Tabinda A, Shafique MS, Qureshi U, Changeez M, Farooqi Sa, Khan JS. Efficiacy of aloe vera cream for healing diabetic foot ulcers. JRMC.2019;23(2):113-5.
- Henshaw FR, Bolton T, Nube V, et al. Topical application of the bee hive protectant propolis is well tolerated and improves human diabetic foot ulcer healing in a prospective feasibility study. J Diabetes Complications. 2014;28(6):850-7. [CrossRef]
- Bardill JR, Laughter MR, Stager M, Liechty KW, Krebs MD, Zgheib C. Topical gel-based biomaterials for the treatment of diabetic foot ulcers. Acta Biomater. 2022;138:73-91. [CrossRef]
- Kerstan A, Dieter K, Niebergall-Roth E, et al. Translational development of ABCB5+ dermal mesenchymal stem cells for therapeutic induction of angiogenesis in non-healing diabetic foot ulcers. Stem Cell Res Ther. 2022;13(1):455. [CrossRef]
- Dubský M, Jirkovská A, Bem R, et al. Comparison of the effect of stem cell therapy and percutaneous transluminal angioplasty on diabetic foot disease in patients with critical limb ischemia. Cytotherapy. 2014;16(12):1733-8. [CrossRef]
- Yu Q, Qiao GH, Wang M, et al. Stem cell-based therapy for diabetic foot ulcers. Front Cell Dev Biol. 2022;10:812262. [CrossRef]
- Krasilnikova OA, Baranovskii DS, Lyundup AV, Shegay PV, Kaprin AD, Klabukov ID. Stem and somatic cell monotherapy for the treatment of diabetic foot ulcers: review of clinical studies and mechanisms of action. Stem Cell Rev Rep. 2022;18(6):1974-85. [CrossRef]
- Hazenberg CE, Bus SA, Kottink AI, Bouwmans CA, Schönbach-Spraul AM, van Baal SG. Telemedical home-monitoring of diabetic foot disease using photographic foot imaging–a feasibility study. J Telemed Telecare. 2012;18(1):32-6. [CrossRef]
- Rasmussen BS, Froekjaer J, Bjerregaard MR, et al. A Randomized controlled trial comparing telemedical and standard outpatient monitoring of diabetic foot ulcers. Diabetes Care. 2015;38(9):1723-9. [CrossRef]
- Smith-Strøm H, Igland J, Østbye T, et al. The Effect of telemedicine follow-up care on diabetes-related foot ulcers: a cluster-randomized controlled noninferiority trial. Diabetes Care. 2018;41(1):96-103. [CrossRef]
- Najafi B, Mishra R. Harnessing digital health technologies to remotely manage diabetic foot syndrome: a narrative review. Medicina (Kaunas). 2021;57(4):377. [CrossRef]
- Giorgino F, Bhana S, Czupryniak L, et al. Management of patients with diabetes and obesity in the COVID-19 era: Experiences and learnings from South and East Europe, the Middle East, and Africa. Diabetes Res Clin Pract. 2021;172:108617. [CrossRef]
- Tele Sağlık Servisi Uygulama Usul ve Esasları Hakkında Yönerge (26 Mart 2015 / 38110390/010.04/644) [Internet]. Ankara: Resmî Gazete. [erişim 24 Ekim 2023]. https://docplayer.biz.tr/790721-Tele-saglik-servisi-uygulama-usul-ve-esaslari-hakkinda-yonerge.html
- e-Nabız Projesi Genelgesi, 2015 [Internet]. Ankara: T.C. Sağlık Bakanlığı Sağlık Bilgi Sistemleri genel Müdürlüğü. [erişim 24 Ekim 2023]. https://ohsad.org/wp-content/uploads/2015/10/e-nabiz_2015-5.pdf
- Uzaktan Sağlık Hizmetlerinin Sunumu Hakkında Yönetmelik (10 Şubat 2022 / 31746) [Internet]. Ankara: Resmî Gazete. [erişim 24 Ekim 2023]. https://www.resmigazete.gov.tr/eskiler/2022/02/20220210-2.htm
- Raspovic KM, Johnson MJ, Wukich DK. A Stepwise approach to nonoperative and operative management of the diabetic foot ulceration. Phys Med Rehabil Clin N Am. 2022;33(4):833-44. [CrossRef]
- Steed DL, Donohoe D, Webster MW, Lindsley L. Effect of extensive debridement and treatment on the healing of diabetic foot ulcers. Diabetic Ulcer Study Group. J Am Coll Surg. 1996;183(1):61-4.
- Uncu H. Diyabetik ayak tedavisi ve cerrahi yaklaşım. In: Uncu H, ed. Yara. 1. baskı. Ankara: Türkiye Klinikleri, 2021: 91-101.
- Hsu CR, Chang CC, Chen YT, Lin WN, Chen MY. Organization of wound healing services: The impact on lowering the diabetes foot amputation rate in a ten-year review and the importance of early debridement. Diabetes Res Clin Pract. 2015;109(1):77-84. [CrossRef]
- Madhok BM, Vowden K, Vowden P. New techniques for wound debridement. Int Wound J. 2013 Jun;10(3):247-51. [CrossRef]
- Ovington LG. Hanging wet-to-dry dressings out to dry. Home Healthc Nurse. 2001;19(8):477-83. [CrossRef]
- McCallon SK, Weir D, Lantis JC. Optimizing wound bed preparation with collagenase enzymatic debridement. J Am Coll Clin Wound Spec. 2015;6(1-2):14-23. [CrossRef]
- Ayello EA, Cuddigan JE. Debridement: controlling the necrotic/cellular burden. Adv Skin Wound Care. 2004;17(2):66-75; quiz 76-8. [CrossRef]
- Uccioli L, Meloni M, Giurato L, et al. Emergency in diabetic foot. Emergency Med 2013;3(6):1-6.
- Armstrong DG, Lavery LA, Harkless LB. Validation of a diabetic wound classification system. The contribution of depth, infection, and ischemia to risk of amputation. Diabetes Care. 1998;21(5):855-9. [CrossRef]
- Zgonis T, Stapleton JJ, Rodriguez RH, Girard-Powell VA, Cromack DT. Plastic surgery reconstruction of the diabetic foot. AORN J. 2008;87(5):951-66; quiz 967-70. [CrossRef]
- Sohrabi S, Russell D. Diabetic foot and foot debridement technique. Surgery (Oxford). 2017;35(9):500-4. [CrossRef]
- Lázaro Martínez JL, Almaraz MC, Álvarez Hermida Á, et al. Consensus document on actions to prevent and to improve the management of diabetic foot in Spain. Endocrinol Diabetes Nutr (Engl Ed). 2021;68(7):509-13. [CrossRef]
- Polk C, Sampson MM, Roshdy D, Davidson LE. Skin and soft tissue infections in patients with diabetes mellitus. Infect Dis Clin North Am. 2021;35(1):183-97. [CrossRef]
- Apelqvist J, Larsson J, Agardh CD. Medical risk factors in diabetic patients with foot ulcers and severe peripheral vascular disease and their influence on outcome. J Diabetes Complications. 1992;6(3):167-74. [CrossRef]
- Fitridge R, Chuter V, Mills J, et al. The intersocietal IWGDF, ESVS, SVS guidelines on peripheral artery disease in people with diabetes mellitus and a foot ulcer. J Vasc Surg. 2023;78(5):1101-31. [CrossRef]
- Margolis DJ, Kantor J, Santanna J, Strom BL, Berlin JA. Risk factors for delayed healing of neuropathic diabetic foot ulcers: a pooled analysis. Arch Dermatol. 2000;136(12):1531-5. [CrossRef]
- Edmonds M. Vascular disease in the lower limb in type 1 diabetes. Cardiovasc Endocrinol Metab. 2019;8(1):39-46. [CrossRef]
- Everhart JE, Pettitt DJ, Knowler WC, Rose FA, Bennett PH. Medial arterial calcification and its association with mortality and complications of diabetes. Diabetologia. 1988;31(1):16-23. [CrossRef]
- Melton LJ 3rd, Macken KM, Palumbo PJ, Elveback LR. Incidence and prevalence of clinical peripheral vascular disease in a population-based cohort of diabetic patients. Diabetes Care. 1980;3(6):650-4. [CrossRef]
- Prompers L, Schaper N, Apelqvist J, et al. Prediction of outcome in individuals with diabetic foot ulcers: focus on the differences between individuals with and without peripheral arterial disease. The EURODIALE Study. Diabetologia. 2008;51(5):747-55. [CrossRef]
- Boyko EJ, Ahroni JH, Stensel V, Forsberg RC, Davignon DR, Smith DG. A prospective study of risk factors for diabetic foot ulcer. The Seattle Diabetic Foot Study. Diabetes Care. 1999;22(7):1036-42. [CrossRef]
- Morbach S, Furchert H, Gröblinghoff U, et al. Long-term prognosis of diabetic foot patients and their limbs: amputation and death over the course of a decade. Diabetes Care. 2012;35(10):2021-7. [CrossRef]
- Edmonds ME, Morrison N, Laws JW, Watkins PJ. Medial arterial calcification and diabetic neuropathy. Br Med J (Clin Res Ed). 1982;284(6320):928-30. [CrossRef]
- Forsythe RO, Apelqvist J, Boyko EJ, et al. Effectiveness of bedside investigations to diagnose peripheral artery disease among people with diabetes mellitus: A systematic review. Diabetes Metab Res Rev. 2020;36 Suppl 1:e3277. [CrossRef]
- Hinchliffe RJ, Andros G, Apelqvist J, et al. A systematic review of the effectiveness of revascularization of the ulcerated foot in patients with diabetes and peripheral arterial disease. Diabetes Metab Res Rev. 2012;28 Suppl 1:179-217. Erratum in: Diabetes Metab Res Rev. 2012;28(4):376. Fiedrichs, S [corrected to Friederichs, S]. [CrossRef]
- Vriens B, D’Abate F, Ozdemir BA, et al. Clinical examination and non-invasive screening tests in the diagnosis of peripheral artery disease in people with diabetes-related foot ulceration. Diabet Med. 2018;35(7):895-902. [CrossRef]
- Tehan PE, Barwick AL, Sebastian M, Chuter VH. Diagnostic accuracy of resting systolic toe pressure for diagnosis of peripheral arterial disease in people with and without diabetes: a cross-sectional retrospective case-control study. J Foot Ankle Res. 2017;10:58. [CrossRef]
- Polat A. Periferik arter hastalığı. In: Bozkurt AK, ed. Periferik Arter ve Ven Hastalıkları: Ulusal Tedavi Kılavuzu, Türk Kalp ve Damar Cerrahisi Derneği, Ulusal Vasküler ve Endovasküler Cerrahi Derneği, Fleboloji Derneği. İstanbul: Bayçınar Yayınevi, 2021: 1-99.
- Özker E. Diyabetik ayak. In: Eray-Yıldız C, Karpuzoğlu E, Uğur M, eds. Kalp Damar Cerrahisinde Yara bakım Ortak Görüş. İstanbul: Ulusal Vasküler ve Endovasküler Cerrahi Derneği, Bayçınar Yayınevi, 2021: 3-17.
- Lehrman ED, Plotnik AN, Hope T, Saloner D. Ferumoxytol-enhanced MRI in the peripheral vasculature. Clin Radiol. 2019;74(1):37-50. [CrossRef]
- Hinchliffe RJ, Brownrigg JR, Andros G, et al; International Working Group on the Diabetic Foot. Effectiveness of revascularization of the ulcerated foot in patients with diabetes and peripheral artery disease: a systematic review. Diabetes Metab Res Rev. 2016;32 Suppl 1:136-44. [CrossRef]
- Chuter V, Schaper N, Mills J, et al. Effectiveness of revascularisation for the ulcerated foot in patients with diabetes and peripheral artery disease: A systematic review. Diabetes Metab Res Rev. 2023:e3700. [CrossRef]
- Farber A, Menard MT, Conte MS, et al; BEST-CLI Investigators. Surgery or Endovascular Therapy for Chronic Limb-Threatening Ischemia. N Engl J Med. 2022;387(25):2305-16. [CrossRef]
- Bradbury AW, Moakes CA, Popplewell M, et al; BASIL-2 Investigators. A vein bypass first versus a best endovascular treatment first revascularisation strategy for patients with chronic limb threatening ischaemia who required an infra-popliteal, with or without an additional more proximal infra-inguinal revascularisation procedure to restore limb perfusion (BASIL-2): an open-label, randomised, multicentre, phase 3 trial. Lancet. 2023;401(10390):1798-809. [CrossRef]
- Waibel FWA, Böni T. Nonoperative treatment of charcot neuro-osteoarthropathy. Foot Ankle Clin. 2022;27(3):595-616. [CrossRef]
- Varma AK. Charcot neuroarthropathy of the foot and ankle: a review. J Foot Ankle Surg. 2013;52(6):740-9. [CrossRef]
- Madan SS, Pai DR. Charcot neuroarthropathy of the foot and ankle. Orthop Surg. 2013;5(2):86-93. [CrossRef]
- Rosskopf AB, Loupatatzis C, Pfirrmann CWA, Böni T, Berli MC. The Charcot foot: a pictorial review. Insights Imaging. 2019;10(1):77. [CrossRef]
- Liao X, Li SH, El Akkawi MM, Fu XB, Liu HW, Huang YS. Surgical amputation for patients with diabetic foot ulcers: A Chinese expert panel consensus treatment guide. Front Surg. 2022;9:1003339. [CrossRef]
- Michelsson O, Tukiainen E. Minor forefoot amputations in patients with diabetic foot ulcers. Foot Ankle Clin. 2022;27(3):671-85. [CrossRef]
- Berli MC. Mid- and hindfoot amputations in diabetic patients. Foot Ankle Clin. 2022;27(3):687-700. [CrossRef]
- Schultz GS, Barillo DJ, Mozingo DW, Chin GA; Wound Bed Advisory Board Members. Wound bed preparation and a brief history of TIME. Int Wound J. 2004;1(1):19-32. [CrossRef]
- Sibbald RG, Elliott JA, Persaud-Jaimangal R, et al. Wound bed preparation 2021. Adv Skin Wound Care. 2021;34(4):183-95. [CrossRef]
- Tuğ T, Konuk Y. Yara bakım ürünleri. In: Uncu H, ed. Yara. 1. baskı. Ankara: Türkiye Klinikleri, 2021: 199-205.
- Eriksson E, Liu PY, Schultz GS, et al. Chronic wounds: Treatment consensus. Wound Repair Regen. 2022;30(2):156-71. Erratum in: Wound Repair Regen. 2022;30(4):536. [CrossRef]
- Dowsett C, von Hallern B. The triangle of wound assessment. A hollistic framework from wound asessment to management goals and treatments. Wounds Int. 2017;8(4):34-9.
- Shi C, Wang C, Liu H, et al. Selection of appropriate wound dressing for various wounds. Front Bioeng Biotechnol. 2020;8:182. [CrossRef]
- Weller CD, Team V, Sussman G. First-line interactive wound dressing update: a comprehensive review of the evidence. Front Pharmacol. 2020;11:155. [CrossRef]
- Demirkan A. Topikal antimikrobiyal ajanlar ve antiseptikler. In: Uncu H, ed. Yara. 1. baskı. Ankara: Türkiye Klinikleri, 2021: 52-60.
- Veves A, Sheehan P, Pham HT. A randomized, controlled trial of Promogran (a collagen/oxidized regenerated cellulose dressing) vs standard treatment in the management of diabetic foot ulcers. Arch Surg. 2002;137(7):822-7. [CrossRef]
- Uppal R, Ramaswamy GN, Arnold C, Goodband R, Wang Y. Hyaluronic acid nanofiber wound dressing–production, characterization, and in vivo behavior. J Biomed Mater Res B Appl Biomater. 2011;97(1):20-9. [CrossRef]
- Türkiye Endokrinoloji ve Metabolizma Derneği Diabetes Mellitus Çalışma ve Eğitim Grubu. Diabetes Mellitus ve Komplikasyonlarının Tanı, Tedavi ve İzlem Kılavuzu-2022. 15. baskı. Ankara: Türkiye Endokrinoloji ve Metabolizma Derneği, 2022.
- El Sayed NA, Aleppo G, Aroda VR, et al. Standards of care in diabetes-2023. Diabetes Care. 2023;46(Supplement_1):S1-S291.
- Pop-Busui R, Boulton AJ, Feldman EL, et al. Diabetic neuropathy: a position statement by the American Diabetes Association. Diabetes Care. 2017;40(1):136-54. [CrossRef]
- Blonde L, Umpierrez GE, Reddy SS, et al. American Association of Clinical Endocrinology Clinical Practice Guideline: developing a diabetes mellitus comprehensive care plan-2022 update. Endocr Pract. 2022;28(10):923-1049. Erratum in: Endocr Pract. 2023;29(1):80-1. [CrossRef]
- Nguyen M, Jankovic I, Kalesinskas L, Baiocchi M, Chen JH. Machine learning for initial insulin estimation in hospitalized patients. J Am Med Inform Assoc. 2021;28(10):2212-9. [CrossRef]
- Nathan DM, Genuth S, Lachin J, et al; Diabetes Control and Complications Trial Research Group. The effect of intensive treatment of diabetes on the development and progression of long-term complications in insulin-dependent diabetes mellitus. N Engl J Med. 1993;329(14):977-86. [CrossRef]
- UK Prospective Diabetes Study (UKPDS) Group. Intensive blood-glucose control with sulphonylureas or insulin compared with conventional treatment and risk of complications in patients with type 2 diabetes (UKPDS 33). Lancet. 1998;352(9131):837-53. Erratum in: Lancet 1999;354(9178):602.
- Kubat-Üzüm A, Satman İ. Diyabetik ayak ülseri olan hastada kan şekerinin düzenlenmesi. In: Baktıroğlu S, Aktaş Ş, eds. Kronik Yarada Güncel Yaklaşımlar. İstanbul: İstanbul Üniversitesi İstanbul Tıp Fakültesi Kronik Yara Konseyi Yayınları, 2013:210-8.
- Miller JD, Carter E, Shih J, et al. How to do a 3-minute diabetic foot exam. J Fam Pract. 2014;63(11):646-56. Erratum in: J Fam Pract. 2015;64(8):452.
- Aydoğdu S, Güler K, Bayram F, et al. [2019 Turkish Hypertension Consensus Report]. Turk Kardiyol Dern Ars. 2019;47(6):535-46. Turkish. [CrossRef]
- Alencherry B, Laffin LJ. Treatment of hypertension in patients with diabetes mellitus: a contemporary approach. Curr Cardiol Rep. 2021;23(3):14. [CrossRef]
- Authors/Task Force Members; ESC Committee for Practice Guidelines (CPG); ESC National Cardiac Societies. 2019 ESC/EAS guidelines for the management of dyslipidaemias: Lipid modification to reduce cardiovascular risk. Atherosclerosis. 2019;290:140-205. Erratum in: Atherosclerosis. 2020;292:160-2. Erratum in: Atherosclerosis. 2020;294:80-2. [CrossRef]
- Bus SA, Lavery LA, Monteiro-Soares M, et al; International Working Group on the Diabetic Foot. Guidelines on the prevention of foot ulcers in persons with diabetes (IWGDF 2019 update). Diabetes Metab Res Rev. 2020;36 Suppl 1:e3269. [CrossRef]
- Fernando ME, Crowther RG. The importance of foot pressure in diabetes. Handbook of Human Motion. 2016;1-29. [CrossRef]
- Wang L, Jones D, Chapman GJ, et al. A Review of wearable sensor systems to monitor plantar loading in the assessment of diabetic foot ulcers. IEEE Trans Biomed Eng. 2020;67(7):1989-2004. [CrossRef]
- Martinez-Santos A, Preece S, Nester CJ. Evaluation of orthotic insoles for people with diabetes who are at-risk of first ulceration. J Foot Ankle Res. 2019;12:35. [CrossRef]
- Gao Y, Wang C, Chen D, et al. Effects of novel diabetic therapeutic footwear on preventing ulcer recurrence in patients with a history of diabetic foot ulceration: study protocol for an open-label, randomized, controlled trial. Trials. 2021;22(1):151. [CrossRef]
- Maciejewski ML, Reiber GE, Smith DG, Wallace C, Hayes S, Boyko EJ. Effectiveness of diabetic therapeutic footwear in preventing reulceration. Diabetes Care. 2004;27(7):1774-82. [CrossRef]
- Lin TL, Sheen HM, Chung CT, et al. The effect of removing plugs and adding arch support to foam based insoles on plantar pressures in people with diabetic peripheral neuropathy. J Foot Ankle Res. 2013;6(1):29. [CrossRef]
- Actis RL, Ventura LB, Lott DJ, et al. Multi-plug insole design to reduce peak plantar pressure on the diabetic foot during walking. Med Biol Eng Comput. 2008;46(4):363-71. [CrossRef]
- Bus SA, Armstrong DG, Gooday C, et al; International Working Group on the Diabetic Foot (IWGDF). Guidelines on offloading foot ulcers in persons with diabetes (IWGDF 2019 update). Diabetes Metab Res Rev. 2020;36 Suppl 1:e3274. [CrossRef]
- Begg L, McLaughlin P, Vicaretti M, Fletcher J, Burns J. Total contact cast wall load in patients with a plantar forefoot ulcer and diabetes. J Foot Ankle Res. 2016;9:2. [CrossRef]
- Fernando ME, Horsley M, Jones S, et al; Australian Diabetes-related Foot Disease Guidelines & Pathways Project. Australian guideline on offloading treatment for foot ulcers: part of the 2021 Australian evidence-based guidelines for diabetes-related foot disease. J Foot Ankle Res. 2022;15(1):31. [CrossRef]
- Ha Van G, Siney H, Hartmann-Heurtier A, Jacqueminet S, Greau F, Grimaldi A. Nonremovable, windowed, fiberglass cast boot in the treatment of diabetic plantar ulcers: efficacy, safety, and compliance. Diabetes Care. 2003;26(10):2848-52. [CrossRef]
- Armstrong DG, Lavery LA, Wu S, Boulton AJ. Evaluation of removable and irremovable cast walkers in the healing of diabetic foot wounds: a randomized controlled trial. Diabetes Care. 2005;28(3):551-4. [CrossRef]
- Chakraborty PP, Ray S, Biswas D, et al. A comparative study between total contact cast and pressure-relieving ankle foot orthosis in diabetic neuropathic foot ulcers. J Diabetes Sci Technol. 2015;9(2):302-8. [CrossRef]
- Faglia E, Caravaggi C, Clerici G, et al. Effectiveness of removable walker cast versus nonremovable fiberglass off-bearing cast in the healing of diabetic plantar foot ulcer: a randomized controlled trial. Diabetes Care. 2010;33(7):1419-23. [CrossRef]
- Lavery LA, Higgins KR, La Fontaine J, Zamorano RG, Constantinides GP, Kim PJ. Randomised clinical trial to compare total contact casts, healing sandals and a shear-reducing removable boot to heal diabetic foot ulcers. Int Wound J. 2015;12(6):710-5. [CrossRef]
- Caravaggi C, Faglia E, De Giglio R, et al. Effectiveness and safety of a nonremovable fiberglass off-bearing cast versus a therapeutic shoe in the treatment of neuropathic foot ulcers: a randomized study. Diabetes Care. 2000;23(12):1746-51. [CrossRef]
- Foto JG, Birke JA. Evaluation of multidensity orthotic materials used in footwear for patients with diabetes. Foot Ankle Int. 1998;19(12):836-41. Erratum in: Foot Ankle Int. 1999;20(2):143. [CrossRef]
- Viswanathan V, Madhavan S, Gnanasundaram S, et al. Effectiveness of different types of footwear insoles for the diabetic neuropathic foot: a follow-up study. Diabetes Care. 2004;27(2):474-7. [CrossRef]
- Pabón-Carrasco M, Juárez-Jiménez JM, Reina-Bueno M, Coheña-Jiménez M. Behavior of provisional pressure-reducing materials in diabetic foot. J Tissue Viability. 2016;25(2):143-9. [CrossRef]
- Hastings MK, Mueller MJ, Pilgram TK, Lott DJ, Commean PK, Johnson JE. Effect of metatarsal pad placement on plantar pressure in people with diabetes mellitus and peripheral neuropathy. Foot Ankle Int. 2007;28(1):84-8. [CrossRef]
- Johnson DJ, Saar BJ, Shevitz AJ, et al. A Total offloading foot brace for treatment of diabetic foot ulcers: results from a halted randomized controlled trial. Wounds. 2018;30(7):182-5.
- Slater RA, Hershkowitz I, Ramot Y, Buchs A, Rapoport MJ. Reduction of digital plantar pressure by debridement and silicone orthosis. Diabetes Res Clin Pract. 2006;74(3):263-6. [CrossRef]
- De Luccia N, Pinto MA, Guedes JP, Albers MT. Rehabilitation after amputation for vascular disease: a follow-up study. Prosthet Orthot Int. 1992;16(2):124-8. [CrossRef]
- Fleury AM, Salih SA, Peel NM. Rehabilitation of the older vascular amputee: a review of the literature. Geriatr Gerontol Int. 2013;13(2):264-73. [CrossRef]
- Jindra M, Věchtová B, Bielmeierová J. [Basic principles and difficulties relating to rehabilitation in diabetic patients following amputation]. Vnitr Lek. 2015;61(6):604-8. Czech.
- Abidia A, Laden G, Kuhan G, et al. The role of hyperbaric oxygen therapy in ischaemic diabetic lower extremity ulcers: a double-blind randomised-controlled trial. Eur J Vasc Endovasc Surg. 2003;25(6):513-8. [CrossRef]
- Kalani M, Jörneskog G, Naderi N, Lind F, Brismar K. Hyperbaric oxygen (HBO) therapy in treatment of diabetic foot ulcers. Long-term follow-up. J Diabetes Complications. 2002;16(2):153-8. [CrossRef]
- Kessler L, Bilbault P, Ortéga F, et al. Hyperbaric oxygenation accelerates the healing rate of nonischemic chronic diabetic foot ulcers: a prospective randomized study. Diabetes Care. 2003;26(8):2378-82. [CrossRef]
- Löndahl M, Katzman P, Nilsson A, Hammarlund C. Hyperbaric oxygen therapy facilitates healing of chronic foot ulcers in patients with diabetes. Diabetes Care. 2010;33(5):998-1003. [CrossRef]
- Chen CY, Wu RW, Hsu MC, Hsieh CJ, Chou MC. Adjunctive hyperbaric oxygen therapy for healing of chronic diabetic foot ulcers: a randomized controlled trial. J Wound Ostomy Continence Nurs. 2017;44(6):536-45. [CrossRef]
- Perren S, Gatt A, Papanas N, Formosa C. Hyperbaric oxygen therapy in ischaemic foot ulcers in type 2 diabetes: a clinical trial. Open Cardiovasc Med J. 2018;12:80-5. [CrossRef]
- Salama SE, Eldeeb AE, Elbarbary AH, Abdelghany SE. Adjuvant hyperbaric oxygen therapy enhances healing of nonischemic diabetic foot ulcers compared with standard wound care alone. Int J Low Extrem Wounds. 2019;18(1):75-80. [CrossRef]
- Nik Hisamuddin NAR, Wan Mohd Zahiruddin WN, Mohd Yazid B, Rahmah S. Use of hyperbaric oxygen therapy (HBOT) in chronic diabetic wound – A randomised trial. Med J Malaysia. 2019;74(5):418-24.
- Faglia E, Favales F, Aldeghi A, et al. Adjunctive systemic hyperbaric oxygen therapy in treatment of severe prevalently ischemic diabetic foot ulcer. A randomized study. Diabetes Care. 1996;19(12):1338-43. [CrossRef]
- Doctor N, Pandya S, Supe A. Hyperbaric oxygen therapy in diabetic foot. J Postgrad Med. 1992;38(3):112-4.
- Fedorko L, Bowen JM, Jones W, et al. Hyperbaric oxygen therapy does not reduce indications for amputation in patients with diabetes with nonhealing ulcers of the lower limb: a prospective, double-blind, randomized controlled clinical trial. Diabetes Care. 2016;39(3):392-9. [CrossRef]
- Santema KTB, Stoekenbroek RM, Koelemay MJW, et al; DAMO2CLES Study Group. Hyperbaric oxygen therapy in the treatment of ischemic lower- extremity ulcers in patients with diabetes: results of the DAMO2CLES multicenter randomized clinical trial. Diabetes Care. 2018;41(1):112-9. [CrossRef]
- Huang ET. Comment on Fedorko et al. Hyperbaric oxygen therapy does not reduce indications for amputation in patients with diabetes with nonhealing ulcers of the lower limb: a prospective, double-blind, randomized controlled clinical trial. Diabetes Care. 2016;39:392-9. Diabetes Care. 2016;39(8):e133-4. [CrossRef]
- Löndahl M, Fagher K, Katzman P. Comment on Fedorko et al. Hyperbaric oxygen therapy does not reduce indications for amputation in patients with diabetes with nonhealing ulcers of the lower limb: a prospective, double-blind, randomized controlled clinical trial. Diabetes Care. 2016;39:392-9. Diabetes Care. 2016;39(8):e131-2. [CrossRef]
- Murad MH. Comment on Fedorko et al. Hyperbaric oxygen therapy does not reduce indications for amputation in patients with diabetes with nonhealing ulcers of the lower limb: a prospective, double-blind, randomized controlled clinical trial. Diabetes Care. 2016;39:392-9. Diabetes Care. 2016;39(8):e135. [CrossRef]
- Mutluoglu M, Uzun G, Bennett M, Germonpré P, Smart D, Mathieu D. Poorly designed research does not help clarify the role of hyperbaric oxygen in the treatment of chronic diabetic foot ulcers. Diving Hyperb Med. 2016;46(3):133-4.
- LeDez KM. Serious concerns about the Toronto Hyperbaric Oxygen for Diabetic Foot Ulcer study. Undersea Hyperb Med. 2016;43(6):737-42.
- Strauss MB. Concerns regarding Fedorko, et al.’s article: Hyperbaric oxygen does not reduce indications. Undersea Hyperb Med. 2016;43(6):742-3.
- Mutluoglu M. Comment on Santema et al. Hyperbaric oxygen therapy in the treatment of ischemic lower-extremity ulcers in patients with diabetes: results of the DAMO2CLES multicenter randomized clinical trial. Diabetes Care. 2018;41:112-9. Diabetes Care. 2018;41(4):e60. [CrossRef]
- Huang E. Comment on Santema et al. Hyperbaric oxygen therapy in the treatment of ischemic lower-extremity ulcers in patients with diabetes: results of the damo2cles multicenter randomized clinical trial. Diabetes Care 2018;41:112-9. Diabetes Care. 2018;41(4):e61. [CrossRef]
- Kranke P, Bennett MH, Martyn-St James M, Schnabel A, Debus SE, Weibel S. Hyperbaric oxygen therapy for chronic wounds. Cochrane Database Syst Rev. 2015;2015(6):CD004123. [CrossRef]
- Elraiyah T, Tsapas A, Prutsky G, et al. A systematic review and meta-analysis of adjunctive therapies in diabetic foot ulcers. J Vasc Surg. 2016;63(2 Suppl):46S-58S.e1-2. [CrossRef]
- Zhao D, Luo S, Xu W, Hu J, Lin S, Wang N. Efficacy and safety of hyperbaric oxygen therapy used in patients with diabetic foot: a meta-analysis of randomized clinical trials. Clin Ther. 2017;39(10):2088-94.e2. [CrossRef]
- Golledge J, Singh TP. Systematic review and meta-analysis of clinical trials examining the effect of hyperbaric oxygen therapy in people with diabetes-related lower limb ulcers. Diabet Med. 2019;36(7):813-26. [CrossRef]
- Brouwer RJ, Lalieu RC, Hoencamp R, van Hulst RA, Ubbink DT. A systematic review and meta-analysis of hyperbaric oxygen therapy for diabetic foot ulcers with arterial insufficiency. J Vasc Surg. 2020;71(2):682-92.e1. [CrossRef]
- Sharma R, Sharma SK, Mudgal SK, Jelly P, Thakur K. Efficacy of hyperbaric oxygen therapy for diabetic foot ulcer, a systematic review and meta-analysis of controlled clinical trials. Sci Rep. 2021;11(1):2189. [CrossRef]
- Wenhui L, Changgeng F, Lei X, Baozhong Y, Guobin L, Weijing F. Hyperbaric oxygen therapy for chronic diabetic foot ulcers: An overview of systematic reviews. Diabetes Res Clin Pract. 2021;176:108862. [CrossRef]
- Moreira DA Cruz DL, Oliveira-Pinto J, Mansilha A. The role of hyperbaric oxygen therapy in the treatment of diabetic foot ulcers: a systematic review with meta-analysis of randomized controlled trials on limb amputation and ulcer healing. Int Angiol. 2022;41(1):63-73. [CrossRef]
- Zhang Z, Zhang W, Xu Y, Liu D. Efficacy of hyperbaric oxygen therapy for diabetic foot ulcers: An updated systematic review and meta-analysis. Asian J Surg. 2022;45(1):68-78. [CrossRef]
- Argenta LC, Morykwas MJ. Vacuum-assisted closure: a new method for wound control and treatment: clinical experience. Ann Plast Surg. 1997;38(6):563-76.
- Karatepe, O., Eken, I., Acet, E., Unal, O., Mert, M., Koc, B., Karahan, S., Filizcan, U., Ugurlucan, M., Aksoy, M. (2011). Vacuum assisted closure improves the quality of life in patients with diabetic foot. Acta Chir Belg. 111(5), s. 298-302
- Meloni M, Izzo V, Vainieri E, Giurato L, Ruotolo V, Uccioli L. Management of negative pressure wound therapy in the treatment of diabetic foot ulcers. World J Orthop. 2015;6(4):387-93. [CrossRef]
- Diabetic foot problems: prevention and management [Internet]. London: National Institute for Health and Care Excellence (NICE). [erişim 23 Kasım 2023]. https://www.nice.org.uk/guidance/ng19/resources/diabetic-foot-problems-prevention-and-management-pdf-1837279828933
- Everett E, Mathioudakis N. Update on management of diabetic foot ulcers. Ann N Y Acad Sci. 2018;1411(1):153-65. [CrossRef]
- Martínez-Sánchez G, Al-Dalain SM, Menéndez S, et al. Therapeutic efficacy of ozone in patients with diabetic foot. Eur J Pharmacol. 2005;523(1-3):151-61. [CrossRef]
- Wainstein J, Feldbrin Z, Boaz M, Harman-Boehm I. Efficacy of ozone-oxygen therapy for the treatment of diabetic foot ulcers. Diabetes Technol Ther. 2011;13(12):1255-60. [CrossRef]
- Mutluoglu M, Karabacak E, Karagöz H, Uzun G, Ay H. Topical ozone and chronic wounds: improper use of therapeutic tools may delay wound healing. N Am J Med Sci. 2012;4(11):615-6. [CrossRef]
- Izadi M, Kheirjou R, Mohammadpour R, et al. Efficacy of comprehensive ozone therapy in diabetic foot ulcer healing. Diabetes Metab Syndr. 2019;13(1):822-5. doi: 10.1016/j.dsx.2018.11.060. [CrossRef]
- Zhang J, Hu W, Diao Q, et al. Therapeutic effect of the epidermal growth factor on diabetic foot ulcer and the underlying mechanisms. Exp Ther Med. 2019;17(3):1643-8. [CrossRef]
- Zhao DY, Su YN, Li YH, Yu TQ, Li J, Tu CQ. Efficacy and safety of recombinant human epidermal growth factor for diabetic foot ulcers: A systematic review and meta-analysis of randomised controlled trials. Int Wound J. 2020;17(4):1062-73. [CrossRef]
- Han CM, Cheng B, Wu P; writing group of growth factor guideline on behalf of Chinese Burn Association. Clinical guideline on topical growth factors for skin wounds. Burns Trauma. 2020;8:tkaa035. [CrossRef]
- Cama VF, Mayola MF, Marí YM, et al. Epidermal growth factor based therapy promotes intracellular trafficking and accumulation of its receptor in the nucleus of fibroblasts from diabetic foot ulcers. J Diabetic Complications Med. 2016;1(3):111.
- Ertugrul BM, Buke C, Ersoy OS, Ay B, Demirez DS, Savk O. Intralesional epidermal growth factor for diabetic foot wounds: the first cases in Turkey. Diabet Foot Ankle. 2015;6:28419. [CrossRef]
- Ertugrul BM, Yapar N, Taşbakan M, et al. Evaluation of the efficacy and safety of topical epidermal growth factor Regen-D® in diabetic foot wounds. The Diabetic Foot Journal. 2021;24(2): 52-7.
- Mohd Zubir MZ, Holloway S, Mohd Noor N. Maggot therapy in wound healing: a systematic review. Int J Environ Res Public Health. 2020;17(17):6103. [CrossRef]
- Clinical Practice Guideline for the Treatment of Acute and Chronic Wounds with Maggot Depridement Therapy [Internet]. México: Mexican Association for Would Care and Healing. [erişim 29 Şubat 2024]. https://s3.amazonaws.com/aawc-new/memberclicks/GPC_larvatherapy.pdf
- Alavi A, Sibbald RG, Mayer D, et al. Diabetic foot ulcers: Part I. Pathophysiology and prevention. J Am Acad Dermatol. 2014;70(1):1.e1-18; quiz 19-20. [CrossRef]
- Alavi A, Sibbald RG, Mayer D, et al. Diabetic foot ulcers: Part II. Management. J Am Acad Dermatol. 2014;70(1):21.e1-24; quiz 45-6. [CrossRef]
- Bandyk DF. The diabetic foot: Pathophysiology, evaluation, and treatment. Semin Vasc Surg. 2018;31(2-4):43-8. [CrossRef]
- Armstrong DG, Fisher TK, Lepow B, White ML, Mills JL. Pathophysiology and principles of management of the diabetic foot. In: Fitridge R, Thompson M, editors. Mechanisms of Vascular Disease: A Reference Book for Vascular Specialists. Adelaide (AU): University of Adelaide Press; 2011.
- Bus SA, Van Netten JJ, Hinchliffe RJ, Apelqvist J, Lipsky BA, Schaper NC; IWGDF Editorial Board. Standards for the development and methodology of the 2019 International Working Group on the Diabetic Foot guidelines. Diabetes Metab Res Rev. 2020;36 Suppl 1:e3267. [CrossRef]
- Thaniyath TA. Diabetic foot syndrome: risk factors, clinical assessment, and advances in diagnosis. In: Zubair M, Ahmad J, Malik A, Talluri MR. (eds), Diabetic Foot Ulcer. Springer, Singapore; 2021.
- American Diabetes Association Professional Practice Committee. 12. Retinopathy, neuropathy, and foot care: standards of medical care in diabetes-2022. Diabetes Care. 2022;45(Suppl 1):S185-94. [CrossRef]
- Wang A, Lv G, Cheng X, et al. Guidelines on multidisciplinary approaches for the prevention and management of diabetic foot disease (2020 edition). Burns Trauma. 2020;8:tkaa017. [CrossRef]
- Satman İ, İmamoğlu Ş, Yılmaz C, Akalın S, Salman S, Dinççağ N; Türkiye Endokrinoloji ve Metabolizma Derneği Diabetes Mellitus Çalışma ve Eğitim Grubu. Diabetes Mellitus ve Komplikasyonlarının Tanı, Tedavi ve İzlem Kılavuzu. 15. baskı. Ankara: Türkiye Endokrinoloji ve Metabolizma Derneği, 2022.
- American Diabetes Association. Standards of medical care in diabetes–2013. Diabetes Care. 2013;36 Suppl 1(Suppl 1):S11-66. [CrossRef]
- Yang L, Wu Y, Zhou C, et al. Diabetic foot ulcer risk assessment and prevention in patients with diabetes: a best practice implementation project. JBI Evid Implement. 2022;20(4):269-79. [CrossRef]
- Nursing Best Practice Guideline. Shaping the Future of Nursing: Reducing Foot Complications for People with Diabetes [Internet]. Ontario: Registered Nurses Association of Ontario. [Erişim tarihi 5 Ocak 2015]. http://rnao.ca/sites/rnao-ca/files/Foot_Compl_Diabetes_Updated.pdf
- Biçer E, Çelik S. [Comprehensive foot examination for diabetes patients and risk assessment: review]. Turkiye Klinikleri J Nurs Sci. 2016;8(1):62-70. Turkish. [CrossRef]
- Beuscher TL. Guidelines for diabetic foot care: a template for the care of all feet. J Wound Ostomy Continence Nurs. 2019;46(3):241-5. Erratum in: J Wound Ostomy Continence Nurs. 2019;46(4):336. [CrossRef]
- Çelik P, Aydın, HT. [The effect of preventive patient educational program about diabetic foot development on patients’ knowledge and practice of foot care]. Turk J Diab Obes. 2020;4(2):90-7. Turkish. [CrossRef]
- Durakbaşa MO. [Diabetic foot: pathogenesis, clinical forms and their management, comorbidities]. 2013;12:464-75. Turkish. [CrossRef]
- Reyhanoğlu DA, Kara B, Şengün İŞ, Yıldırım G. [Biomechanical changes seen in diabetic neuropathy]. DEÜ Tıp Fakültesi Dergisi. 2018;32(2):167-72. Turkish.
- Burrow JG, McLarnon NA. World at work: Evidence based risk management of nail dust in chiropodists and podiatrists. Occup Environ Med. 2006;63(10):713-6. [CrossRef]
- Singh D, Bentley G, Trevino SG. Fortnightly review: Callosities, corns, and calluses. BMJ. 1996;312(7043):1403. [CrossRef]
- Sholz N. Lehrbuch und Bildatlas für die Podologie. München: Verlag Neuer Merkur, 2003:393.
- Grünewald K. Theorie der medizinischen Fubbehand Band 1. München: Verlag Neuer Merkur, 2012: 210-252.
- Bittig F. Bildatlas Podologie Befund, Behanlung, Prophylaaxe. Stuttgard: Karl F Haug, Verlag, 2017: 159.