En Çok Okunanlar
Özet
Amaç: Bu çalışmada, ventilatörle ilişkili pnömoni (VİP) etkeni olan çoklu ilaç direnci gösteren Acinetobacter baumannii izolatlarında biyofilm oluşumu ile ilişkili fenotipik özelliklerin ve virülans genlerinin varlığının araştırılması amaçlandı.
Yöntemler: 2022–2023 yılları arasında yoğun bakım ünitesinde mekanik ventilasyon uygulanan hastaların trakeal aspirat örneklerinden izole edilen, çoklu ilaç direnci gösteren 23 VİP etkeni A. baumannii izolatı dahil edildi. İzolatların biyofilm oluşturma kapasiteleri mikroplaka kristal viyole yöntemi ile değerlendirildi. Virülans ve biyofilm oluşumu ile ilişkili bap, csuE, ompA, pgaB, csgA, abaI, adeG, traT, cpaA, cnf-1, cnf-2, kpsMII, epsA, ptk, fimH, pilA, basD, bauA ve omp33-36 genlerinin varlığı polimeraz zincir reaksiyonu (PCR) yöntemiyle araştırıldı.
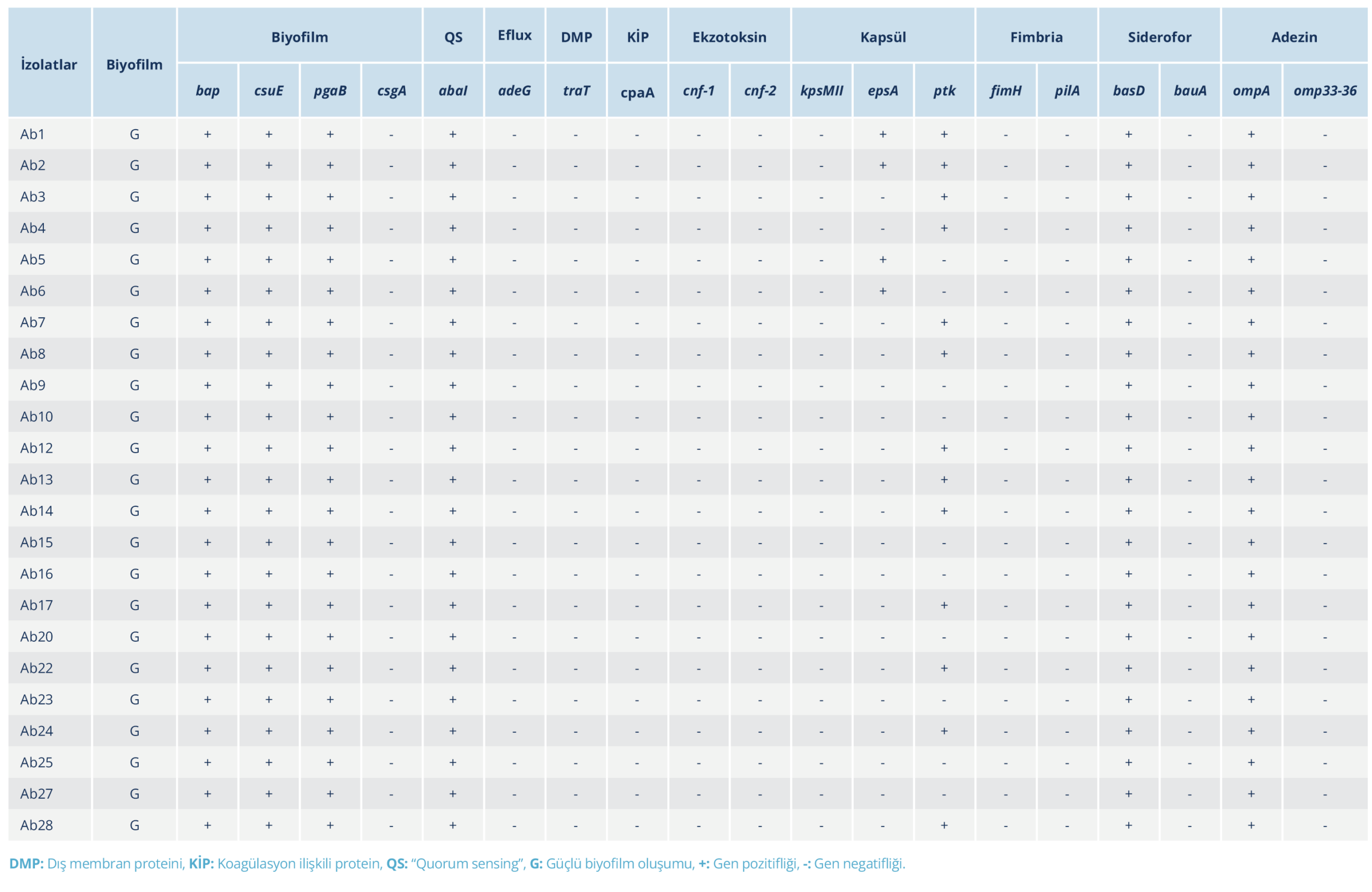
Bulgular: Tüm izolatlarda güçlü biyofilm oluşumu tespit edildi; bap, csuE, ompA ve pgaB genleri tüm izolatlarda pozitif bulunurken, fimH, csgA, adeG, traT, cpaA, cnf-1, cnf-2, kpsMII, pilA, bauA ve omp33-36 genleri hiçbir izolatta tespit edilmedi. Hücreler arası iletişim (quorum sensing, QS) ile ilişkili abaI ve siderofor sisteminden sorumlu basD genleri tüm izolatlarda pozitif iken kapsül ile ilişkili epsA ve ptk genleri sırasıyla %16.6 ve %54.2 oranında pozitif bulundu.
Sonuç: VİP etkeni çoklu ilaç direnci gösteren A. baumannii izolatlarında güçlü biyofilm oluşumu ile bap, csuE, ompA ve pgaB genlerinin tüm izolatlarda saptanması, biyofilm oluşumu ile virülans arasında bir ilişki olabileceğini düşündürmektedir. fimH ve csgA genlerinin saptanmaması, bu genlerin biyofilm oluşumunda belirleyici olmayabileceğine işaret etmektedir. Ayrıca abaI, basD, epsA ve ptk genlerinin varlığı, biyofilm oluşumu ve antibiyotik direnciyle ilişkili olabilecek mekanizmaları desteklemektedir.
GİRİŞ
Hastane kaynaklı pnömoni, Acinetobacter baumannii infeksiyonlarının en önemli klinik tablolarından birini temsil etmektedir. Bu infeksiyonların gelişimine katkıda bulunan risk faktörleri arasında immünosüpresyon, uzun süreli antibiyotik kullanımı, mekanik ventilasyon ve intravenöz ve üriner kateter kullanımı gibi invazif girişimler yer almaktadır. Acinetobacter baumannii’nin doğrudan temas veya kontamine sıvılar yoluyla infeksiyona veya kolonizasyona neden olduğu gösterilmiştir (1).
Tüm dünyada izolasyon sıklığı giderek artan nozokomiyal bir infeksiyon etkeni olan A. baumanni’nin tedavi ve kontrolünde ciddi zorluklar yaşanmaktadır. Bu artışta bakterinin çevresel koşullara uyum yeteneği ile antibiyotiklere karşı geliştirdikleri direnç rol oynamaktadır. Karbapenem dirençli A. baumannii, 2018 yılında Dünya Sağlık Örgütü (DSÖ) tarafından acilen geliştirilmesi gereken birinci öncelikli kritik patojen olarak kabul edilmiştir (2). Artan çoklu ilaç direnci ve uzun süreli nozokomiyal persistans nedeniyle bu etken hastanede yatan hastalar için ciddi bir tehdit haline gelmiştir (3). Hastane kaynaklı infeksiyonların artan önemine rağmen, insan infeksiyonlarının patogenezinde virülans faktörlerinin rolü büyük ölçüde belirsizliğini korumaktadır.
Acinetobacter baumannii ile ilişkili birçok virülans faktörü tanımlanmıştır. Bu faktörler; porinler, lipopolisakkaritler, kapsüler polisakkaritler, fosfolipazlar, protein sekresyon sistemleri, dış membran vezikülleri, demir kazanım mekanizmaları, penisilin bağlayıcı protein 7/8 (PBP7/8), pili ve hareket yeteneği, hemolitik aktivite, biyofilm oluşturma, efluks pompaları ve hücreler arası iletişim (quorum sensing, QS) gibi kritik mekanizmalara etki ederek infeksiyon patogenezinde önemli rol oynamakta ve bakterinin olumsuz koşullarda yaşamını sürdürmesini sağlamaktadır (4).
Acinetobacter baumannii’de seğirme (twitching) hareketi, tip IV pilinin bakteri hücresini tekrarlayan ileri-geri çekme hareketleriyle agar yüzeyinde dallanmış yapılar oluşturması şeklinde tanımlanmıştır (5). Suşların tüm genom analizleri, tip IV pili ile ilişkili çok sayıda genin varlığını ortaya koymuştur. Ana fimbrial alt birim pilA, A. baumannii suşları arasında önemli değişkenlik gösterir ve bu varyasyonların hareket yeteneğindeki farklılıklarla ilişkili olduğu bildirilmiştir (5).
Çoklu ilaç efluks pompaları, geniş substrat özgüllükleri ve yüksek ekspresyon düzeylerinin yanı sıra diğer direnç mekanizmalarıyla sinerjistik etkileri sayesinde çoklu ilaca dirençli suşların ortaya çıkmasında önemli bir rol oynamaktadır. adeABC, adeFGH ve adeIJK genlerinin artan ekspresyonu hem çoklu ilaç direnci hem de virülans ile ilişkilendirilmiştir (6).
Konak yapılarına tutunma, pnömoni gibi infeksiyonların gelişiminde ilk adımı temsil edebilir. ompA, bap ve omp33–36 gibi konak hücreye bağlanmaya aracılık eden adhezinleri kodlayan genler, A. baumannii’nin temel virülans genleri arasında yer almaktadır. Konak hücre içine girdikten sonra, sideroforların (küçük, demir şelatlayıcı moleküller) sentezi ve taşınmasında rol oynayan basD ve bauA gibi genler, bakterinin hayatta kalması için gereklidir (7).
R6–5 plazmidine özgü bir dış membran proteinini kodlayan traT virülans geninin Gram-negatif bakterilerde serumla öldürmeye karşı dirence aracılık ettiği gösterilmiştir. Bu genin özellikle kan dolaşımı infeksiyonlarından izole edilen suşlarda tespit edildiği bildirilmiştir (8). Patogenezin merkezinde yer alan hücreler arası iletişim sistemi (abaI/abaR genleri), bakteri popülasyonları arasında koordineli davranışı mümkün kılarak infeksiyon gelişimini ve konak ortamlarına adaptasyonu kolaylaştırır. Hücreler arası iletişim sisteminin temel bileşenlerinden biri olan abaI geni, sinyal molekülü N-asilhomoserin laktonun (N-AHL) sentezinden sorumlu olup bakteriyel davranış ve patojenitenin düzenlenmesinde kritik rol oynamaktadır (9).
Acinetobacter baumannii, fagositozdan korunmada rol oynayan, kompleman sisteminin aktivasyonunu engelleyen ve virülansına katkıda bulunan bir polisakkarit kapsüle sahiptir. Kapsülün ayrıca hücre yüzeyi hidrofobikliğini artırdığı ve tıbbi cihazlara tutunmayı kolaylaştırdığı bilinmektedir. Kapsül polimerizasyonu için ptk ve epsA genleri gereklidir (10). Grup 2 kapsül genleri arasında sınıflandırılan kpsMII geni ise A. baumannii’de kapsül oluşumu ve konak hücrelere tutunma ile ilişkilendirilmiştir (10).
Acinetobacter baumannii suşlarının, konak antimikrobiyal savunmasının temel bileşenlerinden biri olan ve aynı zamanda çeşitli Gram-negatif bakterilerdeki virülans faktörleri tarafından hedeflenen koagülasyonla ilişkili proteinlere sahip olduğu bulunmuştur. Bu proteinlerden biri, pıhtılaşma süreçlerini hedef alan ve A. baumannii virülansına katkıda bulunan reprolizin benzeri salgılanan bir metalloendopeptidaz olan cpaA’dır (11). Sitotoksik nekrotizan faktör (cnf), insan hücreleri üzerinde sitotoksik etkiler gösterebilen bir ekzotoksin olup, cnf-1, cnf-2, cnf-3, cdt-1, cdt-2, cdt-3 ve cdt-4 genlerini içeren bir gen kümesinin parçası olarak tanımlanmıştır (12).
Acinetobacter baumannii’nin cansız olmalarına rağmen kateter, ventilatör gibi cihazların yüzeylerine tutunma ve kolonize olma yeteneği, hastane ortamlarında uzun süre hayatta kalmasını sağlar; bu durum biyofilm oluşumu ve çoklu ilaç direnci ile yakından bağlantılıdır. Biyofilm oluşturma yeteneğine sahip A. baumannii izolatları konağın bağışıklık sisteminden kaçabilir ve uzun süre hayatta kalarak klinik ortamlarda bulaşıcılığın artmasına neden olabilir (13). Bu etken için biyofilm oluşturma oranı yaklaşık %80–91 aralığında bildirilirken, diğer türlerde %5–24 arasında değişmektedir (14). Biyofilm oluşumu ile antibiyotik direnci gelişimi arasında pozitif bir korelasyon olduğu farklı çalışmalarda gösterilmiştir (15).
Biyofilm oluşumuna A. baumannii’de çeşitli virülans faktörleri katkıda bulunur. Bunlar arasında dış membran proteini A (ompA) ve biyofilmle ilişkili protein (bap) bulunmaktadır. Pilus montajında rol oynayan csuA/BABCDE operonunun yüzeye bağlanma ve biyofilm oluşumu için gerekli olduğu gösterilmiştir. Poli-β-1,6-N-asetilglukozamini kodlayan bir başka operon olan pgaABC de biyofilm gelişiminde önemli bir rol oynamaktadır (16). Fimbria ile ilişkili protein fimH, bakterinin hücre duvarına tutunmasına yardımcı olarak “yakalama bağı” mekanizmasının oluşumuna katkıda bulunur. csgA geni tarafından eksprese edilen curli lifleri, hücre dışı matris proteinleri aracılığıyla konak epitel hücrelerine tutunmayı ve invazyonu kolaylaştırır. Bu lifler konak proteinleriyle etkileşime girerek organizmanın dokularına daha derin nüfuz etmeyi kolaylaştırabilecek bağışıklık tepkilerini tetikler (17).
Bu çalışmada, ventilatörle ilişkili pnömoni (VİP) olgularından izole edilen A. baumannii suşlarında biyofilm oluşumu ve virülans genlerinin varlığının belirlenmesi amaçlandı.
YÖNTEMLER
Bu çalışmaya, VİP etkeni olarak tanımlanan ve çoklu ilaç direnci gösteren 23 A. baumannii izolatı dahil edildi. İzolatlar, 2022–2023 yılları arasında bir eğitim ve araştırma hastanesinin yoğun bakım ünitesinde mekanik ventilasyon uygulanan hastaların trakeal aspirat kültürlerinden elde edildi. Çalışma süresi boyunca toplam 28 A. baumannii etkeni tespit edildi ve tamamı gliseroz stoklara ekilerek saklandı. Daha sonra gen tespiti yapmak için izolatlar uygun besiyerlerine tekrar ekildi. Bu aşamada beş izolat tekrar üretilemediği için 23 A. baumannii izolatıyla çalışma yürütüldü. İzolatların tanımlanması ve antibiyotik duyarlılık profillerinin belirlenmesi, VITEK® otomatize sistemi (bioMérieux, Marcy-l’Étoile, Fransa) kullanılarak gerçekleştirildi.
Bu çalışmada, A. baumannii izolatlarında virülansla ilişkili genlerin ve biyofilmle ilişkili fenotipik özelliklerin genotipik ve fenotipik profilleri araştırıldı. Fenotipik değerlendirmede, izolatların biyofilm oluşturma yetenekleri incelendi. Genotipik değerlendirmede ise patojenite ve biyofilm oluşumundan sorumlu virülans genlerinin varlığı incelendi.
Biyofilm Oluşumunun Araştırılması
İzolatlar kanlı besiyerine pasajlandı ve bir gece inkübasyona bırakıldı. İnkübasyonun ardından %2 glukoz içeren tek koloni 3 ml triptik soy buyyonu (Tryptic Soy Broth, TSB) içerisine ekildi ve 37°C’de çalkalamasız ortamda bir gece inkübe edildi. Gece kültüründen 10 µl alınarak, her kuyucuğunda %2 glukoz içeren 200 µl TSB bulunan düz tabanlı 96 kuyucuklu pleytlere inoküle edildi. Pleytler çalkalamasız ortamda 48 saat inkübe edildi.
İnkübasyon sonunda kuyucuklardaki sıvı besiyeri uzaklaştırıldı. Pleytler üç kez steril distile su (dH2O) ile yıkandı ve oda sıcaklığında kurutuldu. Ardından her kuyucuğa 200 µl %0.2’lik kristal viyole solüsyonu eklendi ve pleytler 45 dakika oda sıcaklığında bekletildi. Süre sonunda kristal viyole uzaklaştırıldı; pleytler üç kez dH2O ile yıkanıp kurutuldu. Ardından her kuyucuğa 200 µl %96 etanol ilave edildi. Çözünmüş solüsyondan 100 µl alınarak yeni bir pleyte aktarıldı.
Örneklerin absorbansı 590 nm dalga boyunda, mikroplaka okuyucu spektrofotometre (BioTek ELx800, BioTek Instruments, ABD) ile ölçüldü. Çalışmada, A. baumannii ATCC 19606 suşu pozitif kontrol olarak kullanıldı. Deney üç tekrar halinde gerçekleştirildi. Optik dansite sınır değeri (ODc), negatif kontrolün ortalama OD değerine 3 standart sapmanın (SS) eklenmesiyle hesaplandı:
ODc = negatif kontrolün ortalama OD’si + (3 × SS)
Sonuçlar optik dansite değerlerine göre; güçlü biyofilm oluşumu (OD > 4 × ODc), orta düzeyde biyofilm oluşumu (2 × ODc < OD ≤ 4 × ODc), zayıf biyofilm oluşumu (ODc < OD ≤ 2 × ODc) ve biyofilm oluşumu olmayan (OD ≤ ODc) olarak sınıflandırıldı (13).
Virülans Genlerinin Araştırılması
İzolatlardan total DNA izolasyonu kaynatma yöntemi ile gerçekleştirildi. Elde edilen total DNA örnekleri çalışma boyunca hedeflenen genlerin çoğaltılmasında kullanıldı (18).
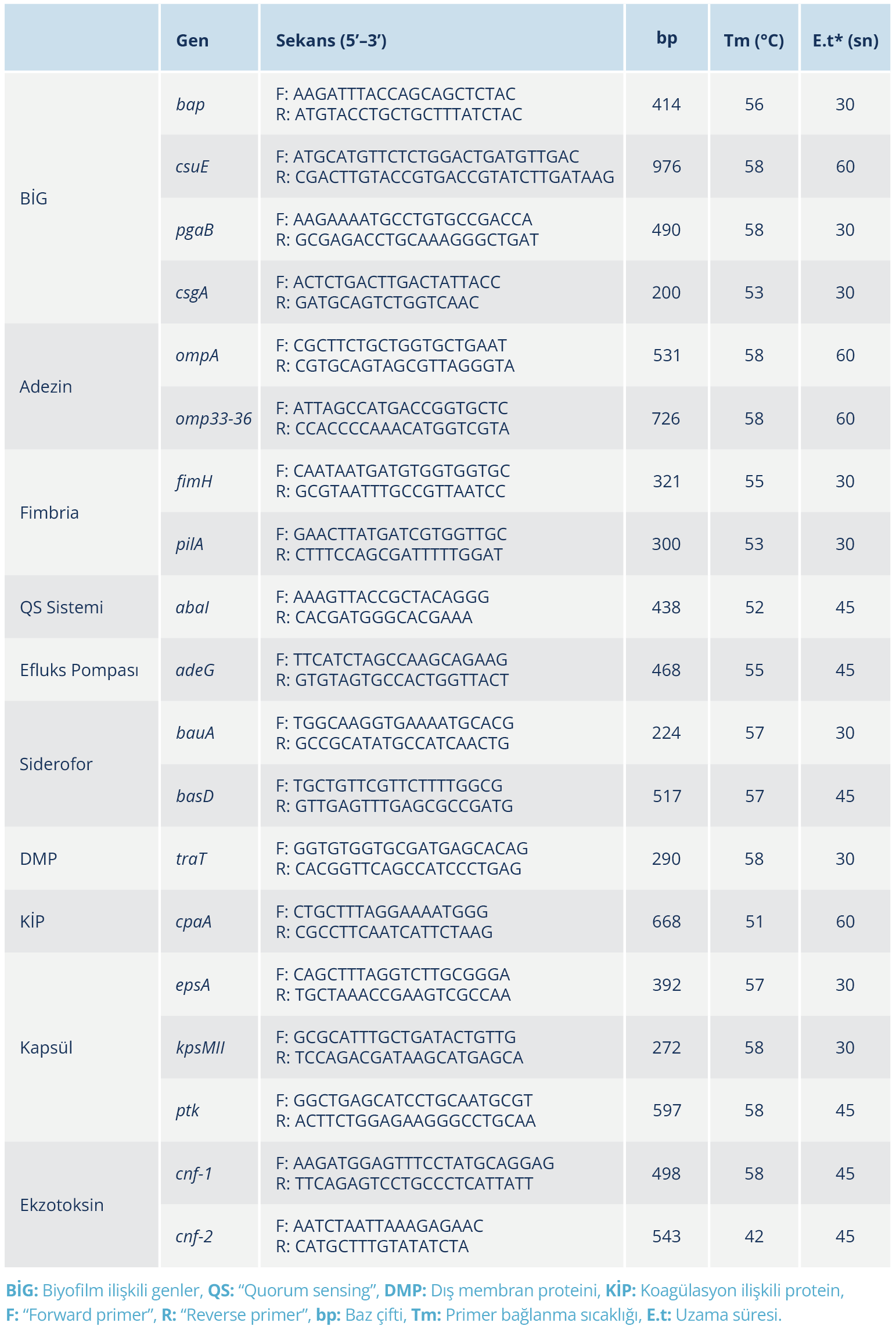
İzolatlarda; bap, ompA, csuE, fimH, pgaB, csgA, abaI, adeG, pilA, bauA, omp33-36, traT, basD, cpaA, epsA, cnf-1, cnf-2, kpsMII ve ptk virülans genlerinin varlığı polimeraz zincir reaksiyonu (PCR) yöntemiyle tespit edildi. Genlerin çoğaltılmasında kullanılan primer dizileri Tablo 1’de sunuldu. PCR reaksiyonları toplam 25 µl son hacimde hazırlandı. Her bir reaksiyon için 12.5 µl 2X PCR Master Mix (Ampliqon, Odense M, Danimarka), 10 pmol/µl konsantrasyonda her bir spesifik primer çiftinden 0.5 µl ve kaynatma yöntemiyle izole edilen total DNA’dan 5 µl eklendi; son hacim dH₂O ile 25 µl’ye tamamlandı.
PCR amplifikasyonu şu koşullarda gerçekleştirildi: başlangıç denatürasyonu 95 °C’de 3 dakika; ardından 35 döngü boyunca 95 °C’de 45 saniye denatürasyon, her gen için belirlenen bağlanma (annealing) sıcaklığında 45 saniye ve 72 °C’de hedef PCR ürününün uzunluğuna göre ayarlanan uzama süresi; son olarak 72 °C’de 5 dakika son uzama basamağı uygulandı (Tablo 1). Ardından amplifiye olan PCR ürünleri etidyum bromür içeren %1’lik agaroz jel elektroforezinde 100 V’da 1 saat süreyle yürütüldü. Jel görüntüleri UV ışığı altında değerlendirildi. Bantların varlığı ve beklenen moleküler ağırlıkları dikkate alınarak incelenen virülans genlerinin izolatlarda bulunup bulunmadığı belirlendi.
BULGULAR
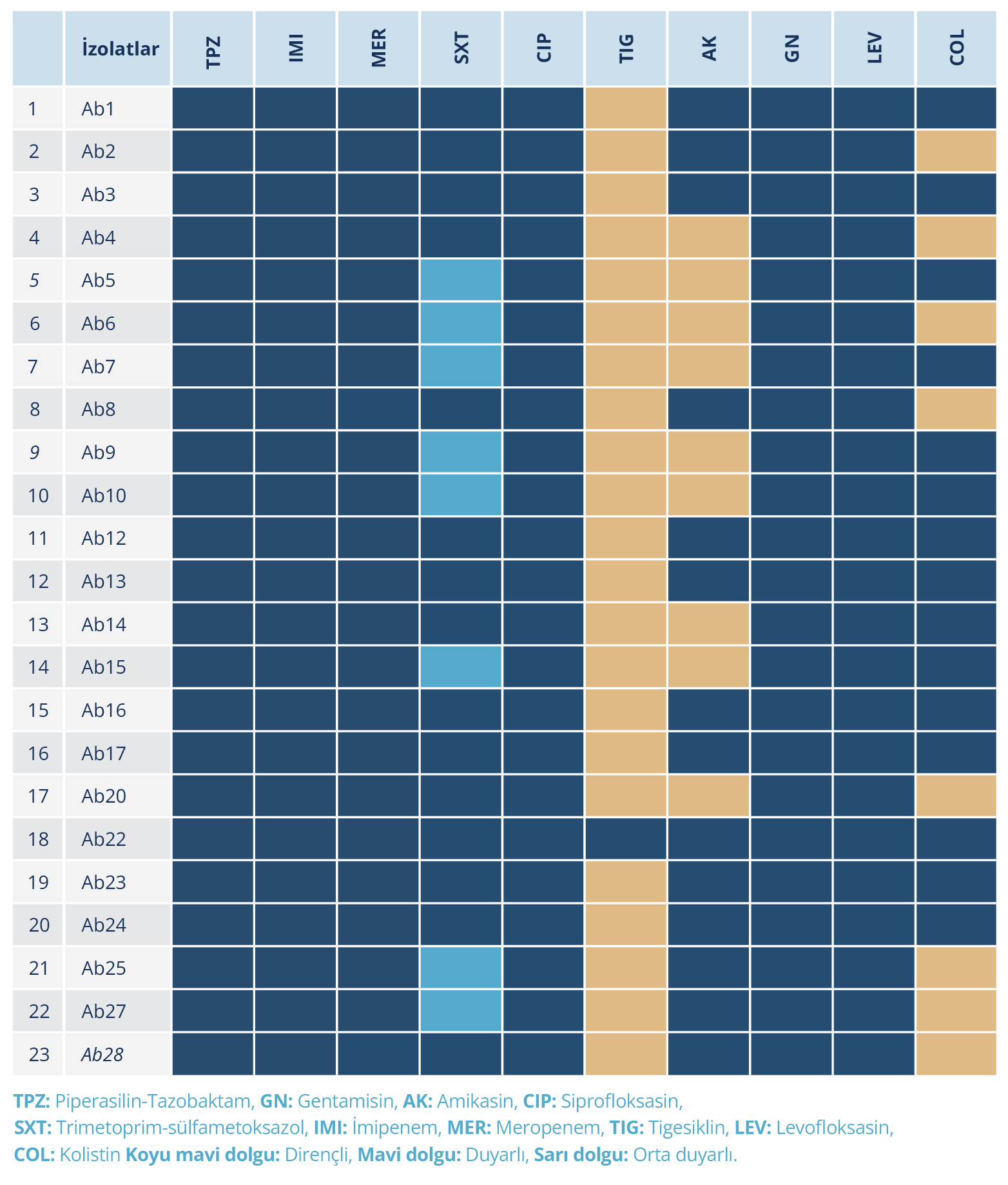
Çalışmaya toplam 23 VİP etkeni A. baumannii izolatı dahil edildi. İzolatlar 23 farklı hastadan elde edildi. İzolatların antibiyotik direnç dağılımı değerlendirildiğinde; piperasilin-tazobaktam, imipenem, meropenem, siprofloksasin, gentamisin, levofloksasine karşı direnç oranı %100 olarak saptandı. Trimetoprim-sülfametoksazol ve kolistine karşı direnç oranı ise %65 idi. Tüm izolatlar çoklu ilaç direnci gösteriyordu (Tablo 2).
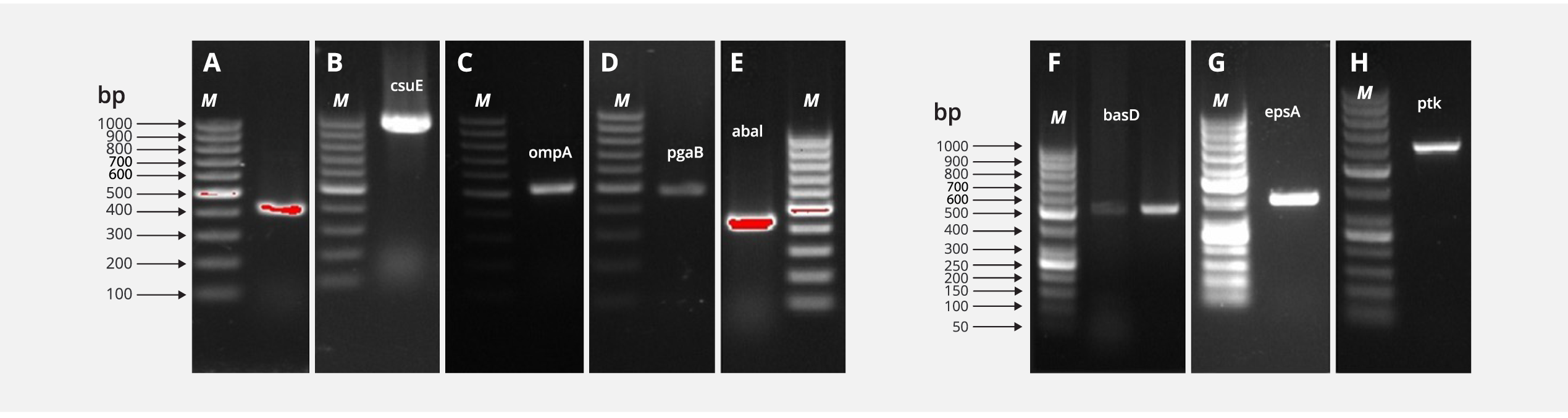
Şekil 1. Acinetobacter baumannii İzolatlarında Virülans Genlerinin Agaroz Jel Elektroforez Görüntüsü
A: bap geni (414 bp), B: csuE geni (976 bp), C: ompA geni (531 bp), D: pgaB geni (490 bp), E: abaI geni (438 bp), F: basD geni (517 bp), G: epsA geni (392 bp), H: ptk geni (597 bp), M: DNA merdiveni [F, G ve H panellerinde Thermo Scientific™ GeneRuler 50 bp DNA Merdiveni; A, B, C, D ve E panellerinde Norgen Biotek PCRSizer 100 bp DNA Merdiveni].
Tablo 3).
Fenotipik değerlendirme sonucunda, biyofilm oluşturma özelliği 23 (%100) izolatın tamamında güçlü düzeyde tespit edildi (Tablo 2). Tüm izolatlarda biyofilm oluşumu ile ilişkili bap, ompA, csuE ve pgaB genleri pozitif iken fimH ve csgA genleri tespit edilmedi (Resim 1, Tablo 3).
İRDELEME
Toplumdan ve özellikle hastanelerden izole edilen Gram-negatif bakterilerde, geniş spektrumlu antibiyotiklerin kullanımının artmasına paralel olarak antibakteriyel ajanlara karşı gelişen direnç, dünya genelinde önemli bir halk sağlığı sorunu hâline gelmiştir. Özellikle çoklu ilaç direnci ve yaygın ilaç direnci (extensively drug resistant, XDR) bulunan A. baumannii infeksiyonlarının tedavisinde yaşanan güçlükler giderek artmaktadır. Bu çalışmada yer alan A. baumannii izolatlarının tamamının klinikte yaygın olarak kullanılan antibiyotiklerin çoğuna dirençli bulunması, literatürde bildirilen verilerle uyumludur (12,14). Buna karşın kolistin direncinin yüksek bulunması literatürden farklılık göstermektedir; bu durum, hastanemizde A. baumannii infeksiyonlarının tedavisinde zorluk riski oluşturabileceğini düşündürmektedir.
Hücreler arası iletişim sisteminde yer alan genlerden biri olan abaI geninin, sinyal molekülü N- AHL sentezini sağlayarak bakteriyel davranışları ve patojeniteyi düzenler. Literatürde yer alan birçok çalışma, abaI, abaR ve abaM genlerini içeren QS sisteminin A. baumannii patojenitesi üzerindeki etkisini incelemiş ve büyüme, hareketlilik, virülans, biyofilm oluşumu ve antibiyotik duyarlılığı ile ilişkili olduğunu ortaya koymuştur (19). Ayrıca abaI delesyonunun virülansı, enerji üretimini, biyofilm oluşumunu ve antibiyotiklere karşı olan direnci azalttığı bildirilmiştir (20). Bu çalışmada da literatürle uyumlu olarak biyofilm oluşturma kapasitesi ve virülans düzeyi yüksek bulunan tüm izolatlarda abaI geni pozitif idi.
Çoklu ilaç efluks pompalarının çalışmasından sorumlu “Resistance-Nodulation-Division” (RND) ailesinin üç üyesi olan adeABC, adeFGH ve adeIJK’nın artan ekspresyonu, çoklu ilaç direnci ve virülans ile ilişkilendirilmiştir (6). İnsanlardan izole edilen A. baumannii suşlarında adeF, adeG ve adeH efluks pompası genlerinin yüksek prevalansa sahip olduğunu bildiren çalışmalar bulunmaktadır (21). AdeFGH’nin aşırı ekspresyonunun, biyofilm oluşumu sırasında AHL’lerin sentezini ve taşınmasını artırdığı; ayrıca adeFGH ve abaI genlerinin birlikte yukarı regülasyonunun A. baumannii tarafından biyofilm gelişimi üzerinde potansiyel bir etkiye sahip olduğu gösterilmiştir (21). Buna karşılık bazı çalışmalarda, RND tipi efluks pompası genleri olan adeB, adeG ve adeJ’nin bir veya daha fazlasının ekspresyonu ile biyofilm oluşumu arasında negatif bir korelasyon olduğu bildirilmiştir (22). Negatif korelasyon gözlemi, Csu pili’deki azalma ve demir edinimi ve hareketliliğinde rol oynayan genlerin aşağı regülasyonu gibi bakteri membranında efluks pompası aşırı ekspresyonu ile ilişkili değişikliklerin varlığı ile açıklanmıştır (22). Bu çalışmada RND ailesinden adeG geni incelenmiş olup izolatların hiçbirinde bu gen tespit edilmedi. Bu bulgu, bazı çalışmalarda bildirilen negatif korelasyonla uyumlu olabilir. Ayrıca tüm izolatlarda güçlü biyofilm oluşumunun saptanması ve pili ile ilişkili csuE ve demir edinimi ile ilişkili basD genlerinin pozitif bulunması da literatürde bildirilen verilerle uyumludur.
Demir edinimi, A. baumannii patogenezinin temel bileşenlerinden biridir; bakterinin hayatta kalmasını sağlar ve konakta infeksiyona neden olur. bauA geni, demir kazanımında rol oynayan bir siderofor olan ferrik asinetobaktinin bağlanması ve hücre içine alınmasından sorumlu proteini kodlamakta ve aynı zamanda biyofilm oluşumuna katkıda bulunmaktadır. Bu mekanizma, bakterinin konaktan demir emmesini sağlayarak hayatta kalmasını sağlar. basD geni ise asinetobaktin biyosentezinde rol oynayan bir enzimi kodlar. Asinetobaktin, demir ediniminde kritik öneme sahip olup basD aktivitesi bu sideroforun üretimi için gereklidir. Bu durum, bakterinin virülansını ve antibiyotik direncini artıran bir avantaj sağlamaktadır. Literatürde bauA ve basD pozitif suşlarda antibiyotik direnci prevalansının, duyarlı izolatlara kıyasla anlamlı derecede daha yüksek olduğu bildirilmiştir (23). Çalışmamızda bauA geni izolatların hiçbirinde tespit edilemezken, basD geni tüm izolatlarda pozitif bulundu. Bu bulgu, etkenin hayatta kalmak için gerekli demir edinimini basD geni aracılığı ile yaptığını düşündürmektedir.
Çalışmamızda, A. baumannii’nin sitotoksisitesi ile konak hücreye adezyon ve invazyondan sorumlu iki dış membran proteiniyle ilişkili ompA ve omp33-36 genleri incelendi (24); ompA geni tüm izolatlarda tespit edilirken omp33-36 geni izolatların hiçbirinde tespit edilmedi. Bu durum bakterinin konak hücreye adezyon ve invazyon süreçlerinde ompA aracılı mekanizmaları kullandığını düşündürmektedir.
Kapsüler polisakkarit, kompleman aktivitesine ve konak fagositozuna direnç göstererek patojenitede önemli rol oynar. Konak bağışıklık yanıtından kaçış ve serumda çoğalma, kapsül biyosentezinde rol oynayan ptk ve epsA genleri tarafından kolaylaştırılmaktadır (24). Bu genler, A. baumanii’de kapsül polimerizasyonu ve montajı için gereklidir ve bu da organizmanın konak bağışıklık mekanizmalarına direnmesine yardımcı olur. Abdulsadah ve arkadaşlarının çalışmasında, çeşitli kültürlerden izole edilen çoklu ilaç direnci gösteren A. baumannii suşlarında ompA geni %90 pozitif bulunurken, epsA %37, ptk %21 oranında bildirilmiştir (25). Benzer şekilde başka bir çalışmada, izolatların tamamında bap ve ompA genleri bulunurken epsA geni %25’inde ptk ise %50’sinde pozitif bulunmuştur (26). Bizim çalışmamızda da literatürle uyumlu şekilde epsA geni izolatların %16.6’sında, ptk geni ise %54.2’sinde pozitifti. İzolatlarımızda bu genlerin görece düşük sıklıkta bulunmasının, biyofilm oluşumu ile ilişkili ompA ve bap gibi genlerin yüksek oranlarda saptanmış olmasıyla ilişkili olabileceği düşünülmektedir.
Acinetobacter baumannii, biyofilm üretimine yönelik yüksek kapasitesiyle tanınmaktadır (13). Çalışmamızda da literatürle uyumlu olarak izolatların tamamında güçlü biyofilm oluşumu tespit edildi. Birçok çalışmada, biyofilm oluşumu ile virülans arasında pozitif bir ilişki olduğu bildirilmiştir (13, 27). Acinetobacter baumannii virülansında önemli rol oynayan bap, csuE, ompA, fimH, pgaB ve csgA gibi birçok genin varlığı, bakterinin biyofilm oluşturma kapasitesini artırmaktadır. Bu genlerin bazıları biyofilm oluşturmayan izolatlarda da tespit edilmekle birlikte, görülme sıklıklarının ve ekspresyon düzeylerinin biyofilm oluşturan izolatlarda daha yüksek olduğu bildirilmiştir (27).
Biyofilm yapısının güçlü olduğu A. baumannii izolatlarının incelendiği çalışmalarda bap geninin varlığı sıklıkla gösterilmiştir (28). Çalışmamızda da izolatların tamamında bap geni tespit edildi. Bu gen ile biyofilm oluşumu arasındaki ilişkinin incelendiği bir çalışmada; bap pozitif A. baumannii izolatlarının biyofilm oluşturma kapasitelerinin, bap geni taşımayan izolatlara göre önemli ölçüde farklılık gösterdiği bildirilmiştir (28).
Acinetobacter baumannii’nin biyofilm oluşturmasında, csuA/BABCDE operon sistemi aracılığıyla üretilen pilusun abiyotik yüzeylere tutunmak için gerekli olduğu gösterilmiş ve bu sistemin A. baumannii izolatlarında sıklıkla bulunduğu bildirilmiştir (13,29). Çalışmamızda izolatların tamamında csuE geninin varlığı tespit edildi. İzolatların tamamında güçlü biyofilm oluşumunun tespit edilmesi ve pilA ile fimH genlerinin izolatların hiçbirinde görülmemesi, biyofilm oluşumu ve yüzeye tutunmada csuE geninin rolünü destekler niteliktedir.
Yapılan çalışmalarda A. baumannii izolatlarında ompA geninin yüksek oranlarda bulunduğu gösterilmiştir (13). Çalışmamızda da izolatların tamamında ompA geni tespit edildi; izolatların tamamının çoklu ilaç direnci göstermesi, güçlü biyofilm oluşumu ve yüksek oranda ompA geni varlığı, ompA’nin infeksiyon gelişimi ve antibiyotik direnci ile ilişkili olabileceğini düşündürmektedir.
Yapılan çalışmalarda pgaABCD gen kümesinin güçlü biyofilm oluşumunda rol oynadığı, etkenlerin direnç potansiyelini artırarak çoklu ilaç direnci gelişimine katkı sağladığı, virülansı artırdığı ve pgaB genini taşıyan izolatların daha yüksek öldürücülük gösterdiği bildirilmiştir (30). Çalışmamızda da izolatların hepsinde pgaB geni tespit edilmiş olup çoklu ilaç direnci varlığı da düşünüldüğünde bulgularımız literatürle uyumludur.
Sonuç olarak; bu çalışmada VİP etkeni olan ve çoklu ilaç direnci gösteren A. baumannii izolatlarında güçlü biyofilm oluşumunun saptanması ve biyofilm oluşumu ile ilişkili bap, csuE, ompA ve pgaB genlerinin tüm izolatlarda pozitif bulunması, bu izolatlarda virülans ile biyofilm oluşumu arasında olası bir ilişki bulunduğunu düşündürmektedir. Buna karşılık fimH ve csgA genlerinin izolatlarda tespit edilmemiş olması, bu izolatlarda biyofilm oluşumunda belirleyici olmayabileceğine işaret etmektedir. Ayrıca VİP etkeni A. baumannii izolatlarında güçlü biyofilm oluşumunun varlığı ile birlikte abaI, basD, epsA ve ptk gibi bazı virülans genlerinin varlığı, bu genlerin biyofilm oluşumu ve antibiyotiklere karşı direnç gelişimiyle ilişkili olabileceğini desteklemektedir. Yüksek biyofilm oluşturma kapasitesi ve virülans genlerinin varlığı nedeniyle A. baumannii nozokomiyal infeksiyonlarda önemli bir tehdit oluşturmaktadır. Bu bağlamda özellikle bap, csuE, ompA, pgaB, abaI ve basD genlerinin baskılanmasına, dolayısıyla biyofilm oluşumu ve virülansın engellenmesine yönelik ileri çalışmaların, A. baumannii infeksiyonlarıyla mücadelede önemli katkılar sağlayabileceği düşünülmektedir.
Hasta Onamı
Veriler retrospektif olarak değerlendirildiği için hasta onamı alınmamıştır.
Etik Kurul Kararı
Çalışma için Kırşehir Ahi Evran Üniversitesi Klinik Araştırmalar Etik Kurulu’ndan 06 Aralık 2022 tarih ve 2022/22-190 karar numarasıyla onay alınmıştır.
Danışman Değerlendirmesi
Bağımsız dış danışman
Yazar Katkıları
Fikir/Kavram – B.Ç., E.S., L.H.; Tasarım – B.Ç., E.S., L.H.; Denetleme – E.S.; Veri Toplama ve/veya İşleme – B.Ç., E.S., L.H.; Analiz ve/veya Yorum – B.Ç., E.S., L.H.; Literatür Taraması – B.Ç., Makale Yazımı – B.Ç., L.H., E.S.; Eleştirel İnceleme – E.S.
Çıkar Çatışması
Yazarlar herhangi bir çıkar çatışması bildirmemiştir.
Finansal Destek
Yazar finansal destek beyan etmemiştir.
Yapay Zekâ Kullanım Beyanı
Çalışmanın tüm bilimsel içeriği, veri analizi ve sonuçları yazarlara aittir. Araştırmanın tasarımı, veri analizi ve yorumlanmasında yapay zekâ destekli araçlar kullanılmamıştır.
Referanslar
- French GL. Antimicrobial resistance in hospital flora and nosocomial infections. In: Mayhall CG, editor. Hospital epidemiology and infection control. 4th ed. New York: Lippincott Williams & Wilkins; 1999. p. 1243–64.
- Shlaes DM, Bradford PA. Antibiotics-from there to where?: How the antibiotic miracle is threatened by resistance and a broken market and what we can do about it. Pathog Immun. 2018;3(1):19–43. [CrossRef]
- Freire MP, de Oliveira Garcia D, Garcia CP, Campagnari Bueno MF, Camargo CH, Kono Magri ASG, et al. Bloodstream infection caused by extensively drug-resistant Acinetobacter baumannii in cancer patients: high mortality associated with delayed treatment rather than with the degree of neutropenia. Clin Microbiol Infect. 2016;22(4):352–8. [CrossRef]
- Skariyachan S, Taskeen N, Ganta M, Venkata Krishna B. Recent perspectives on the virulent factors and treatment options for multidrug-resistant Acinetobacter baumannii. Crit Rev Microbiol. 2019;45(3):315–33. [CrossRef]
- Harding CM, Tracy EN, Carruthers MD, Rather PN, Actis LA, Munson RS Jr. Acinetobacter baumannii strain M2 produces type IV pili which play a role in natural transformation and twitching motility but not surface-associated motility. mBio. 2013;4(4):e00360–13. [CrossRef]
- Eze EC, Chenia HY, El Zowalaty ME. Acinetobacter baumannii biofilms: effects of physicochemical factors, virulence, antibiotic resistance determinants, gene regulation, and future antimicrobial treatments. Infect Drug Resist. 2018;11:2277–99. [CrossRef]
- Liu C, Chang Y, Xu Y, Luo Y, Wu L, Mei Z, et al. Distribution of virulence-associated genes and antimicrobial susceptibility in clinical Acinetobacter baumannii isolates. Oncotarget. 2018;9(31):21663–73. [CrossRef]
- Montenegro MA, Bitter-Suermann D, Timmis JK, Agüero ME, Cabello FC, Sanyal SC, et al. traT gene sequences, serum resistance and pathogenicity-related factors in clinical isolates of Escherichia coli and other Gram-negative bacteria. J Gen Microbiol. 1985;131(6):1511–21. [CrossRef]
- Zhao X, Yu Z, Ding T. Quorum-sensing regulation of antimicrobial resistance in bacteria. Microorganisms. 2020;8(3):425. [CrossRef]
- Russo TA, Luke NR, Beanan JM, Olson R, Sauberan SL, MacDonald U, et al. The K1 capsular polysaccharide of Acinetobacter baumannii strain 307-0294 is a major virulence factor. Infect Immun. 2010;78(9):3993–4000. [CrossRef]
- Tilley D, Law R, Warren S, Samis JA, Kumar A. CpaA a novel protease from Acinetobacter baumannii clinical isolates deregulates blood coagulation. FEMS Microbiol Lett. 2014;356(1):53–61. [CrossRef]
- Zer Y, Akboru M, Sağlam M, Manay AB. [Investigation of virulence genes of nosocomial Acinetobacter baumannii isolates]. Turk Mikrobiyol Cemiy Derg. 2024;54(1):32–9. Turkish. [CrossRef]
- Gürpınar Ö, Ergin A, Zarakolu P, Köseoğlu E. [Biofilm production and presence of virulence genes in invasive and non-invasive Acinetobacter baumannii isolates]. Flora. 2021;26(4):720–6. Turkish. [CrossRef]
- Sung JY. Molecular characterization and antimicrobial susceptibility of biofilm-forming Acinetobacter baumannii clinical isolates from Daejeon, Korea. Korean J Clin Lab Sci. 2018;50(2):100–9. [CrossRef]
- Qi L, Li H, Zhang C, Liang B, Li J, Wang L, et al. Relationship between antibiotic resistance, biofilm formation, and biofilm-specific resistance in Acinetobacter baumannii. Front Microbiol. 2016;7:483. [CrossRef]
- Wright MS, Jacobs MR, Bonomo RA, Adams MD. Transcriptome remodeling of Acinetobacter baumannii during infection and treatment. mBio. 2017;8(2):e02193–16. [CrossRef]
- Wu L, Wu L, Wang T, Zou Z, Jiang X, Yin Q, et al. Use of magnetic nanoparticles for the detection of multidrug-resistant Acinetobacter baumannii. Nanosci Nanotechnol Lett. 2018;10(8):1165–71. [CrossRef]
- Ausubel FM, Kingston RE, Moore DD, Seidman JG, Smith JA, Struhl K, editors. Current protocols in molecular biology. 2nd ed. New York: John Wiley & Sons; 1995.
- Xiong L, Yi F, Yu Q, Huang X, Ao K, Wang Y, et al. Transcriptomic analysis reveals the regulatory role of quorum sensing in the Acinetobacter baumannii ATCC 19606 via RNA-seq. BMC Microbiol. 2022;22(1):198. [CrossRef]
- Tang J, Chen Y, Wang X, Ding Y, Sun X, Ni Z. Contribution of the AbaI/AbaR quorum sensing system to resistance and virulence of Acinetobacter baumannii clinical strains. Infect Drug Resist. 2020;13:4273–81. [CrossRef]
- He X, Lu F, Yuan F, Jiang D, Zhao P, Zhu J, et al. Biofilm formation caused by clinical Acinetobacter baumannii isolates is associated with overexpression of the AdeFGH efflux pump. Antimicrob Agents Chemother. 2015;59(8):4817–25. [CrossRef]
- Abd El-Rahman OA, Rasslan F, Hassan SS, Ashour HM, Wasfi R. The RND efflux pump gene expression in the biofilm formation of Acinetobacter baumannii. Antibiotics (Basel). 2023;12(2):419. [CrossRef]
- Li J, Yu T, Luo Y, Peng JY, Li YJ, Tao XY, et al. Characterization of carbapenem-resistant hypervirulent Acinetobacter baumannii strains isolated from hospitalized patients in the mid-south region of China. BMC Microbiol. 2020;20(1):281. [CrossRef]
- Mendes SG, Combo SI, Allain T, Domingues S, Buret AG, Da Silva GJ. Co-regulation of biofilm formation and antimicrobial resistance in Acinetobacter baumannii: from mechanisms to therapeutic strategies. Eur J Clin Microbiol Infect Dis. 2023;42(12):1405–23. [CrossRef]
- Abdulsadah BG, Hadi ZJ. First identification of phospholipase C (PlcH) gene in multi-drug resistant Acinetobacter baumannii isolated from clinical specimens in Iraq. Med Sci J Adv Res. 2024;5(3).
- Fiji E, Anandharaj B, Jijo GV. Molecular determination of virulence factor genes of Acinetobacter baumannii isolates from clinical specimens. Int J Life Sci Pharma Res. 2022;12(3):L150–8. [CrossRef]
- Smitran A, Lukovic B, Bozic L, Jelic D, Jovicevic M, Kabic J, et al. Carbapenem-resistant Acinetobacter baumannii: biofilm-associated genes, biofilm-eradication potential of disinfectants, and biofilm-inhibitory effects of selenium nanoparticles. Microorganisms. 2023;11(1):171. [CrossRef]
- Fallah A, Rezaee MA, Hasani A, Barhaghi MHS, Kafil HS. Frequency of bap and cpaA virulence genes in drug resistant clinical isolates of Acinetobacter baumannii and their role in biofilm formation. Iran J Basic Med Sci. 2017;20(8):849–55. [CrossRef]
- Zeighami H, Valadkhani F, Shapouri R, Samadi E, Haghi F. Virulence characteristics of multidrug resistant biofilm forming Acinetobacter baumannii isolated from intensive care unit patients. BMC Infect Dis. 2019;19(1):629. [CrossRef]
- Reheama EE, Ibrahim SA. Prevalence of pgaABCD locus in biofilm formation Acinetobacter baumannii. Rev Res Med Microbiol. 2024;35(3):151–9.