En Çok Okunanlar
Özet
Amaç: Bu çalışmada, HIV infeksiyonu açısından düşük endemik bir bölgede yaşayan gebelerde yalancı pozitif HIV test oranını belirlemeyi ve gereksiz antiretroviral profilaksiyi önleyebilmek için uygun stratejiler geliştirmeyi amaçladık.
Yöntemler: Retrospektif olarak gerçekleştirilen çalışmaya, 01 Ocak 2018 – 31 Aralık 2022 tarihleri arasında Sağlık Bilimleri Üniversitesi (SBÜ) Gazi Yaşargil Eğitim ve Araştırma Hastanesi Kadın Hastalıkları ve Doğum Kliniği’ne başvuran ve ELISA HIV Ag/Ab testi yapılan 18 yaş ve üzeri toplam 115 217 kadın dahil edildi. HIV Ag/Ab testleri, dördüncü nesil HIV Ag/Ab Combo kemilüminesans mikropartikül immünoassay yöntemi ile çalışıldı; pozitif sonuçlar referans laboratuvarda doğrulandı.
Bulgular: HIV Ag/Ab ELISA testi pozitiflik oranı gebelerde %0.18 (91/49.560), gebe olmayan kadınlarda %0.02 (14/65.657) olarak bulundu. Doğrulama testleri ve HIV-RNA testlerinde ise 2 (%0.004) gebe ve 3 (%0.005) gebe olmayan kadın pozitif saptandı. Gebelerde %0.18 (89/49.560), gebe olmayan kadınlarda %0.02 (11/65.657) oranında yalancı pozitif HIV testine rastlandı; bu fark istatistiksel olarak anlamlı bulundu (p=0.016). Gerçek HIV pozitifliği olan gebelerde HIV Ag/Ab S/Co titre ortalamasının anlamlı derecede yüksek olduğu gözlendi.
Sonuç: Gebe kadınlarda HIV Ag/Ab ELISA testlerinde yalancı pozitiflik oranı gebe olmayan kadınlara göre daha yüksektir. Gerçek HIV pozitifliği olan gebelerde ise yüksek HIV Ag/Ab S/Co titre değerleri dikkati çekmektedir. Yalancı pozitiflik oranlarının yüksekliği nedeniyle, gebelerde HIV tanısının antiretroviral tedaviye başlanmadan önce en kısa sürede doğrulanması önerilmektedir.
GİRİŞ
İnsan immün yetmezlik virusu (HIV), Lentivirinae alt ailesine ait zarflı bir retrovirustur; bağışıklık sistemini baskılayarak fırsatçı infeksiyonların gelişmesine yol açar ve kazanılmış immün yetmezlik sendromu (Acquired Immunodeficiency Syndrome, AIDS) tablosuyla karakterize kronik bir hastalığa neden olur (1). HIV ile infekte annelerden bebeklerine gebelik sürecinde, doğum sırasında veya sonrasında emzirmeyle bulaşma olabilmektedir (2). Horizontal veya perinatal geçiş olarak da adlandırılan anneden bebeğe HIV bulaşması, çocuk ölümlerinin önemli nedenlerinden biridir ve dünya genelinde yaklaşık iki milyon çocuğun HIV ile infekte olduğu tahmin edilmektedir (3). Gebelik sırasında alınan antiretroviral tedavi (ART), HIV’in horizontal bulaşmasını önleyebilmektedir; tedavi almayan gebelerden yenidoğanlara bulaşma oranı %15 ile %45 arasında değişmektedir (4).
Türkiye’de HIV prevalansı hâlen düşük olmakla birlikte (%0.1–0.3) son beş yıldır olgu sayıları hızla artmakta ve özellikle genç nüfusta infeksiyon oranları yükselmektedir (5). Çalışmamızın gerçekleştirildiği Diyarbakır ilinde, sağlıklı kan bağışçılarında yapılan seroprevalans çalışmalarında HIV seroprevalans oranı ülke ortalamasından düşük seyretmekle birlikte yıllar içerisinde artış göstermektedir (6,7). Türkiye’de kadın popülasyonunda HIV tanısı açısından gebelik taraması önemli bir fırsat olarak değerlendirilmektedir; HIV ile infekte kadınların %17’sinde gebelik taraması ile tanı konulduğu bildirilmiştir (8).
HIV infeksiyonunun laboratuvar tanısı, serolojik tarama testleriyle yapılmaktadır. Yüksek duyarlılığı nedeniyle hem HIV’e özgü antikorları hem de p24 antijenini eşzamanlı saptayan 4. nesil HIV Ag/Ab Combo kemilüminesans mikropartikül immünoassay testi tarama amacıyla tercih edilmektedir (9). Bununla birlikte HIV Ag/Ab ELISA testlerinde HIV ile ilişkili olmayan bazı proteinler HIV’e özgü antikorlar olarak tanımlanarak yalancı pozitif sonuçlara yol açabilmektedir. Bazı araştırmacılar alloantikorların gebelik, transfüzyon, transplantasyon ve otoimmün hastalıklarla ilişkili olarak artan yalancı pozitiflik oranlarından sorumlu olabileceğini ileri sürmektedir (10). Yalancı pozitiflik, özellikle HIV seroprevalansının düşük olduğu toplumlarda önemli bir endişe kaynağıdır; gebe kadınlar bu açıdan en yüksek risk grubunu oluşturmaktadır (11).
Bu çalışmada, HIV infeksiyonu açısından düşük endemik bir bölgede yaşayan gebelerde yalancı pozitif HIV test oranını belirlemeyi ve gereksiz antiretroviral profilaksiyi önleyebilmek için uygun stratejiler geliştirmeyi amaçladık.
YÖNTEMLER
Retrospektif olarak gerçekleştirilen çalışmaya, 01 Ocak 2018 – 31 Aralık 2022 tarihleri arasında Sağlık Bilimleri Üniversitesi (SBÜ) Gazi Yaşargil Eğitim ve Araştırma Hastanesi Kadın Hastalıkları ve Doğum Kliniği’ne başvuran ve ELISA HIV Ag/Ab testi yapılan 18 yaş ve üzeri toplam 115 217 kadın dahil edildi.
HIV-1/2 Ag/Ab testleri, üretici firma önerilerine uygun olarak ve dördüncü nesil HIV Ag/Ab Combo kemilüminesans mikropartikül immünoassay yöntemi kullanılarak (Architect i2000 SR; Abbott Laboratories, ABD) çalışıldı. En az iki örnekte HIV Ag/Ab S/Co (signal-to-cutoff) değeri ≥1 olan testler pozitif kabul edildi. Pozitif sonuçlar, T.C. Sağlık Bakanlığı Ulusal AIDS Doğrulama Merkezi’nde VIDAS HIV Duo Ultra (bioMérieux, Fransa) HIV-1/2 Ag/Ab ve HIV-1/2 antikor ayırt edici hızlı doğrulama testi (Geenius HIV-1/2 Supplemental Assay; Bio-Rad Laboraties, ABD) kitleri kullanılarak doğrulandı. Viral yük ölçümü için HIV-1 kantitatif gerçek zamanlı polimeraz zincir reaksiyonu (RT-PCR) GeneXpert Dx otomatize sistemi (Cepheid AB, ABD) kullanıldı.
Hastane veri tabanındaki aynı hastaya ait yalnızca bir HIV Ag/Ab ELISA testi pozitifliği çalışmaya dahil edilerek mükerrer hasta girişi önlendi. Antiretroviral tedavi almış ve HIV RNA negatif saptanan hastalar çalışma dışı bırakıldı.
Çalışma Sağlık Bilimleri Üniversitesi Gazi Yaşargil Eğitim ve Araştırma Hastanesi Klinik Araştırmalar Etik Kurulu tarafından 30 Eylül 2022 tarih ve 195 karar numarasıyla onaylandı.
İstatistiksel Analizler
Verilerin analizi, SPSS (Statistical Package for the Social Sciences) versiyon 18.0 programı (IBM Corp., Armonk, NY, ABD) ile yapıldı. Verilerin değerlendirilmesinde yüzde (%), aritmetik ortalama, standart sapma gibi tanımlayıcı istatistiksel yöntemler kullanıldı. Değişkenler arasındaki ilişkiler χ² testi ve Fisher kesin testi ile değerlendirildi. İstatistiksel anlamlılık sınırı p<0.05 olarak kabul edildi.
BULGULAR
Tablo 1. Akut Bruselloz ve KKKA Hastalarının Başvuru Anında Elde Edilen Biyokimyasal Parametrelerinin ROC Analizi
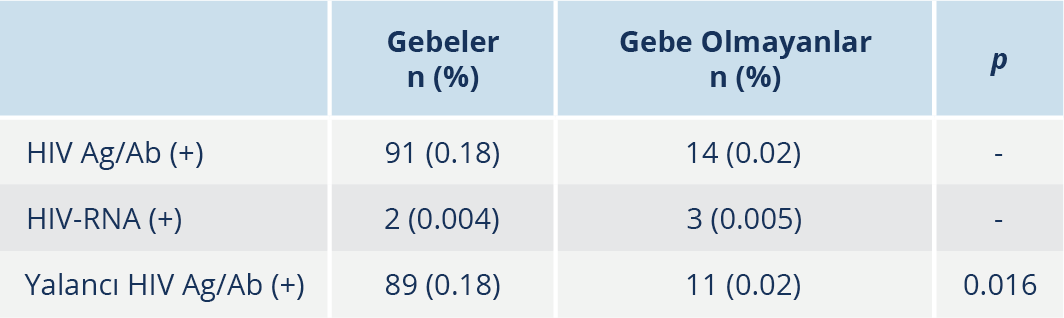
HIV Ag/Ab ELISA testi, gebelerde %0.18 (91/49.560) ve gebe olmayan kadınlarda %0.02 (14/65.657) oranında pozitifti; 2 (%0.004) gebede ve 3 (%0.005) gebe olmayan kadında ise doğrulama testleri ve HIV-RNA pozitif saptandı. Gebe kadınlarda %0.18 (89/49.560), gebe olmayan kadınlarda %0.02 (11/65.657) oranında yalancı pozitif HIV testine rastlandı ve aradaki fark, istatistiksel olarak anlamlı bulundu (p=0.016) (Tablo 1). HIV Ag/Ab ELISA testinin pozitif prediktif değeri (PPD) gebeler için %2.2, gebe olmayanlar için ise %21.4 olarak tespit edildi.
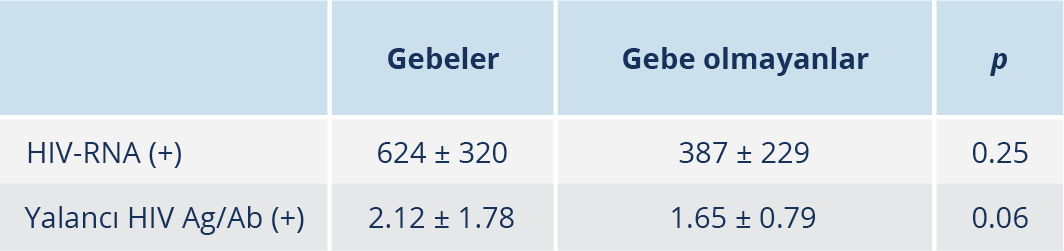
Doğrulama testleri ve HIV-RNA testi negatif olan, HIV Ag/Ab ELISA reaktif 89 gebe kadının yaş ortalaması 28.7 ± 6.6 (aralık 18–44) yıl, HIV Ag/Ab testi S/Co titre ortalaması ise 2.12 ± 1.78 (aralık 1.00–9.44) idi. HIV RNA pozitif saptanan gebenin yaş ortalaması 28.5 ± 2.1 (aralık 27–30) yıl, HIV Ag/Ab testi S/Co titre ortalaması ise 624 ± 320 (aralık 398–852) olarak belirlendi.
Gebe olmayan, HIV Ag/Ab ELISA reaktif testi, doğrulama testleri ve HIV-RNA testi negatif olan kadınların yaş ortalaması 43.5 ± 9.3 (aralık 29–64) yıl olup anti-HIV testi S/Co titre ortalaması 1.65 ± 0.79 (aralık 1.02–2.99) idi. HIV RNA pozitif saptanan ve gebe olmayan üç olguda yaş ortalaması 38 ± 2.0 (aralık 36–40) yıl, HIV Ag/Ab testi S/Co titre ortalaması 387 ± 229 (aralık 136–586) olarak belirlendi (Tablo 2).
İRDELEME
Bu çalışma, ülkemizde gebelik sırasında rutin olarak yapılan ELISA HIV tarama testlerinde yüksek oranda yalancı pozitiflikle karşılaşılabileceğini göstermektedir. Ayrıca, gebelerde referans laboratuvarda yapılan testlerle doğrulanan HIV kesin tanısı için yüksek HIV Ag/Ab testi S/Co titre ortalamasının gerekli olduğu görülmektedir. Bununla birlikte, T.C. Sağlık Bakanlığı HIV-AIDS Tanı-Tedavi Rehberi’ne göre titre değeri ister yüksek ister düşük olsun, HIV Ag/Ab testi pozitif saptanan annelerde doğrulama veya viral yük sonucu çıkana kadar bebeğe mümkün olan en kısa sürede mutlaka zidovudin (oral/paranteral) başlanması ve emzirmenin kesilmesi önerilmektedir (12).
Çalışmamızın yürütüldüğü merkezde HIV Ag/Ab testi pozitif çıkan numunelerin referans laboratuvara gönderilmesi nedeniyle yaşanan gecikmeler (ortalama 3–5 gün) yenidoğanlara gereksiz antiretroviral profilaksi başlanmasına yol açmaktadır. Ayrıca, gebelerde yalancı pozitif HIV testleri damgalanma, annenin bebeğinden ayrılması ve emzirememe gibi istenmeyen sonuçlara neden olabilmektedir.
ARCHITECT HIV Ag/Ab testinde S/Co değerinin 1–10 aralığında olduğu durumlarda yanlış pozitiflik oranının %100; S/Co değeri ≥30 olduğunda ise yanlış pozitiflik oranının sıfır olduğu ve S/Co değeri arttıkça yanlış pozitiflik oranının düştüğü yapılan çalışmalarda gösterilmiştir (13,14). Ayrıca, düşük HIV yaygınlığına sahip popülasyonlarda, HIV risk faktörü olmayan bireyler için doğum eylemi gibi akut durumlarda RNA testlerine erişim mümkün olmadığında, ARCHITECT HIV Ag/Ab testi S/Co değeri <5 olan ve doğrulama testi reaktif olmayan kombinasyonun, yalancı pozitiflik için yeterli kanıt sağlayabileceğine dair veriler bulunmaktadır (15).
Gebelikteki yalancı pozitif HIV testlerinin araştırıldığı İstanbul’da yapılan bir çalışmada, gebe kadınlarda %0.25, gebe olmayan kadınlarda ise %0.10 oranında yalancı pozitifliğe rastlanmış ve aradaki fark istatistiksel olarak anlamlı bulunmuştur. Çalışmamıza benzer şekilde, ülkemizde gebeliğin yalancı pozitif HIV testlerine yol açan bir risk faktörü olduğu sonucuna varılmıştır (16). Kuzey Kıbrıs Türk Cumhuriyeti’nde yakın zamanda yapılan retrospektif bir analiz çalışmasında da gebe kadınlarda (%0.3) yalancı pozitiflik oranı, gebe olmayanlara (%0.02) kıyasla anlamlı olarak daha yüksek bulunmuş; pozitif HIV ELISA test sonuçlarının ART’ye başlanmadan önce moleküler yöntemlerle doğrulanması gerektiği vurgulanmıştır (17).
Yalancı HIV tarama testi pozitifliklerinin yüksek oranda görülmesi, gereksiz ART kullanımına ve istenmeyen yan etkilere neden olmaktadır. Bu sorunun çözümü için bazı önerilerimiz bulunmaktadır. İlk olarak, tüm gebelerde doğum öncesi takiplerde HIV Ag/Ab ELISA testleri düzenli olarak çalışılmalı ve sonuçlar kayıt altına alınmalıdır. İkinci olarak, yüksek nüfus ve doğurganlık oranına sahip illere yakın referans laboratuvarlar kurularak, doğrulama testlerinin sonuç alma süreleri kısaltılmalıdır. Son olarak, gebelerde ve yenidoğanlarda antiretroviral profilaksi kararının verilmesinde HIV Ag/Ab S/Co titre değerinin dikkate alınacağı farklı bir algoritma oluşturulması faydalı olabilir.
Beş yıllık dönem için toplam hasta başvuru sayısına ait veri setine ulaşılamaması nedeniyle HIV Ag/Ab testi oranının hesaplanamaması çalışmamızın en önemli kısıtlılığıdır. Bir diğer önemli kısıtlılık ise verilerin retrospektif olarak hastane bilgi sisteminden alınması nedeniyle yalancı HIV testi sonucunda bebeklerin ne kadarına profilaksi başlandığı ve emzirmenin geciktirildiğine dair verilere ulaşılamamasıdır.
Sonuç olarak; gebelik sırasında yalancı pozitiflikle karşılaşılabileceğinden, pozitif HIV Ag/Ab ELISA sonuçlarının ART’ye başlanmadan önce en kısa sürede doğrulanması gerekmektedir. Ülkemizde 4. kuşak HIV Ag/Ab ELISA testleri kullanılmasına rağmen gebe kadınlarda, gebe olmayan kadınlara göre daha fazla yalancı HIV test pozitifliği görülmektedir. Ayrıca, gerçek HIV pozitifliği saptanan gebelerde yüksek HIV Ag/Ab S/Co değerleri dikkati çekmektedir.
Hasta Onamı
Veriler retrospektif olarak değerlendirildiği için hasta onamı alınmamıştır.
Etik Kurul Kararı
Çalışma Sağlık Bilimleri Üniversitesi Gazi Yaşargil Eğitim ve Araştırma Hastanesi Klinik Araştırmalar Etik Kurulu tarafından 30 Eylül 2022 tarih ve 195 karar numarasıyla onaylanmıştır.
Danışman Değerlendirmesi
Bağımsız dış danışman
Yazar Katkıları
Fikir/Kavram – M.B.; Tasarım – B.Y.E.; Denetleme – M.B.; Kaynak ve Fon Sağlama – S.E., B.Y.E.; Malzemeler/Hastalar – B.Y.E., S.E.; Veri Toplama ve/veya İşleme – M.B., S.E.; Analiz ve/veya Yorum – M.B.; Literatür Taraması – M.B., B.Y.E.; Makale Yazımı – M.B. Eleştirel İnceleme – M.B.
Çıkar Çatışması
Yazarlar herhangi bir çıkar çatışması bildirmemiştir.
Finansal Destek
Yazar finansal destek beyan etmemiştir.
Bilimsel Etkinlik
Bu çalışma, Türk Klinik Mikrobiyoloji ve İnfeksiyon Hastalıkları Derneği tarafından Antalya’da 13-16 Mart 2023 tarihleri arasında düzenlenen XXIII. Türk Klinik Mikrobiyoloji ve İnfeksiyon Hastalıkları Kongresi’nde bildiri olarak sunulmuştur.
Referanslar
- HIV/AIDS Tanı Tedavi Rehberi [Internet]. Ankara: T.C. Sağlık Bakanlığı Halk Sağlığı Genel Müdürlüğü; 2019. [erişim 3 Ekim 2024]. https://hsgm.saglik.gov.tr/depo/birimler/bulasici-hastaliklar-ve-erken-uyari-db/Dokumanlar/Rehberler/HIV-AIDS_Tani-Tedavi_Rehberi_2019.pdf
- Myburgh D, Rabie H, Slogrove AL, Edson C, Cotton MF, Dramowski A. Horizontal HIV transmission to children of HIV-uninfected mothers: A case series and review of the global literature. Int J Infect Dis. 2020;98:315-20. [CrossRef]
- Volmink J, Marais B. HIV: mother-to-child transmission. BMJ Clin Evid. 2008;2008:0909.
- Luzuriaga K. Mother-to-child transmission of HIV: a global perspective. Curr Infect Dis Rep. 2007;9(6):511-7. [CrossRef]
- Gökengin D, Oprea C, Uysal S, Begovac J. The growing HIV epidemic in Central Europe: a neglected issue? J Virus Erad. 2016;2(3):156-61. [CrossRef]
- Dayan S, Tekin A, Tekin R, et al. HBsAg, anti-HCV, anti-HIV 1/2 and syphilis seroprevalence in healthy volunteer blood donors in southeastern Anatolia. J Infect Dev Ctries. 2013;7(9):665-9. [CrossRef]
- Dayan S, Özekinci T, Bekçibaşi M, Deveci Ö. HBsAg, anti-HCV and anti-HIV seroprevalence among blood donors in Southeastern Anatolia, Turkey, 2011-2015. Infez Med. 2019;27(3):316-21.
- Yemisen M, Aydın OA, Gunduz A, et al. Epidemiological profile of naive HIV-1/AIDS patients in İstanbul: The largest case series from Turkey. Curr HIV Res. 2014;12(1):60-4. [CrossRef]
- Aslan FG, Altındiş M. Current Diagnostic Algorithm of HIV and Emerging Prevention Methods. Turk Mikrobiyol Cemiy Derg. 2017;47(2):47-60. [CrossRef]
- Doran TI, Parra E. False-positive and indeterminate human immunodeficiency virus test results in pregnant women. Arch Fam Med. 2000;9(9):924-9. [CrossRef]
- Wesolowski LG, Delaney KP, Lampe MA, Nesheim SR. False-positive human immunodeficiency virus enzyme immunoassay results in pregnant women. PLoS One. 2011;6(1):e16538. [CrossRef]
- T.C. Sağlık Bakanlığı, Halk Sağlığı Genel Müdürlüğü. HIV-AIDS Tanı ve Tedavi Rehberi. Ankara: Sağlık Bakanlığı; 2019 [erişim 3 Ekim 2024]. https://hsgm.saglik.gov.tr/depo/birimler/bulasici-hastaliklar-ve-erken-uyari-db/Dokumanlar/Rehberler/HIV-AIDS_Tani-Tedavi_Rehberi_2019.pdf
- Chacón L, Mateos ML, Holguín Á. Relevance of cutoff on a 4th generation ELISA performance in the false positive rate during HIV diagnostic in a low HIV prevalence setting. J Clin Virol. 2017;92:11-3. [CrossRef]
- Wang L, Xiao Y, Tian XD, Ruan JX, Chen W, Yu Y. HIV infection in Xi’an, China: epidemic characterization, risk factors to false positives and potential utility of the sample-to-cutoff index to identify true positives using Architect HIV Ag/Ab combo. Antimicrob Resist Infect Control. 2019;8:9. [CrossRef]
- Adhikari EH, Macias D, Gaffney D, et al. Diagnostic accuracy of fourth-generation ARCHITECT HIV Ag/Ab Combo assay and utility of signal-to-cutoff ratio to predict false-positive HIV tests in pregnancy. Am J Obstet Gynecol. 2018;219(4):408.e1-e9. [CrossRef]
- Sayan M, İnci A, Şanlı K. [Does anti-HIV positivity in pregnancy suggest the requirement of HIV prophylaxis for newborn?]. Klimik Derg. 2018;31(3):210-3. Turkish. [CrossRef]
- Güler E, Arıkan A, Abobakr M, Sayan M, Süer K, Şanlıdağ T. Positive anti-HIV ELISA results in pregnancy: Is it reliable? Infect Dis Obstet Gynecol. 2022;2022:1157793. [CrossRef]