En Çok Okunanlar
Özet
Amaç: Çalışmamızda; virolojik baskılanması sağlanmış, tedavi deneyimli ve tenofovir alafenamid/emtrisitabin/biktegravir (TAF/FTC/BIC) rejimine geçiş yapılmış hastaların, 48 haftalık takiplerinde tedavi etkinliğini gösteren virolojik ve immünolojik değişimlerin yanı sıra böbrek fonksiyonları ve lipid profillerindeki değişikliklerin değerlendirilmesi amaçlandı.
Yöntemler: Retrospektif ve tek merkezli olarak gerçekleştirilen çalışmaya, İnfeksiyon Hastalıkları Polikliniği’ne Ocak 2020-Aralık 2021 tarihleri arasında başvuran, 18 yaş ve üzeri, HIV ile yaşayan tedavi deneyimli bireyler dahil edildi. TAF/FTC/BIC rejimine geçiş yapılan HIV ile yaşayan bireylerin tedavi değişimi öncesi ve sonrası takip parametre sonuçları değerlendirildi.
Bulgular: Çalışmaya virolojik süpresyonu sağlanmış ve TAF/FTC/BIC rejimine geçiş yapılmış 77 hasta dahil edildi. Hastaların 71 (%92.2)’i erkek, ortanca yaş 42 (35-51.5) yıl ve hepatit B koinfeksiyonu olan hasta sayısı 5 (%6.4) idi. Hastaların antiretroviral tedavi (ART) alma süresi 6 (5-9) yıl olarak tespit edildi. Hastaların 60 (%77.9)’ında, tenofovir alafenamid/emtrisitabin/elvitegravir/kobisistat (TAF/FTC/EVG/Cob) içeren rejimden TAF/FTC/BIC’e geçiş yapılmıştı. Tedavi sonrası 24. ve 48. haftada viral yük saptanan hastaların ortanca HIV RNA düzeyleri sırasıyla 35 (27-77) kopya/ml ve 34 (24-49) kopya/ml olarak saptandı. Tedavi öncesi değerlerle karşılaştırıldığında; CD4+T lenfosit sayısında, CD4+ T lenfosit yüzdesinde ve CD4+/CD8+ oranında anlamlı düzeyde fark saptanmadı. TAF/FTC/BIC rejimine geçiş sonrası hastaların 19 (%24.7)’unda virolojik süpresyonun bozulduğu görüldü. Farklı düzeylerdeki virolojik yanıtlar değerlendirildiğinde; “tam olmayan virolojik yanıt” saptanmamakla birlikte, hastaların 2 (%2.6)’sinde virolojik geri tepme (“rebound”), 1 (%1.3)’inde virolojik yanıtsızlık, 8 (%10.4)’inde düşük düzeyli viremi ve 16 (%20.8)’sında virolojik sıçrama (“blip”) saptandı. TAF/FTC/BIC rejimine geçiş öncesi ve sonrası karşılaştırılan 77 hastanın 48. haftada bakılan glomerüler filtrasyon hızı (GFH) (101 ml/dk/1.73m² vs. 96 ml/dk/1.73m²; p=0.05) ve total kolesterol (199 mg/dl vs. 185 mg/dl; p=0.05) değerlerinde azalma istatistiksel anlamlılık sınırına yakındı. TAF/FTC/EVG/Cob rejiminden TAF/FTC/BIC’e geçişte ise GFH (101 ml/dk/1.73m² vs. 95 ml/dk/1.73m²; p=0.016) ve total kolesterol (205 mg/dl vs. 182 mg/dl; p<0.001) değerlerinde anlamlı azalma saptandı.
Sonuç: TAF/FTC/BIC rejimine geçiş öncesi virolojik süpresyon sağlanmış olsa da geçiş sonrası hastaların önemli bir oranında virolojik baskılanmanın bozulabileceği göz önünde bulundurulmalı ve bu hastalar detaylı sorgulanmalıdır. Ayrıca TAF/FTC/EVG/Cob rejiminden geçilen hastaların total kolesterol değerlerinde azalma görülmekle birlikte GFH değerlerinde anlamlı düşüş olması nedeniyle böbrek fonksiyonları yakın takip edilmelidir.
GİRİŞ
İnsan immün yetmezlik virusu (“human immunodeficiency virus” – HIV”) infeksiyonu tüm dünyada önemli bir sağlık sorunu olup Dünya Sağlık Örgütü (DSÖ) 2023 yılı verilerine göre yaklaşık 40 milyon kişinin ölümüne sebep olmuştur. Küresel ve kronik bir halk sağlığı sorunu olan hastalık, kür olarak tanımlanabilecek bir tedavisi olmamakla birlikte önleme, tanı, tedavi ve bakım hizmetlerine erişim sayesinde yönetilebilir durumdadır (1).
HIV ile yaşayan bireylere CD4+T lenfosit sayısından bağımsız olarak antiretroviral tedavi (ART)’ye en kısa sürede başlanması önerilmektedir. Günümüzde ilaç rejiminde, direnç bariyeri yüksek ve HIV viral yükünü (HIV RNA) hızlı baskılayacak ilaçların seçilmesi önerilmektedir. Hastaların tedavi takiplerinde, hasta veya ilaç kaynaklı tedavi değişikliği yapılabilmektedir. Tedavi değişikliği sonrası izlemde kullanılacak parametreler kılavuzlarda benzerdir (2-3). Bununla birlikte, tedavi yanıtının ve yan etkilerin yakın takibi gerekmektedir (4). Literatürde tedavi değişikliği sonrası tedavi yanıtı, yan etki ve uzun dönem takibi açısından sınırlı sayıda gerçek yaşam verisi bulunmaktadır.
TAF/FTC/BIC; tenofovir alafenamid, emtrisitabin ve biktegravirden oluşan ve tek tablet olan bir ART rejimidir; HIV ile yaşayan bireylerde, tedavi deneyimli hastalarda ve tedavi değişiminde ulusal ve uluslararası rehberlerde önerilmektedir (2-3). Biktegravir, dirence karşı yüksek genetik bariyere sahip integraz inhibitörüdür. Kemik mineral yoğunluğu ve böbrek fonksiyonları üzerine olumsuz etkisi tenofovir disoproksil fumarat (TDF) bazlı rejime göre daha az iken daha fazla ağırlık artışı rapor edilmiş olup birçok klinik çalışma, tedavi naif ve HIV ile yaşayan tedavi deneyimli bireylerde etkili ve iyi tolere edilen bir rejim olduğunu göstermiştir (5-9).
Çalışmamızda; virolojik baskılanması sağlanmış, tedavi deneyimli ve TAF/FTC/BIC rejimine geçiş yapılmış hastaların, 48 haftalık takiplerinde tedavi etkinliğini gösteren virolojik ve immünolojik değişimlerin yanı sıra böbrek fonksiyonları ve lipid profillerindeki değişikliklerin değerlendirilmesi amaçlandı.
YÖNTEMLER
Retrospektif ve tek merkezli olarak gerçekleştirilen çalışmaya, hastanemizin İnfeksiyon Hastalıkları Polikliniği’ne Ocak 2020-Aralık 2021 tarihleri arasında başvuran, 18 yaş ve üzeri, HIV ile yaşayan tedavi deneyimli bireyler dahil edildi. TAF/FTC/BIC rejimine geçiş yapılmış 155 hasta dosyasına ulaşıldı ve bu hasta grubunda, verilerine ulaşılamayan 47 hasta ve saptanabilir HIV RNA düzeyi tespit edilen 31 hasta çalışmadan dışlandı. Geriye kalan 77 hasta üzerinden virolojik ve biyokimyasal karşılaştırmalar yapıldı.
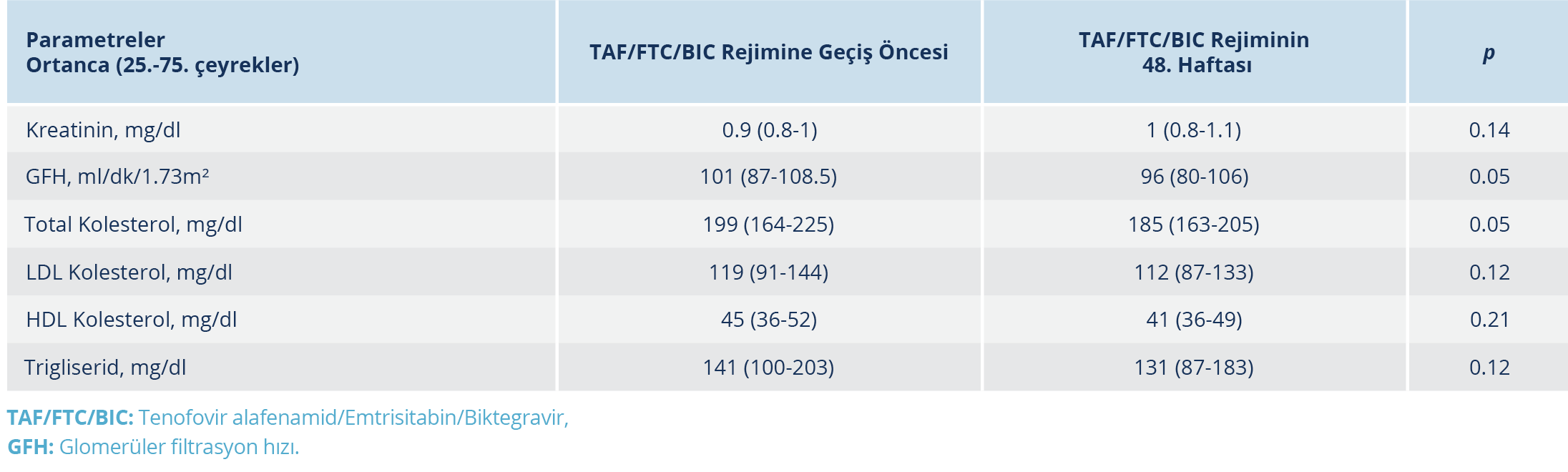
HIV ile yaşayan, ART alan ve virolojik süpresyonu sağlanmış olup TAF/FTC/BIC rejimine herhangi bir nedenle geçiş yapılan bireylerin; tedavi değişimi öncesi ve sonrası takiplerindeki virolojik ve immünolojik parametre sonuçları, böbrek fonksiyon ve lipid profillerinin belirlendiği laboratuvar test sonuçları elektronik tıbbi kayıtlardan alındı. Kreatinin, glomerüler filtrasyon hızı (GFH), total kolesterol, düşük yoğunluklu lipoprotein kolesterol (LDL-kolesterol), yüksek yoğunluklu lipoprotein kolesterol (HDL-kolesterol) ve trigliserid (TG) tedavi değişimi öncesi ve tedavi değişimi sonrası 48. haftada; HIV RNA, CD4+T lenfosit sayısı, CD4+ T lenfosit yüzdesi ve CD4+T lenfosit / CD8+T lenfosit oranı tedavi değişimi öncesi ve sonrasında 24. ve 48. haftada değerlendirildi.
Merkezimizde saptanabilir HIV RNA düzeyi >20 kopya/ml idi. Hastaların tedavi değişimi sonrası ART’ye verilen farklı virolojik yanıt seviyelerinin tanımlamaları aşağıda verildiği şekilde yapıldı (5):
- Virolojik süpresyon; HIV RNA düzeyinin mevcut testlerin alt limit değerinin altında olması.
- Virolojik yanıtsızlık; viral replikasyonun HIV RNA düzeyi <200 kopya/ml olacak şekilde baskılanamaması veya sürdürülememesi.
- Tam olmayan virolojik yanıt; 24 hafta ART rejimi uygulandıktan sonra, bu rejimde henüz virolojik baskılanma belgelenmemiş bir hastada ardışık iki plazma HIV RNA düzeyinin ≥200 kopya/ml olarak saptanması.
- Virolojik geri tepme (“rebound”); virolojik süpresyonun ardından HIV RNA düzeyinin ≥200 kopya/ml olarak saptanması.
- Virolojik sıçrama (“blip”); virolojik süpresyonun ardından izole edilmiş, saptanabilir bir HIV RNA düzeyi saptanması ve ardından virolojik süpresyona geri dönüş sağlanması.
- Düşük seviyeli viremi; saptanabilir HIV RNA düzeyinin <200 kopya/ml olması.
Dünya Tabipler Birliği Helsinki Bildirgesi’ne uygun olarak yürütülen çalışma için İstanbul Haseki Eğitim ve Araştırma Hastanesi Etik Kurulu’ndan 6 Aralık 2023 tarih ve 225-2023 karar numarasıyla onay alındı. Çalışmamızın retrospektif niteliğinden dolayı yazılı bilgilendirilmiş onamdan feragat edildi.
İstatistiksel Analiz
Nicel değişkenlerde, sürekli normal dağılımlı olmayan veriler için ortanca (25-75. çeyrekler) değerler hesaplanarak karakterize edilirken, kategorik veriler yüzde (%) ve sayı (n) cinsinden ifade edildi. Kategorik verileri karşılaştırmak için Pearson χ2 testi kullanıldı. Parametrik testleri seçmek üzere sürekli verilerin normal dağılımını değerlendirmek için Kolmogorov-Smirnov testi, kutu grafiği, ortalama-ortalama ölçüleri ve Skewness-Kurtosis değerleri kullanıldı. Dikotom bağımsız non-parametrik gruplar arasında sürekli verileri analiz etmek için Mann-Whitney U testi uygulandı. Sonuçlar, %95 güven aralığı (GA)’nda incelendi ve önceden belirlenen istatistiksel anlamlılık düzeyi p<0.05 olarak kabul edildi. Verilerin analizi, SPSS (Statistical Package for the Social Sciences) versiyon 21.0 programı (IBM Corp., Armonk, NY, ABD) ile yapıldı.
BULGULAR
Çalışmamıza, virolojik süpresyonu sağlanmış ve TAF/FTC/BIC rejimine geçiş yapılan 77 hasta dahil edildi. Hastaların 71 (%92.2)’i erkek, ortanca yaş 42 (35-51.5) yıl ve hepatit B koinfeksiyonu olan hasta sayısı 5 (%6.4) idi. Hastaların ART alma süresi 6 (5-9) yıl olarak tespit edildi. Hastaların 60 (%77.9)’ında tenofovir alafenamid/emtrisitabin/elvitegravir/kobisistat (TAF/FTC/EVG/Cob) içeren rejimden TAF/FTC/BIC’e geçiş yapılırken 15 (%19.5)’inde tenofovir disoproksil fumarat/emtrisitabin/dolutegravir (TDF/FTC/ DTG) içeren rejimden geçiş yapılmıştı. TAF/FTC/BIC rejimine geçişin en sık nedeni 61 (%79.2) hasta ile hekim kararıyla tedaviyi basitleştirmeydi; bunu osteopeni/osteoporoz gelişimi, hasta isteği, ilaç
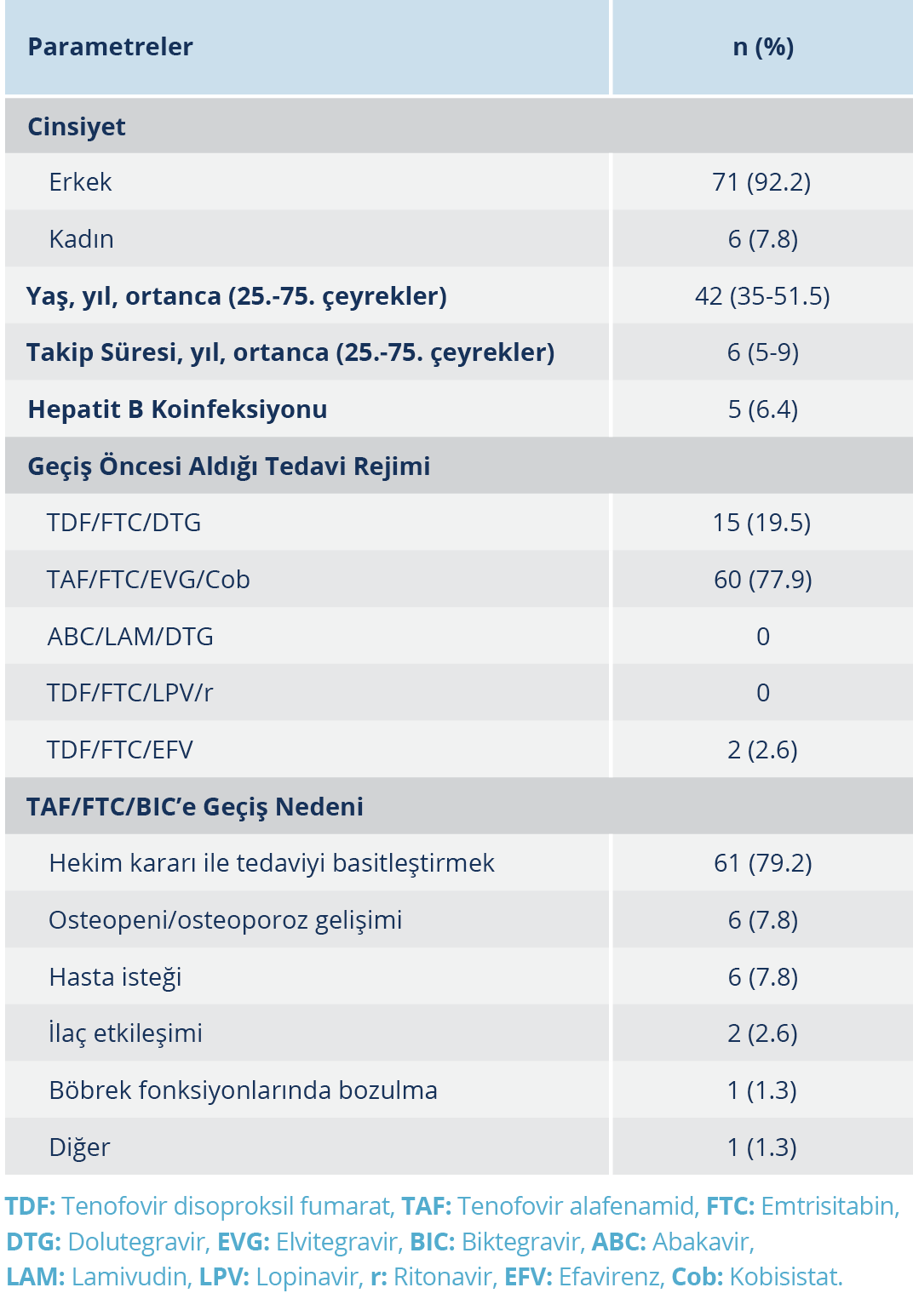
Tablo 1. HIV ile Yaşayan Bireylerin Demografik Verileri, Tedavi Rejimleri ve Tedavi Değişikliği Nedenleri
etkileşimi ve böbrek fonksiyonlarında bozulma takip ediyordu (Tablo 1).
TAF/FTC/BIC rejimine geçiş öncesi ve sonrası karşılaştırılan 77 hastanın 48. haftada bakılan GFH (101 ml/dk/1.73m² vs. 96 ml/dk/1.73m²; p=0.05) ve total kolesterol (199 mg/dl vs. 185 mg/dl; p=0.05) değerlerinde azalma istatistiksel anlamlılık sınırına yakın saptanırken; kreatinin, trigliserid, LDL-kolesterol ve HDL-kolesterol değerlerinde anlamlı düzeyde fark saptanmadı (Tablo 2). TAF/FTC/BIC rejimine geçiş öncesi tedaviler, alt grup analiziyle değerlendirildiğinde; GFH (101 ml/dk/1.73m² vs. 95 ml/dk/1.73m²; p=0.016) ve total kolesterol (205 mg/dl vs. 182 mg/dl; p<0.001) değerlerindeki azalmanın sadece TAF/FTC/EVG/Cob rejiminden TAF/FTC/BIC’e geçişte olduğu görüldü.
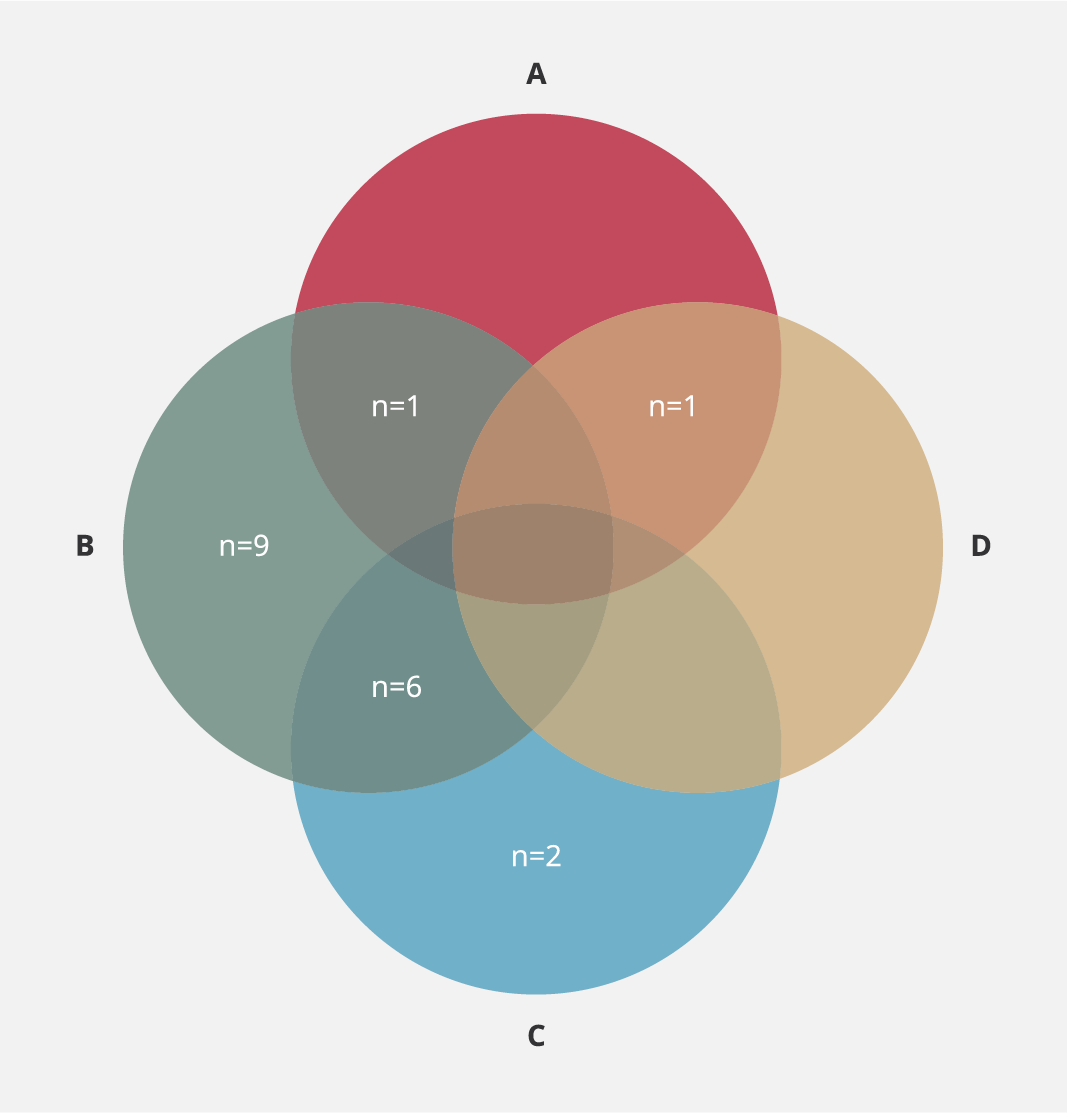
Şekil 1. HIV ile Yaşayan Tedavi Deneyimli Bireylerde TAF/FTC/
BIC Rejimine Geçiş Sonrası Virolojik Yanıt Parametre Sonuçlarının
Venn Şeması ile Gösterimi (A: Virolojik geri tepme, B: Virolojik
sıçrama, C: Düşük düzeyli viremi, D: Virolojik yanıtsızlık)
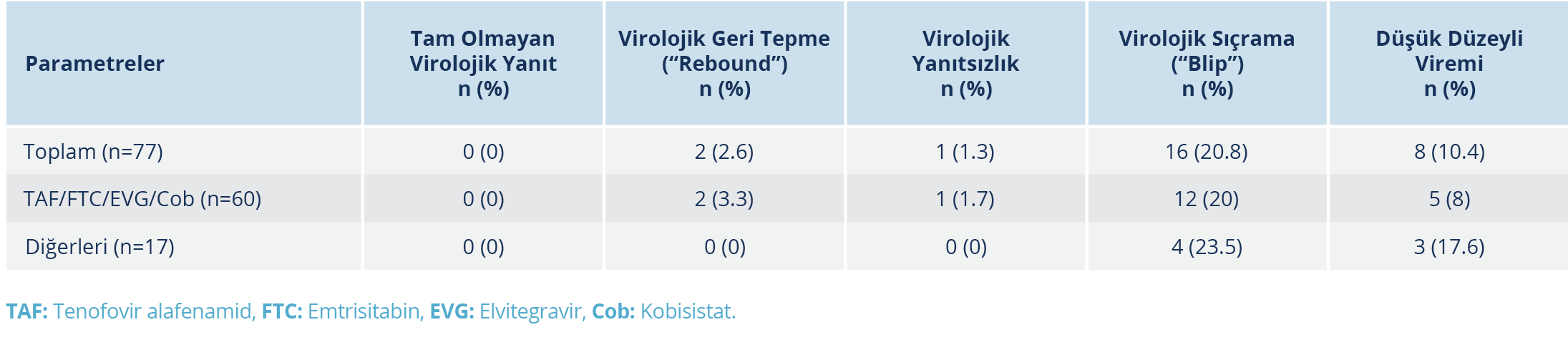
TAF/FTC/BIC rejimine geçiş sonrası hastaların 19 (%24.7)’unda virolojik süpresyonun bozulduğu görüldü. Farklı düzeylerdeki virolojik yanıtlar değerlendirildiğinde; “tam olmayan virolojik yanıt” saptanmamakla birlikte, hastaların 2 (%2.6)’sinde virolojik geri tepme, 1 (%1.3)’inde virolojik yanıtsızlık, 8 (%10.4)’inde düşük düzeyli viremi ve 16 (%20.8)’sında virolojik sıçrama saptandı (Tablo 3, Şekil 1).
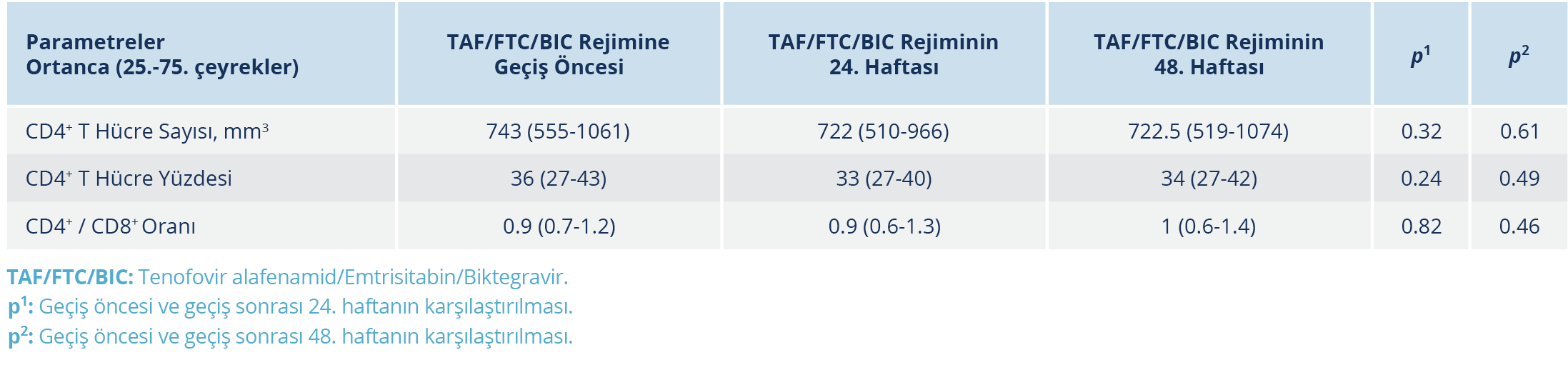
Virolojik süpresyonu bozulan hastaların takiplerinde; hastaların %89 (17/19)’unda spontan virolojik süpresyon görülmüş ve TAF/FTC/BIC tedavisinin değiştirilmesine gerek duyulmamıştı. Tedavi sonrası 24. ve 48. haftada viral yük saptanan hastaların ortanca HIV RNA düzeyi 35 (27-77) kopya/ml ve 34 (24-49) kopya/ml olarak saptandı. 24. haftada HIV RNA düzeyi ≥50 kopya/ml olan hasta oranı %9.1 (7/77) iken, HIV RNA düzeyi ≥200 kopya/ml olan hasta oranı %1.3 (1/77) idi. 48. haftada ise HIV RNA ≥ 50 kopya/ml oranı %3.9 (3/77) iken, HIV RNA>200 kopya/ml oranı %1.3 (1/77) olarak saptandı. Tedavi öncesi değerlerle karşılaştırıldığında, CD4+T lenfosit sayısında (24. hafta p=0.32, 48. hafta p=0.61), CD4+ T lenfosit yüzdesinde (24. hafta p=0.24 ve 48. hafta p=0.49) ve CD4+/CD8+ oranında (24. hafta p=0.82 ve 48. hafta p=0.46) anlamlı düzeyde fark saptanmadı (Tablo 4).
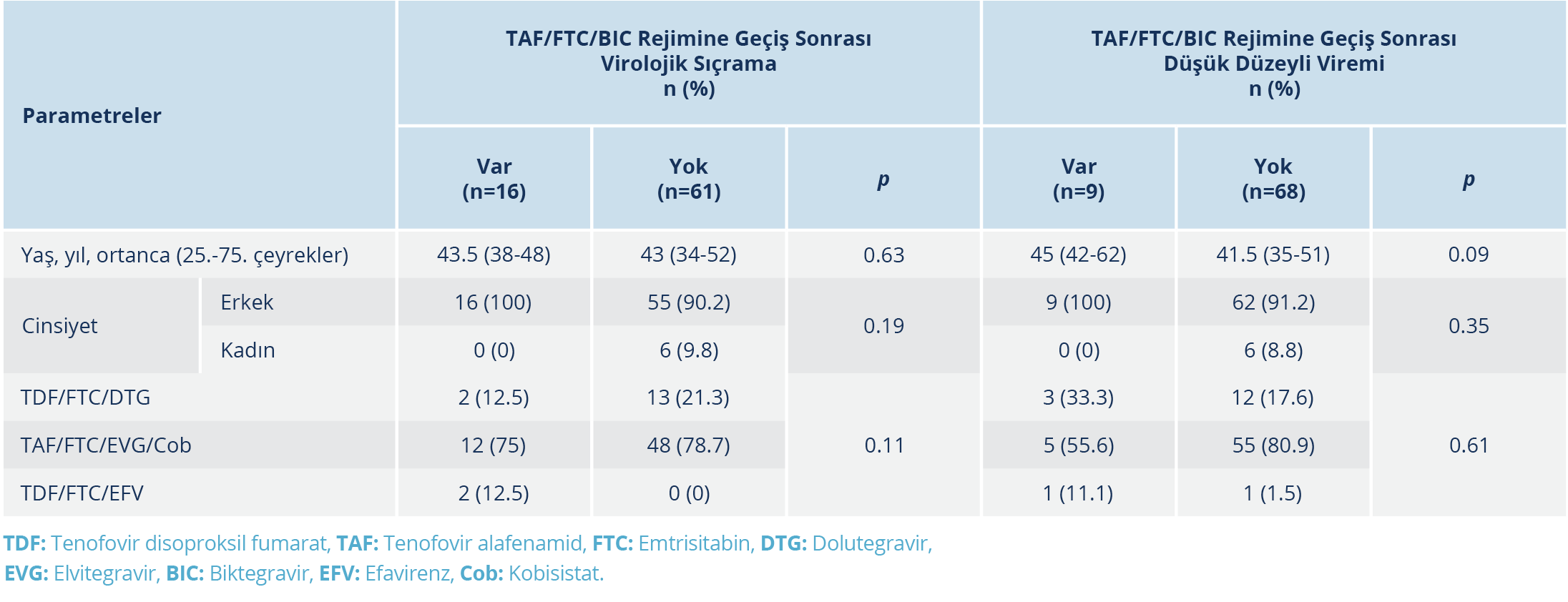
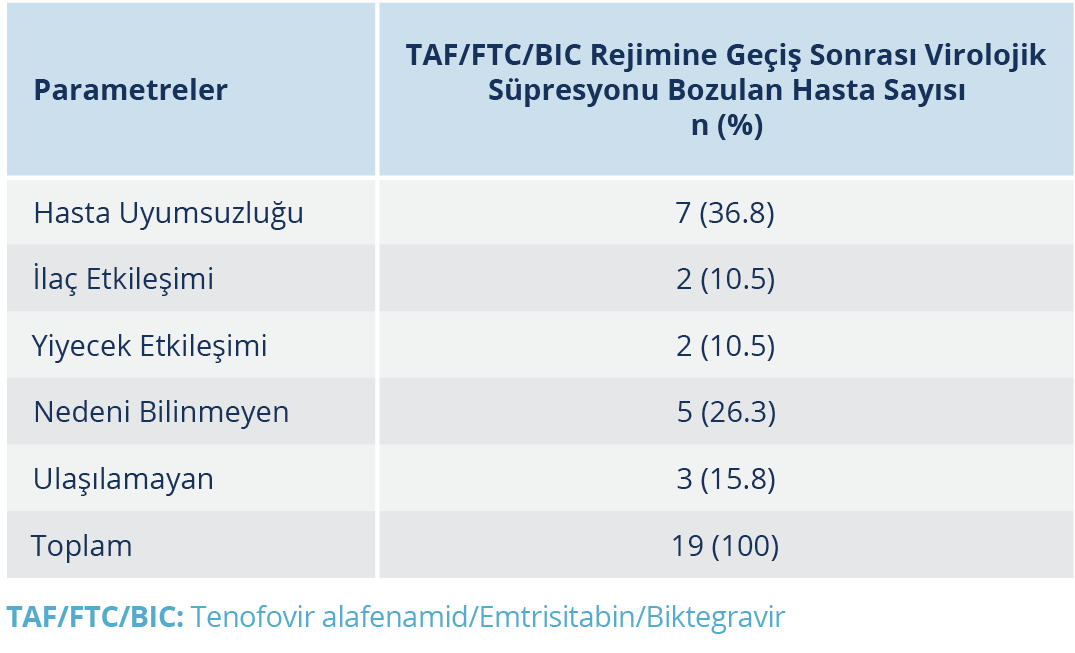
Tedavi değişikliği sonrası virolojik sıçrama saptanan ve saptanmayan hastaların yaş (p=0.63), cinsiyet (p=0.19) ve geçiş öncesi ART rejimleri (p=0.11) karşılaştırıldığında anlamlı düzeyde bir fark saptanmadı. Tedavi değişikliği sonrası düşük düzeyli viremi saptanan ve saptanmayan hastaların yaş (p=0.09), cinsiyet (p=0.35) ve geçiş öncesi ART rejimleri (p=0.61) karşılaştırıldığında da anlamlı düzeyde bir fark saptanmadı (Tablo 5). Virolojik süpresyonun korunamamasının olası nedenleri araştırıldığında, en sık karşılaşılan neden %38.8 (7/19) oranıyla tedavi uyumsuzluğu idi (Tablo 6).
İRDELEME
Çalışmamızda, HIV infeksiyonu nedeniyle tedavi alıp virolojik baskılanması sağlanmış ve TAF/FTC/BIC rejimine geçiş yapılmış 77 hastanın 24 ve 48 haftalık takiplerindeki virolojik ve immünolojik parametre sonuçları, böbrek fonksiyonları ve lipid profillerindeki değişiklikler retrospektif olarak değerlendirildi. Hastaların yaklaşık %75’inde tedavi değişikliği öncesi var olan virolojik süpresyon TAF/ FTC/BIC rejimine geçiş sonrası da devam etmesine rağmen yaklaşık %25’inde virolojik süpresyonun korunamadığı görüldü. Hastaların yaklaşık %3’ünde virolojik geri tepme, %1’inde virolojik yanıtsızlık, %10’unda ise düşük düzeyli viremi ve %21’inde virolojik sıçrama saptandı.
TAF/FTC/BIC rejimi ile diğer ART rejimleri ile kıyaslandığında virolojik başarısızlık oranlarının benzer olduğu görülmüştür (10-11). Gan ve arkadaşlarının (12) çalışmasında, daha önce ART almayan 80 hastaya TAF/FTC/BIC başlandıktan 24 hafta sonra hastaların %13.4’ünde virolojik süpresyonun sağlanamadığı bildirilmiştir. Bir diğer çalışmada, 48. haftada, HIV RNA düzeyi ≥50 kopya/ml olan katılımcıların oranı %6.1 (14/229) iken düşük düzeyli viremi insidansı %4.9 (10/206) olarak saptanmıştır (13). Rolle ve arkadaşlarının (14) çalışmasında, TAF/FTC/BIC’e geçiş yapılan hastaların 48 haftalık takip sonrasında %94 (330/350)’ü virolojik baskılamayı sürdürürken, %6 (20/350)’sında HIV RNA düzeyinin ≥50 kopya/ml olduğu görülmüştür (14). Çalışmamızda, düşük düzey viremi oranı literatüre kıyasla yüksek saptandı. Bu durum merkemizde saptanabilir HIV RNA düzeyinin >20 kopya/ml olmasıyla ilişkilendirildi. Çalışmamızda, 24. haftada HIV RNA düzeyi ≥50 kopya/ml olan hasta oranı %9.1 (7/77) iken, 48. haftada bu oran %3.9 (3/77) idi. Knobel ve arkadaşlarının (15) çalışmasında, virolojik süpresyonu sağlanmış TAF/FTC/BIC’e geçiş yapılan HIV ile yaşayan bireylerde virolojik başarısızlık (iki ardışık ölçümde HIV RNA düzeyi >200 kopya/ml) %0.9 oranında bildirilmiştir. Çalışmamızda, güncel virolojik yanıt tanımlamaları kullanılmakla birlikte 48. hafta sonunda HIV RNA düzeyi >200 kopya/ml olan yalnızca bir hasta vardı (1/77).
Gidari ve arkadaşlarının (16) çalışmasında, tedavi geçişi öncesi hastaların %69.6 (166/242)’sında HIV RNA düzeyi <20 kopya/ml iken geçişten sonra bu oran %83 (203/242)’e yükselmiştir (p<0.0001). Lazzaro ve arkadaşlarının (17) çalışmasında ise TAF/FTC/BIC rejimine geçiş yapılan hastaların 48 haftalık takibi sonrasında HIV RNA düzeyi <37 kopya/ml olan hasta sayısı yaklaşık %4’e yükselmiştir (p<0.033). Çalışmamızda ise dahil edilen hastaların tümünde tedavi değişikliği öncesi HIV RNA saptanamaz düzeyde olup tedavi sonrası 24. ve 48. haftada ortanca HIV RNA değerleri sırasıyla 35 (27-77) kopya/ml ve 34 (24-49) kopya/ml olarak saptandı. Armenia ve arkadaşlarının (18) çalışmasında, TAF/FTC/BIC rejimine geçişten 96 hafta sonra, ortalama viremi düzeyi 284 (187-980) kopya/ml olarak bildirilmiştir; 96 haftanın sonunda virolojik geri tepme oranı %5’tir. Çalışmamızda ise virolojik geri tepme oranı %2.6 olarak saptandı. Bununla birlikte çalışmamızda takip süresi 48 hafta ile daha kısaydı.
Xiao ve arkadaşlarının (19) çalışmasında, total kolesterol değerinde azalma, GFH ve serum kreatinin seviyelerinde iyileşme eğilimi gözlenmiştir (p<0.001). Bir diğer çalışmada, 48 haftalık takip sonunda total kolesterol düzeyinde %6.9 oranında azalma (p<0.001), LDL kolesterol değerinde % 6.8 oranında azalma (p=0.007) ve HDL kolesterol değerinde ise %4.4 oranında artış (p=0.007) tespit edilmiştir; bu çalışmada serum kreatinin seviyelerinde gözlenen %0.8’lik anlamlı artışa (p=0.014) rağmen GFH’de herhangi bir değişiklik tespit edilmemiştir (p=0.784) (17). Hsu ve arkadaşlarının (20) çalışmasında da geçişten 96 hafta sonra total kolesterol değerinde 11.6 mg/dl (p<0.0001) ve LDL-kolesterol 3.4 mg/dl ile azalma (p=0.0084) tespit edilmiştir. Çalışmamızda ise TAF/FTC/BIC rejimine geçiş öncesi ve geçişten 48 hafta sonra bakılan GFH (101 ml/dk/1.73m² vs. 96 ml/dk/1.73m²; p=0.05) ve total kolesterol (199 mg/dl vs. 185 mg/dl; p=0.05) değerlerinde azalma saptandı. LDL-kolesterol düzeyinde de azalma görülmekle birlikte bu azalma anlamlı düzeyde bulunmadı (p=0.12).
Çalışmamızda tedavi değişikliği öncesi alınan tedaviler, alt grup analiziyle değerlendirildiğinde; GFH ve total kolesterol değerlerindeki azalmanın sadece TAF/FTC/EVG/Cob rejiminden TAF/FTC/BIC’e geçişte olduğu görüldü. Xiao ve arkadaşlarının (19) çalışmasında da TAF/FTC/EVG/Cob rejiminden geçiş yapılan hastalarda da total kolesterol ve LDL-kolesterol düzeylerinde azalma eğilimi bildirilmiştir. Balcı ve arkadaşlarının (21) çalışmasında, geçiş sonrası hastaların takiplerinde GFR değerinin bazal değerine göre azalmasının istatistiksel olarak anlamlı düzeyde olduğu bildirilmiştir (p<0.05). Literatürde TAF/FTC/BIC rejimine geçiş sonrası total kolesterol ve LDL kolesterol düzeylerinin anlamlı düzeyde arttığını bildiren bir çalışma da mevcuttur; söz konusu çalışmada glukoz ve kreatinin seviyelerinde de anlamlı düzeyde artış bildirilmiştir (19). Çalışmamızda, kreatinin seviyelerinde artış saptanmış olmakla birlikte bu fark istatistiksel olarak anlamlı bulunmadı (p=0.14).
Lazzaro ve arkadaşlarının (17) çalışmasında, tedavi değişikliği sonrasında CD4+ T lenfosit sayısında %30.1 (p<0.001), CD8+ T lenfosit sayısında %7.1 (p=0.004) ve CD4+/CD8+ oranında %21.5 artış (p<0.001) saptanmıştır. Peng ve arkadaşlarının (23) çalışmasında ise tedavi değişikliği sonrası 24. haftada CD4+ T hücre sayısında anlamlı düzeyde bir artış bildirilmiştir (p=0.037). Çalışmamızda TAF/FTC/BIC rejimine geçiş öncesiyle karşılaştırıldığında, CD4+T lenfosit sayısında, CD4+ T lenfosit yüzdesinde ve CD4+/CD8+ oranında anlamlı düzeyde bir değişiklik yoktu.
Canetti ve arkadaşlarının (7), virolojik başarısızlık nedenlerinin irdelendiği ve 1040 hastanın dahil edildiği çalışmasında, toplam 44 hastada virolojik başarısızlık görülmüş ve bunun için en sık karşılaşılan neden olarak ilaç uyumsuzluğu bildirilmiştir. Yaptığımız çalışmada da en sık (%36.8) karşılaşılan virolojik başarısızlık nedeni olarak tedavi uyumsuzluğu tespit edildi. Canetti ve arkadaşlarının (7) çalışmasında, virolojik başarısızlık bildirilen olguların %75’inin takibinde spontan virolojik süpresyon sağlanmıştır. Çalışmamızda da hastaların %89’unda spontan virolojik süpresyon görüldü ve TAF/FTC/BIC rejiminin değiştirilmesine gerek duyulmadığı tespit edildi. Bir başka çalışmadaysa, TAF/FTC/BIC rejiminde ilaç-ilaç etkileşimi nedeniyle %19 oranında başarısızlık bildirilmiştir (24). Çalışmamızda ilaç uyumsuzluğu sonrası en sık (%10.5) virolojik başarısızlık nedeni ilaç-ilaç etkileşimiydi. Literatürdeki farklı çalışmalarda, TAF/FTC/BIC’e geçtikten sonra ilaç-ilaç etkileşimi oranlarında azalma tespit edildiği vurgulanmıştır (14-25). Çalışmamızda hastaların önceki ilaç rejimlerinin etkileşim oranlarına değinilmediğinden oransal kıyaslama yapılamadı.
Çalışmamızın en önemli kısıtlılığı tek merkezli ve retrospektif olmasıdır. Ayrıca, hastaların total kolesterol ve GFH değerlerindeki azalmanın istatistiksel olarak anlamlılık sınırına yakın olması hasta sayısının göreceli olarak azlığı ile açıklanabilir. Hasta verilerinin yetersizliği nedeniyle, bel çevresi ve vücut kitle indeksi gibi parametrelerdeki değişiklikler izlenemedi. Çalışmamız kapsamında, virolojik baskılanması gerçekleşmiş olan hastalarda TAF/FTC/BIC rejimine geçiş sonrası sonuçlar değerlendirilemedi ve bu nedenle virolojik baskılanması olmayan grupta geçiş sonrası sonuçlar öngörülemedi.
Sonuç olarak; TAF/FTC/BIC rejimine geçiş öncesi virolojik süpresyon sağlanmış olsa da geçiş sonrası hastaların önemli bir oranında virolojik baskılanmanın bozulabileceği göz önünde bulundurulmalı ve bu hastalar detaylı sorgulanmalıdır. Ayrıca, özellikle TAF/FTC/EVG/Cob rejiminden geçilen hastaların total kolesterol değerlerinde azalma görülmekle birlikte GFH değerlerinde anlamlı düşüş olması nedeniyle böbrek fonksiyonları yakın takip edilmelidir.
Hasta Onamı
Veriler retrospektif olarak incelendiği için hasta onamı alınmamıştır.
Etik Kurul Kararı
Çalışma için İstanbul Haseki Eğitim ve Araştırma Hastanesi Etik Kurulu’ndan 6 Aralık 2023 tarih ve 225-2023 karar numarasıyla onay alınmıştır.
Danışman Değerlendirmesi
Bağımsız dış danışman
Yazar Katkıları
Fikir/Kavram – G.T., Ç.Y., S.S., B.Ç., C.G.G.; Tasarım – G.T., Ç.Y., S.S., B.Ç., C.G.G., O.F.B.; Denetleme – G.Ş., M.Y., F.P.; Veri Toplama ve/veya İşleme – G.T., Ç.Y., S.S., B.Ç., C.G.G.; Analiz ve/veya Yorum – G.T., Ç.Y., S.S., C.G.G., K.G.G., O.F.B., B.A.B.; Literatür Taraması – G.T., Ç.Y., S.S., C.G.G., K.G.G., O.F.B., B.A.B.; Makale Yazımı – Tüm Yazarlar; Eleştirel İnceleme – Tüm Yazarlar.
Çıkar Çatışması
Yazarlar herhangi bir çıkar çatışması bildirmemiştir.
Finansal Destek
Yazar finansal destek beyan etmemiştir.
Sunulan Bilimsel Etkinlik
6-9 Mart 2024 tarihinde gerçekleştirilen 24. Türk Klinik Mikrobiyoloji ve İnfeksiyon Hastalıkları Kongresi’nde bildiri olarak sunulmuştur.
Referanslar
- HIV and AIDS [Internet]. Geneva: World Health Organization (WHO). [erişim 15 Kasım 2023]. https://www.who.int/news-room/fact-sheets/detail/hiv-aids
- EACS Guidelines 2023, v.12.0., [Internet]. Brussels: European AIDS Clinical Society (EACS). [erişim 15 Kasım 2023]. https://eacs.sanfordguide.com/
- HIV/AIDS Tanı, İzlem ve Tedavi El Kitabı, Sürüm 3.0, Şubat 2024. [Internet]. Türk HIV/AIDS Platformu. [erişim 01 Mart 2024]. https://www.klimik.org.tr/wp-content/uploads/2024/02/HIV-AIDS.El_.Kitabi_Surum.3.pdf
- Benli A, Başaran S, Şimşek-Yavuz S, et al. [Comparison of antiretroviral therapy regimens in terms of virological response, immunological response and adverse effects in treatment-naive HIV-positive patients]. Klimik Derg. 2018;31(2):94-100. Turkish.
- Guidelines for the use of antiretroviral agents in adult and adolecents with HIV [Internet]. Rocville: Office of AIDS Research National Institutes of Health (Clinicalinfo). [erişim 01 Aralık 2023]. https://clinicalinfo.hiv.gov/en/guidelines/hiv-clinical-guidelines-adult-and-adolescent-arv
- Esser S, Brunetta J, Inciarte A, et al. Twelve-month effectiveness and safety of bictegravir/emtricitabine/tenofovir alafenamide in people with HIV: Real-world insights from BICSTaR cohorts. HIV Med. 2023;1-14. [CrossRef]
- Canetti D, Galli L, Lolatto R, et al. Bictegravir/emtricitabine/tenofovir alafenamide treatment: Efficacy and tolerability in clinical practice. Drug Des Devel Ther. 2023;17:3697-706. [CrossRef]
- Januszka JE, Drwiega EN, Badowski ME. Bictegravir/emtricitabine/tenofovir alafenamide for HIV-1: What is the hidden potential of this emerging treatment? HIV AIDS (Auckl). 2023;15:705-11. [CrossRef]
- De Clercq E, Zhang Z, Huang J, Zhang M, Li G. Biktarvy for the treatment of HIV infection: Progress and prospects. Biochem Pharmacol. 2023;217:115862. [CrossRef]
- Wang R, Wright J, Saggu P, et al. Assessing the virologic impact of archived resistance in the dolutegravir/lamivudine 2-drug regimen HIV-1 switch study TANGO through week 144. Viruses. 2023;15(6):1350. [CrossRef]
- Fernvik E, Sierra Madero J, Espinosa N, et al. Impact of treatment adherence on efficacy of dolutegravir + lamivudine and dolutegravir + tenofovir disoproxil fumarate/emtricitabine: Pooled week 144 analysis of the GEMINI-1 and GEMINI-2 clinical studies. J Acquir Immune Defic Syndr. 2023;94(3):e9-12. [CrossRef]
- Gan L, Xie X, Fu Y, et al. Bictegravir/emtricitabine/tenofovir alafenamide versus dolutegravir plus lamivudine for switch therapy in patients with HIV-1 infection: A real-world cohort study. Infect Dis Ther. 2023;12(11):2581-93. [CrossRef]
- Gan L, Xie X, Fu Y, et al. Efficacy and safety of bictegravir/emtricitabine/tenofovir alafenamide fumarate for adult patients with human immunodeficiency virus-1 in China: a retrospective real-world cohort study. Expert Rev Anti Infect Ther. 2023:1-7. [CrossRef]
- Rolle CP, Nguyen V, Patel K, Cruz D, DeJesus E, Hinestrosa F. Real-world efficacy and safety of switching to bictegravir/emtricitabine/tenofovir alafenamide in older people living with HIV. Medicine (Baltimore). 2021;100(38):e27330. [CrossRef]
- Knobel H, Cañas-Ruano E, Guelar A, et al. Switching to dolutegravir/lamivudine or bictegravir/emtricitabine/tenofovir alafenamide. A comparative real-world study. HIV Res Clin Pract. 2023;24(1):2239564.
- Gidari A, Benedetti S, Tordi S, et al. Bictegravir/tenofovir alafenamide/emtricitabine: A real-life experience in people living with HIV (PLWH). Infect Dis Rep. 2023;15(6):766-77. [CrossRef]
- Lazzaro A, Cacciola EG, Borrazzo C, et al. Switching to a bictegravir single tablet regimen in elderly people living with HIV-1: Data analysis from the BICTEL cohort. Diagnostics (Basel). 2021;12(1):76. [CrossRef]
- Armenia D, Forbici F, Bertoli A, et al. Bictegravir/emtricitabine/tenofovir alafenamide ensures high rates of virological suppression maintenance despite previous resistance in PLWH who optimize treatment in clinical practice. J Glob Antimicrob Resist. 2022;30:326-34. [CrossRef]
- Xiao J, Gao G, Ding Y, et al. Reasons, safety and efficacy analysis for conversion of HAART to TAF/FTC/BIC among HIV-infected patients. Chin Med J (Engl). 2023;136(24):2931-7. [CrossRef]
- Hsu JY, Sun HY, Chen LY, et al. Weight and metabolic changes among virally-suppressed people living with HIV who switched to co-formulated bictegravir/emtricitabine/tenofovir alafenamide. J Glob Antimicrob Resist. 2023:S2213-7165(23)00181-9. [CrossRef]
- Balcı U, Üser Ü, Tahmaz A, Sarigul Yildirim F. Real-life experience with bictegravir/emtricitabine/tenofovir alafenamide in Turkey. Cureus. 2023;15(10):e47253. [CrossRef]
- Pérez-Barragán E, Guevara-Maldonado MF, Mancilla-Galindo J, et al. Weight gain after 12 months of switching to bictegravir/emtricitabine/tenofovir alafenamide in virologically suppressed HIV patients. AIDS Res Hum Retroviruses. 2023;39(10):511-7. [CrossRef]
- Peng Y, Cao X, Wang Y, Yu W, Zeng Z, Wang M. Outcomes of bictegravir/emtricitabine/tenofovir alafenamide versus efavirenz-based regimens in central China: a real-world assessment. Chin Med J (Engl). 2023;136(22):2738-40. [CrossRef]
- Lopes S, O’Day K, Meyer K, et al. Comedication prescription patterns and potential for drug-drug interactions with antiretroviral therapy in people living with human immunodeficiency virus type 1 infection in Germany. Pharmacoepidemiol Drug Saf. 2020;29(3):270-8. [CrossRef]
- Schafer JJ, Pandit NS, Cha A, et al. Incidence and severity of drug ınteractions before and after switching antiretroviral therapy to bictegravir/emtricitabine/tenofovir alafenamide in treatment-experienced patients. Open Forum Infect Dis. 2020;8(1):ofaa625. [CrossRef]