En Çok Okunanlar
Özet
Amaç: Bu çalışmada, kliniğimizde izlenen insan immün yetmezlik virusu (HIV) ile infekte kadınların tercih ettiği doğum kontrol yöntemlerinin belirlenmesi ve gebelik yönetim şekillerinin incelenmesi amaçlandı.
Yöntemler: 1999-2021 yılları arasında, Ege Üniversitesi Tıp Fakültesi Hastanesi İnfeksiyon Hastalıkları ve Klinik Mikrobiyoloji Kliniği’nde takip edilmiş ve verilerine ulaşılabilen HIV ile infekte kadınların dosyaları geriye dönük olarak incelendi. Çalışma kapsamında; olguların demografik özellikleri, kendilerinin ve partnerlerinin kullanmış oldukları doğum kontrol yöntemleri ile bunları kullanma süreleri, HIV ile infekte olduktan sonra gebe kalanlarda gebe kalma yöntemleri, gebeliğin planlı olup olmadığı, gebelikten önce kullanılan antiretroviral tedaviler ve gebelik sırasında tedavi rejiminde değişiklik yapılıp yapılmadığı, doğumdan önceki HIV-1 RNA düzeyi ile CD4+ T lenfosit sayıları, doğum şekli, bebeğe ve anneye uygulanan profilaksiler ve bunların süreleri ile bebeklerin HIV serolojik durumu analiz edildi.
Bulgular: Aktif olarak takip edilmiş 80 kadın olgunun verilerine ulaşılabilen 75’i (%93.7) çalışmaya dâhil edildi. Olguların yaş ortalaması 43.5 ±11.4’tü (minimum=18-maksimum=68). Doğum kontrol yöntemlerinden herhangi birini kullanan olgu sayısı 51 (%68) olup en sık kullanılan doğum kontrol yöntemi 31(%60.7) bireyle kondom kullanımıydı. Cinsel olarak aktif olan ve menopoz döneminde olmayan 60 olgunun 25’inde (%41.6) toplam 36 gebelik gerçekleşmiş, 33 bebek dünyaya gelmişti. Bebeklerden yalnızca biri HIV ile infekte olmuştu.
Sonuç: Cinsel olarak aktif olup HIV ile infekte olan kadınlarda seçilecek doğum kontrol yöntemine hasta ile birlikte karar verilmelidir. Gebelik döneminde yakın izlem ve standart bakım hem anne hem de bebeğin uzun dönem prognozu açısından önem taşımaktadır.
GİRİŞ
Anneden bebeğe insan immün yetmezlik virusu (HIV) bulaşması, dünya çapında yapılan çalışmalar sonucunda 2015 ile 2020 yılları arasında küresel ölçekte %20, HIV yükünün yüksek olduğu ülkelerde de %24 azalmıştır (1). Ancak tüm bu gelişmelere rağmen, Dünya Sağlık Örgütü (DSÖ) ve Birleşmiş Milletler HIV/AIDS Ortak Programı (Joint United Nations Programme on HIV/AIDS – UNAIDS) raporlarına göre 2020 yılında dünya çapında 150 000 çocuk yeni tanı almıştır ve HIV ile yaşayan 15 yaşından küçük çocuk sayısı 1.7 milyondur. Yine aynı yıl içinde AIDS nedeniyle hayatını kaybeden çocuk sayısının 90 000 olduğu bildirilmiştir (2). Herhangi bir korunma önlemi uygulanmayan gebeliklerde vertikal geçiş, gelişmekte olan ülkelerde %25-40, gelişmiş ülkelerde ise %14-25 olarak bildirilmiştir (3).
Seropozitif annelerin emzirdiği bebeklerin popülasyonu oluşturduğu bir çalışmada, seri polimeraz zincir reaksiyonu sonucu elde edilen tahmini rahim içi (in utero) bulaşma oranı %7.7, rahim içi ve doğum süreci (intrapartum) kombine bulaşma oranı %17.6 ve geç doğum (late postnatal) sonrası bulaşma oranı %4.9 olarak; yayınlanmış literatürün bir meta-analizinde ise emzirme yoluyla bulaşma riskinin oranı %14 olarak bildirilmiştir (4).
Ülkemizde ilk olgunun bildirildiği 1985 yılından bu yana resmi olarak rapor edilen olgu sayısı 15 Kasım 2021 itibariyle 29 284’tür. Bunların 285 (%0.97)’i 15 yaşın altındaki çocuklardır. Ülkemizde anneden bebeğe HIV bulaşma oranı %0.64 olarak tespit edilmiştir (5).
Anneden bebeğe bulaşmanın önlenebilmesi ancak gebeliğin erken döneminde yapılacak tarama ile HIV infeksiyonunun erken tespit edilmesi, gebelik boyunca antiretroviral tedavi kullanılarak HIV RNA ölçümünün özellikle doğum sırasında saptanabilir düzeyin altında tutulması, doğumdan sonra bebeğe antiretroviral profilaksi verilmesi ve bebeğin emzirilmemesi ile mümkündür (6,7). Bu önlemleri tam olarak uygulayan Amerika Birleşik Devletleri’nde ve Avrupa ülkelerinde bebeğe bulaşma oranının ≤%1 düzeylerine indiği bildirilmiştir (8).
Gebelik sırasında HIV infeksiyonunun erken tespit edilmesi, anneden bebeğe bulaşmayı önlemenin temel unsurudur. Öte yandan, HIV ile yaşayan ve çocuk doğurma potansiyeli olan tüm kadınların, konsepsiyon ve gebelik konusunda bilgilendirilmesi ve gebelik süreçlerini hekimleri ile birlikte planlayıp yürütmeleri, bulaşmanın önlenmesi açısından son derece önemlidir. Antiretroviral tedavinin kullanıma girmesiyle birlikte HIV ile yaşayan kadınlarda gebelik ve canlı doğum insidansının giderek yükseldiği ve tedavi almayanlara göre daha yüksek olduğu bildirilmektedir (9-11). Ayrıca planlanmamış gebelik insidansı (24.6/1000 kadın-yıl) da planlı gebelik insidansına (16.6/1000 kadın yılı) göre görece daha yüksek bulunmuştur (9). Tüm bunlara ek olarak, gebelikte kullanılması bebek açısından sakıncalı olabilecek antiretrovirallerin de bulunduğu bilinmektedir.
Bu bağlamda, HIV ile yaşayan kadınlarda planlanmamış gebelikten kaçınılması, gebelik düşünmeyenlere aile planlaması konusunda kapsamlı bir bilgilendirme yapılması ve en uygun doğum kontrol yönteminin seçilmesi, istenmeyen gebeliklerin önlenmesi açısından önem taşımaktadır. Gebe kalmak isteyen kadınlarda da güvenli bir gebelik süreci geçirilmesi ve hem annenin hem de bebeğin sağlığı açısından; gebeliğin hekim ile birlikte planlanması, gebe kadının izlemini yapan kadın hastalıkları ve doğum hekimi ile iletişim içinde olunması ve gebelik/doğum sürecinde bebeğe bulaşmayı engelleyecek tüm önlemlerin alınması HIV ile yaşayan kadına verilecek sağlık hizmetinin ayrılmaz bir parçası olmalıdır.
Çalışmamızda, kliniğimizde izlenen HIV ile infekte kadınların ve partnerlerinin tercih ettiği doğum kontrol yöntemlerinin, gebeliği yönetim şekillerinin ve bebeklere bulaşmayı önlemek amacıyla uygulanan korunma yöntemlerinin tespit edilmesi amaçlandı.
YÖNTEMLER
1999-2021 yılları arasında Ege Üniversitesi Tıp Fakültesi Hastanesi İnfeksiyon Hastalıkları ve Klinik Mikrobiyoloji Kliniği’nde takip edilmiş ve verilerine ulaşılabilen HIV ile infekte kadınların dosyaları geriye dönük olarak incelendi. Çalışma kapsamında; olguların demografik özellikleri, kendilerinin ve partnerlerinin kullanmış oldukları doğum kontrol yöntemleri ile bunları kullanma süreleri, HIV ile infekte olduktan sonra gebe kalanlarda gebe kalma yöntemleri, gebeliğin planlı olup olmadığı, gebelikten önce kullanılan antiretroviral tedaviler ve gebelik sırasında tedavi rejiminde değişiklik yapılıp yapılmadığı, doğumdan önceki HIV-1 RNA düzeyi ile CD4+ T lenfosit sayıları, doğum şekli, bebeğe ve anneye uygulanan profilaksiler ve bunların süreleri ile bebeklerin HIV serolojik durumu analiz edildi.
Çalışma, Ege Üniversitesi Tıp Fakültesi Klinik Araştırmalar Etik Kurulu tarafından 02 Mart 2022 tarih ve E.578865 karar numarasıyla onaylandı.
BULGULAR
1999-2021 yılları arasında aktif olarak takip edilen toplam olgu sayısı 644’tür; bunların 80 (%12.4)’i kadındır. Kapsamla uyumlu olarak ilgili verilerine ulaşılabilen 75 (%93.7) kadın olgu çalışmaya dâhil edilmiş olup yaş ortalaması 43.5 ±11.4 (minimum=18-maksimum=68) yıl olarak tespit edildi.
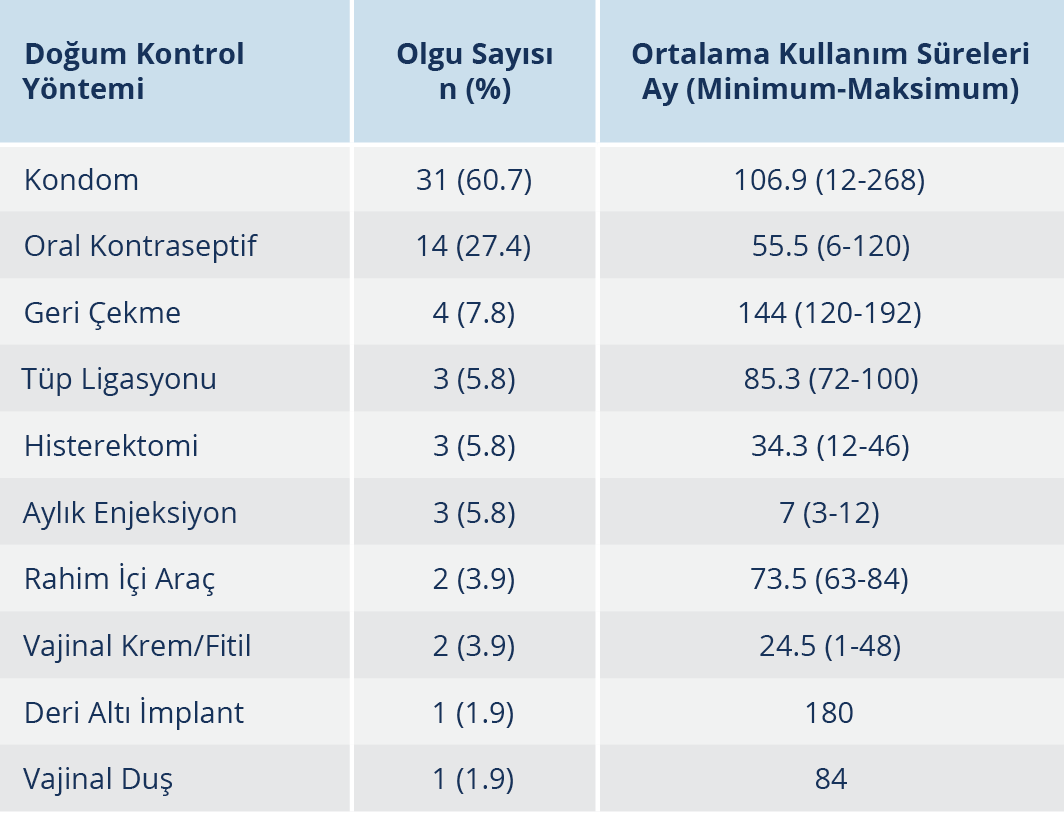
Tablo 1. HIV ile İnfekte Kadınların Kullandıkları Doğum Kontrol Yöntemleri ve Ortalama Kullanım Süreleri
Doğum kontrol yöntemlerinden herhangi birini kullanan olgu sayısı 51 (%68)’di. Doğum kontrol yöntemi kullanmayan 23 olgunun 15(%65.2)’inin cinsel aktivite göstermediği ve 8 (%34.7)’inin 40 yaş ve üzerinde olmaları nedeniyle kendi istekleriyle korunmadıkları öğrenildi. Olgulardan 41(%80.3)’inin tek, 9 (%17.6)’unun iki ve 2 (%3.9)’sinin üç farklı yöntemle korunduğu belirlendi. Birden fazla yöntem kullanan olguların %72.7’si oral kontrasepsiyona, %54.5’i ise kondoma ek olarak farklı bir yöntem kullanmıştı. Doğum kontrol yöntemlerinin genellikle HIV izlemini yapan hekimin bilgisi dışında, kadın hastalıkları ve doğum hekimlerinin önerisiyle veya bireyin kendi kararı ile kullanıldığı tespit edildi (Tablo 1).
Cinsel aktive gösteren ve menopoz döneminde olmayan 60 olgunun 25 (%41.6)’inde toplam 36 gebelik gerçekleştiği, bir olguda ikiz olmak üzere 33 bebek dünyaya geldiği tespit edildi; üç olguda gebelik annenin kendi isteği ile sonlandırılmış ve bir olguda düşük olmuştu. Gebelik gerçekleşen olguların 7 (%28)’sinin gebelik döneminde, diğerlerinin ise gebelik gerçekleşmeden önce HIV tanısı aldığı görüldü. Gebelik dönemlerinde antiretroviral ilaç tedavisinin ortalama 19. (minimum=6-maksimum=32) haftada başlandığı tespit edildi; gebelikten önceki dönemde tanı alan üç olguda tedaviye gebelik gerçekleştikten sonra başlanmış olup bu olgularda tedavinin başlama zamanı ortalama 15. (minimum=8-maksimum=31) haftaydı.
Olguların 24 (%96)’ünün korunmasız cinsel ilişki, 1 (%4)’inin ise aşılama yöntemiyle gebe kaldığı görüldü. Olguların birinde doğumun vajinal yolla gerçekleştiği, diğerlerinde ise sezaryen uygulandığı tespit edildi. Doğumla sonuçlanan 32 gebeliğin (bir olguda ikiz gebelik) 26’sında doğumdan önceki CD4+ T lenfosit sayısı ortalama 659±296 hücre/mm3 (minimum=158-maksimum=1294) olup 28’sinde de doğumdan önceki HIV RNA ölçümü saptanabilir düzeyin altındaydı; bir olguda doğumdan önceki RNA değeri kaydedilmemişti. Üç olguda da doğumdan önceki viral yük değerlerinin sırasıyla 100 kopya/ml, 1689 kopya/ml ve 5018 kopya/ml ölçüldüğü görüldü; son iki ölçüm, tek olgunun iki farklı gebeliğine aitti. Doğumdan önceki HIV-1 RNA değerleri saptanabilir düzeyde gelen üç olgu dahil olmak üzere doğum yapan 32 gebenin 12 (%37.5)’sinde anneye travayda intravenöz zidovudin ile profilaksi verilmişti. Bebeklerin tamamına zidovudin şurup ile ortalama altı hafta süreyle profilaksi uygulanmış; bir bebekte zidovudin tedavisine ek olarak altı hafta süreyle lamivudin ve bir kez üç tablet nevirapin, diğer bir bebekte de nevirapin üç tablet kullanılmıştı. Doğumdan önceki HIV-1 RNA değeri 100 kopya/ml olan anneden doğan bebek HIV ile infekte; RNA değeri 1689 kopya/ml olan anneden doğan bebek ise HIV negatifti. HIV-1 RNA düzeyi 5018 kopya/ml olan anneden doğan bebeğin durumu ise annenin takipten çıkmış olması nedeniyle öğrenilemedi. Akıbeti öğrenilemeyen bebek dışında mortalite gözlenmedi.
HIV ile infekte olan bebeğin annesinin, gebelikten dört yıl önce HIV infeksiyonu tanısı aldığı, düzenli takibe gelmediği ve antiretroviral ilaç kullanmadığı tespit edildi. Korunmasız vajinal ilişki yoluyla gebe kalan ve gebeliğinin 31. haftasında kliniğe başvuran olguya hemen antiretroviral tedavi başlanmıştı. Doğumdan yaklaşık bir ay önce yaygın herpes zoster infeksiyonu geçiren olgunun doğumdan bir ay önce yapılan HIV-1 RNA ölçümü 100 kopya/ml, CD4+ T lenfosit sayısı da 180 (%16) idi. Olguya sezaryen uygulanmış, doğum sırasında intravenöz zidovudin profilaksisi, bebeğe de altı hafta süreyle zidovudin şurup verilmişti. Ancak bebekte erken dönemde sitomegalovirus pnömonisi ve retiniti gelişmiş olup bilateral görme kaybı yaşanmıştı. Bu bebek halen hayattadır ve antiretroviral tedavisi devam etmektedir.
İRDELEME
Antiretroviral tedavinin kullanıma girmesi ve yıllar içinde daha erişilebilir ve daha kolay kullanılır olmasıyla birlikte, HIV ile yaşayan kadınların gebelik istek ve talepleri de artmaktadır. Ege Üniversitesi Tıp Fakültesi Hastanesi İnfeksiyon Hastalıkları ve Klinik Mikrobiyoloji Kliniği kohortunda bulunan ve cinsel yönden aktif olan doğurganlık çağındaki kadınların önemli bir bölümünde bir veya daha fazla sayıda gebelik gerçekleşmiş olması bunun göstergesidir. Türkiye’de HIV epidemisinde dikkati çeken önemli noktalardan biri yeni tanı alan olguların yaşlarının giderek düşmeye başlamış olmasıdır. Bu durum hem T.C. Sağlık Bakanlığı’nın resmi verilerinde hem de gerçek yaşam verilerinde açık bir şekilde görülmektedir (5,6,12). Yeni tanılarda en yüksek oran halen 25-34 yaş grubunda görülmekle birlikte 35-44 yaş grubunda bu oranın giderek azaldığı, buna karşılık 20-24 yaş grubunda arttığı dikkati çekmektedir (5,6,12). Her ne kadar yeni tanı alan olgular arasında kadınların oranı yıllar içinde giderek azalmışsa da cinsel aktivitelerine devam eden ve doğurganlık çağındaki HIV ile infekte kadınların oranının yıllar içinde artması bu olguların hem kontrasepsiyon hem de konsepsiyon ve gebelik açısından yönetimlerini giderek daha önemli bir hale getirmektedir.
Anneden bebeğe HIV geçişinin belirli önlemlerin kullanılmasıyla büyük oranda engellenebilir olması; gebe kadınların HIV açısından taranması konusunda ulusal bir politika geliştirilmesini, doğurganlık çağındaki kadınlarda gebeliğin izleyen hekim ile birlikte planlanmasını ve uygun şekilde yönetilmesini, anne ve bebek sağlığı açısından gerekli kılmaktadır. Ülkemizde anneden bebeğe geçiş oranları çok düşük olmakla birlikte, 2021 yılında halen HIV ile infekte olan bebeklerin bulunduğu da yadsınamayacak bir gerçektir (5).
Anneden bebeğe geçişi önlemenin ilk koşulu, gebe kadınları ilk ziyarette ve mümkünse doğumdan kısa süre önce HIV açısından taramaktır. Bu tarama, infekte kadında erken dönemde antiretroviral tedavi başlanmasına ve doğuma kadar HIV RNA düzeyinin azaltılmasına, doğuma yakın tarihte HIV RNA ölçümü halen saptanabilir düzeyde olan kadında ise travay anında profilaksi kullanılmasına olanak tanır. Ülkemizde gebenin ilk ziyareti sırasında HIV taramasının yapılması, ilk olarak T.C. Sağlık Bakanlığı’nın 2018 tarihli Doğum Öncesi Bakım Yönetim Rehberi’nde öneri olarak yer almıştır (13). Ancak bu tarihe kadar bu önerinin yapılmamış olması nedeniyle anneden bebeğe HIV geçişini önleyecek pek çok fırsat kaçırılmıştır. Taramanın genelge ile zorunlu tutulmamış olması nedeniyle özellikle birinci basamakta izlenen gebelerde HIV testinin ne oranda ve ne sıklıkta istendiğine dair elimizde veri bulunmamaktadır; bu durum HIV ile infekte olma olasılığı olan bebekler için fırsatların kaçırılmaya devam edeceği anlamına gelmektedir.
Gebelik planı doğurganlık çağındaki kadınlarla her klinik ziyaretinde konuşulmalı ve cinsel aktivite gösteren ancak gebelik planı olmayan her kadına uygun ve etkin kontraseptif yöntemler önerilmelidir (6,7). HIV ile yaşayan kadınlar tüm kontraseptif yöntemleri kullanabilmektedir. Ancak bazı hormonal kontraseptifler ile antiretroviral ilaçlar arasındaki etkileşimler kontraseptiflerin etkinliğini azaltabileceğinden, kontraseptif seçiminin kullanılan antiretroviral tedaviye uygun olacak şekilde yapılması önem taşımaktadır (14,15).
HIV izlemi yapılan kliniklerde, kontraseptif önerileri yapma konusunda yeterli bir bilgi birikimi ve deneyim bulunmamaktadır; bu öneriler hastalara genellikle kadın hastalıkları ve doğum hekimleri tarafından yapılmaktadır. Bu bağlamda, kadın hastalıkları ve doğum hekimlerinin, HIV ile yaşayan bireyi takip eden hekim ile yakın temas halinde olması, hastanın kullandığı kontraseptif yöntem hakkında hekimini bilgilendirmesi ve infeksiyon hastalıkları hekiminin hastayı kontrasepsiyon gereksinimi konusunda sorgulaması ve gerekli yönlendirmeyi yapması önem taşımaktadır. Çalışmamızda, en sık tercih edilen kontrasepsiyon yöntemi, farklı ülkelerde yapılmış çeşitli çalışmalardan farklı olarak %60.7oranıyla kondom olarak tespit edildi. Bu durumun en olası nedeni; 2017 yılında, belirlenemeyen=bulaştırmayan (B=B) yaklaşımı gündeme gelinceye dek hastalarımıza, HIV bulaşmasını önlemek amacıyla kondom kullanmalarını tavsiye etmemiz olabilir. Doğru kullanıldığı takdirde kondomun koruyuculuk oranı yüksektir; cinsel yolla bulaşan diğer hastalıklardan korunma konusunda da farklı yöntemlere göre üstündür ancak uzun vadede kondom kullanımını sürdürmek kolay değildir. Tablo 2’de sunulmuş olan çalışmalarda genellikle enjeksiyon tipi kontrasepsiyon yöntemlerinin tercih edilen yöntemler olduğu ve HIV ile infekte kadınlarda bu yöntemlerin %25.7 ila %51.4 oranında kullanıldığı tespit edilmiştir (16-24). 2015 yılında yayınlanan ve HIV ile infekte 5153 kadının incelendiği bir çalışmada %9 oranında implant, %40 oranında enjeksiyon ve %14 oranında oral kontrasepsiyon kullanıldığı saptanmıştır (18). Enjeksiyon yoluyla uygulanan hormonal kontrasepsiyonun; aylık, iki aylık veya üç aylık aralıklarla uygulanma imkânının olması, kullanımı sonlandıktan sonra doğurganlığın hızlı geri dönüşü ve cinsel ilişki zamanlamasından bağımsız olarak uygulanabilmesi nedeniyle HIV ile infekte kadınlarda da daha çok tercih edilmektedir (25,26).
Çalışmamızda kadınların %21.5’inin iki veya daha fazla korunma yöntemi kullandığı tespit edildi. Bunun nedenleri sorgulanmamış olmakla birlikte; söz konusu bulgu, olguların gebelikten korunma yöntemleri hakkında yeterince bilgi sahibi olmamalarına ve kullanılan yönteme güvenmemelerine bağlanabilir. Kontrasepsiyon yönteminin, kadın doğum ve infeksiyon hastalıkları hekimlerinin işbirliği ile mümkün olan en az sayıda ve olgunun kişisel özelliklerine uygun olarak seçilmesi ve uygulanması gerekmektedir; doğurganlık çağındaki olgulara kontrasepsiyon yöntemlerinin anlatılması ve kullanımının sorgulanması son derece önemlidir.
Anneden bebeğe HIV geçişinin en yüksek olduğu süreçler; doğum ve doğum sonrası dönemdir. Gebeliğin herhangi bir döneminde başlanacak antiretroviral tedavi ile doğum anında HIV RNA baskılanabildiği takdirde, bebeğin HIV ile infekte olma olasılığı önemli ölçüde azalmaktadır (27, 28). Kılavuzlarda, gebelikte antiretroviral tedaviye başlama zamanına ilişkin öneriler yıllar içinde önemli farklılıklar göstermiştir. Kohortumuzdaki gebelerde de antiretroviral tedavi başlama zamanlarının değişkenlik gösterdiği ve bazı olgularda 32. haftaya kadar geciktiği tespit edildi. Bu durumun nedenleri olarak; olgunun gebelik sırasında tanı alması, gebelik durumu hakkında hekimine geç bilgi vermesi, hekim ziyaretlerini aksatması veya antiretroviral ilaç tedavisine dönemin kılavuzlarına uygun olarak başlanması sayılabilir. Ancak olguların büyük çoğunluğunda doğum anında HIV RNA’nın baskılandığı tespit edildi. HIV RNA düzeyi baskılanamayan olgulardan biri, gebeliğe yakın dönemde yaygın herpes zoster infeksiyonu geçiren ve bebeği HIV ile infekte olan bir bireydir. Diğeri ise iki gebeliğinde de antiretrovirallere ve klinik ziyaretlerine uyumlu olmayan hastadır. Geç başvurusu nedeniyle tedavisine de geç başlanan ve doğumdan kısa süre önce yaygın zona geçiren olgu ve hakkında bilgi alınamayan diğer olgu dışındaki tüm olgularda bebeklere HIV geçişinin engellenmiş olması, bulaşmada en önemli unsurun tedaviye başlama zamanından çok, doğum anında HIV RNA ölçümünün saptanabilir düzeyin altına indirilmesi olduğunu belirten yayınları doğrular niteliktedir (4,6,7).
Gebelikte antiretroviral tedaviye zamanında başlamak kadar, doğru antiretroviral ilaçların kullanılması da önem taşımaktadır. Bazı antiretroviral ilaçların gebelerde kullanımına ilişkin yeterli bilgi bulunmadığı için gebelik sürecinde kullanılmaları önerilmemektedir. Bu bağlamda, anne ve bebek sağlığı ve güvenliğinin en üst düzeyde tutulması açısından gebeliğin, hekim ve hasta arasında yakın iletişim sağlanarak ve önceden planlanarak gerçekleştirilmesi ve gebe kadının yakından izlenmesi son derece önemlidir. Gebelikte antiretroviral tedavi ve sonuçları ayrı bir araştırma konusu olduğu için çalışmamızda bu kapsamda veri sunulmadı.
Türkiye’de anneden bebeğe HIV geçişi; 1985 yılında bildirilen ilk olgudan itibaren 30 Haziran 2019 tarihine kadar bildirilen toplam 175 (%0.8) olguda görülmüştür (5). Çalışmamızda 1 (%3.1) bebeğin HIV ile infekte olduğu görüldü. Dünyada farklı gelişmişlik düzeyine sahip ülkelerde yapılan çalışmalarda, anneden bebeğe HIV geçiş oranının yaklaşık olarak %1.3-9.6 arasında değiştiği görülmektedir (37-41). Çalışmamızdaki oran yüksek gibi görünmekle birlikte, bulaşmanın olduğu olguda anneden bebeğe geçişi önleyecek tüm önlemlerin alınmış olduğu, olgunun gebeliğin geç döneminde kliniğe başvurduğu ve doğuma yakın dönemde HIV RNA düzeyini yükseltebilecek bir infeksiyon geçirmiş olduğu dikkate alındığında, bebeğin intrapartum bulaşma ile infekte olmuş olabileceği kanısı doğmaktadır. HIV infeksiyonunun doğum sürecinde saptanması, gebelikte antiretroviral ilaç tedavisi alınmamış olması ve tespit edilebilir bir viral yük ile doğuma girilmesi, perinatal HIV geçiş riskini artıran en önemli faktörler arasındadır (42). Tayland’da 1437 HIV ile infekte gebe kadında yapılan bir çalışmada; HIV-1 RNA düzeyinin >35 000 kopya/ml olmasının 4.2 kat, doğum için indüksiyon uygulanmasının 2.6 kat ve tokoliz ile prematüre doğumunun gerçekleşmesinin 15.1 kat olmak üzere doğum sürecinde HIV geçişini istatistiksel olarak anlamlı ölçüde artırdığı bildirilmiştir (43). 2020 yılında yayınlanan ve 1641 HIV ile infekte kadındaki 520 doğumun incelendiği bir başka çalışmada doğum sürecinde geçiş oranının %0.82 olduğu bildirilmiştir (44).
Ülkemizde 2007-2015 yılları arasında HIV ile infekte gebe kadınları izleyen bir çalışmada, kadınların %46.9’unun HIV tanısını gebelikten önce, %31.3’ünün gebelik sürecinde, %21.8’inin ise doğum sırasında aldığı tespit edilmiştir (45). Bu da olguların yaklaşık yarısında perinatal bulaşma riskinin ciddi oranda yüksek olduğuna işaret etmektedir. Çalışmamızda da benzer şekilde olguların %28’inin gebelik döneminde HIV tanısı aldığı görüldü. Söz konusu bulgular, gebeliğin hem erken hem de doğuma yakın dönemlerinde HIV taramasının ne kadar önemli olduğunu ortaya koymaktadır.
Sonuç olarak; gebelikte HIV taramasının rutin uygulama haline gelmesi, anne adayında antiretroviral tedaviye erken başlanmasına olanak tanıyarak, anneden bebeğe HIV bulaşma riskini en aza indirmektedir. HIV ile yaşayan bireylerde, gebeliğin hekimle birlikte planlanması, tedaviye doğru zamanda başlanmasına ve annenin sağlık ve esenliğinden ödün vermeden bebeğe en az zarar verecek antiretroviral tedavinin seçilmesine olanak tanıyacaktır. HIV ile yaşayan çocuk doğurma çağındaki bireylerin konsepsiyon ve kontrasepsiyon yöntemleri açısından bilgilendirilmesinin yanı sıra infeksiyon hastalıkları ve kadın hastalıkları ve doğum uzmanlarının yakın iş birliği önem taşımaktadır; bu yaklaşım HIV izleminin standart bir unsuru olarak değerlendirilmelidir.
Hasta Onamı
Olguların dosyaları retrospektif olarak incelendiği için hasta onamı alınmamıştır.
Etik Kurul Kararı
Çalışma, Ege Üniversitesi Tıp Fakültesi Klinik Araştırmalar Etik Kurulu tarafından 02 Mart 2022 tarih ve E.578865 karar numarasıyla onaylanmıştır.
Danışman Değerlendirmesi
Bağımsız dış danışman.
Yazar Katkıları
Fikir/Kavram – D.G.; Tasarım – D.G.; Denetleme – D.G.; Kaynak ve Fon Sağlama – D.G.; Malzemeler/Hastalar – D.G.; Veri Toplama ve/veya İşleme – D.G., D.A.; Analiz ve/veya Yorum – D.G.; Literatür Taraması – D.G., D.A.; Makale Yazımı – D.G., D.A.; Eleştirel İnceleme – D.G.
Çıkar Çatışması
Yazarlar herhangi bir çıkar çatışması bildirmemiştir.
Finansal Destek
Yazarlar finansal destek beyan etmemiştir.
Referanslar
- New report reveals stark inequalities in access to HIV prevention and treatment services for children-partners call for urgent action (21 July 21, 2021) [Internet]. Geneva: Joint United Nations Programme on HIV/AIDS (UNAIDS). [erişim 15 Ocak 2022].https://www.unaids.org/en/keywords/pmtct
- UNAIDS Data 2019 [Internet]. Geneva: Joint United Nations Programme on HIV/AIDS(UNAIDS) [erişim 30 Ocak 2022]. https://www.unaids.org/sites/default/files/media_asset/2019-UNAIDS-data_en.pdf
- Bertolli J, St. Louis ME, Simonds RJ, et al. Estimating the timing of mother-to-child transmission of human immunodeficiency virus in a breast-feeding population in Kinshasa, Zaire. J Infect Dis. 1996;174(4):722-6. [CrossRef]
- John GC, Kreiss J. Mother-to-child transmission of human immunodeficiency virus type 1. Epidemiol Rev. 1996;18(2):149-57. [CrossRef]
- HIV-AIDS İstatistik [Internet]. Ankara: T.C. Sağlık Bakanlığı Halk Sağlığı Genel Müdürlüğü. [erişim 01 Nisan 2021]. https://hsgm.saglik.gov.tr/tr/bulasici-hastaliklar/hiv-aids/hiv-aids-liste/hiv-aids-istatislik.html
- Recommendations for the use of antiretroviral drugs in pregnant women with HIV infection and interventions to reduce perinatal HIV transmission in the United States [Internet]. Rockvill: Office of AIDS Research National Institutes of Health. [erişim 20 Ocak 2022]. https://clinicalinfo.hiv.gov/en/guidelines/perinatal/recommendations-arv-drugs-pregnancy-overview
- European AIDS Clinical Society Guidelines (version 11.0, October 2021) [Internet]. Brussels: European AIDS Clinical Society. [erişim 20 Ocak 2022]. https://www.eacsociety.org/media/final2021eacsguidelinesv11.0_oct2021.pdf
- Peters H, Francis K, Sconza R, et al. UK mother-to-child HIV transmission rates continue to decline: 2012–2014. Clin Infect Dis. 2017;64(4):527-8. [CrossRef]
- Salters K, Loutfy M, Pokomandy A, Money D, Pick N, Wang L. Pregnancy incidence and intention after HIV diagnosis among women living with HIV in Canada. PLoS One. 2017;12(7):e0180524. [CrossRef]
- Blair JM, Hanson DL, Jones JL, Dworkin MS. Trends in pregnancy rates among women with human immunodeficiency virus. Obstet Gynecol. 2004;103(4):663-8. [CrossRef]
- Agangi A, Thorne C, Newell ML. Increasing likelihood of further live births in HIV-infected women in recent years. BJOG. 2005;112(7):881-8. [CrossRef]
- Erdinç FŞ, Dokuzoğuz B, Ünal S, et al. Temporal trends in the epidemiology of HIV in Turkey. Curr HIV Res. 2020;18(4):258-66. [CrossRef]
- Doğum Öncesi Bakım Yönetim Rehberi [Internet]. Ankara: T.C. Sağlık Bakanlığı Halk Sağlığı Genel Müdürlüğü Kadın ve Üreme Sağlığı Dairesi Başkanlığı. [erişim 27 Ocak 2022]. https://khgmsaglikhizmetleridb.saglik.gov.tr/Eklenti/28085/0/dogumoncesibakimyonetimrehberipdf.pdf
- Scarsi KK, Darin KM, Chappell CA, Nitz SM, Lamorde M. Drug-drug interactions, effectiveness, and safety of hormonal contraceptives in women living with HIV. Drug Saf. 2016;39(11):1053-72. [CrossRef]
- Tittle V, Bull L, Boffito M, Nwokolo N. Pharmacokinetic and pharmacodynamic drug interactions between antiretrovirals and oral contraceptives. Clin Pharmacokinet. 2015;54(1):23-34. [CrossRef]
- Blanchard K, Holt K, Bostrom A, et al. Impact of learning HIV status on contraceptive use in the MIRA trial. J Fam Plann Reprod Health Care. 201;37(4):204-8. [CrossRef]
- Heffron R, Donnell D, Rees H, et al; Partners in Prevention HSV/HIV Transmission Study Team. Use of hormonal contraceptives and risk of HIV-1 transmission: a prospective cohort study. Lancet Infect Dis. 2012;12(1):19-26. [CrossRef]
- Pyra M, Heffron R, Mugo NR, et al; Partners in Prevention HSV-HIV Transmission Study and Partners PrEP Study Teams. Effectiveness of hormonal contraception in HIV-infected women using antiretroviral therapy. AIDS. 2015;29(17):2353-9. [CrossRef]
- Marlow HM, Maman S, Moodley D, Curtis S, Reyes LM. HIV status and postpartum contraceptive use in an antenatal population in Durban, South Africa. Contraception. 2015;91(1):39-43. [CrossRef]
- Moodley J, Naidoo S, Wand H, Ramjee G; Microbicides Development Programme Team. Contraception use and impact on pregnancy prevention in women participating in an HIV prevention trial in South Africa. J Fam Plann Reprod Health Care. 2016;42(1):5-11. [CrossRef]
- Chanda MM, Ortblad KF, Mwale M, et al. Contraceptive use and unplanned pregnancy among female sex workers in Zambia. Contraception. 2017;96(3):196-202. [CrossRef]
- Feyissa TR, Harris ML, Forder PM, Loxton D. Contraceptive use among sexually active women living with HIV in western Ethiopia. PLoS One. 2020;15(8):e0237212. [CrossRef]
- Sheth AN, Angert CD, Haddad LB, Mehta CC, Cohn SE. Contraception methods used among women with HIV starting antiretroviral therapy in a large United States clinical trial, 2009-2011. Contraception. 2021;103(4):225-31. [CrossRef]
- Wagner GJ, Mindry D, Hurley EA, et al. Reproductive intentions and corresponding use of safer conception methods and contraception among Ugandan HIV clients in serodiscordant relationships. BMC Public Health. 2021;21(1):156. [CrossRef]
- Schivone G, Dorflinger L, Halpern V. Injectable contraception: updates and innovation. Curr Opin Obstet Gynecol. 2016;28(6):504-9. [CrossRef]
- Barden-O’Fallon J, Mason J, Tluway E, Kwesigabo G, Kamanyi E. Counseling on injectable contraception and HIV risk: Evaluation of a pilot intervention in Tanzania. PLoS One. 2020;15(4):e0231070. [CrossRef]
- Fang G, Burger H, Grimson R, et al. Maternal plasma human immunodeficiency virus type 1 RNA level: a determinant and projected threshold for mother-to-child transmission. Proc Natl Acad Sci USA. 1995;92(26):12100-4. [CrossRef]
- European Collaborative Study. Mother-to-child transmission of HIV infection in the era of highly active antiretroviral therapy. Clin Infect Dis. 2005;40(3):458-65. [CrossRef]
- Zash R, Makhema J, Shapiro RL. Neural-tube defects with dolutegravir treatment from the time of conception. N Engl J Med. 2018;379(10):979-81. [CrossRef]
- European AIDS Clinical Society Guidelines (version 10.0, November 2019) [Internet]. Brussels: European AIDS Clinical Society. [erişim 20 Ocak 2022] https://www.eacsociety.org/media/2019_guidelines-10.0_final.pdf
- Lockman S, Brummel SS, Ziemba L, et al. Efficacy and safety of dolutegravir with emtricitabine and tenofovir alafenamide fumarate or tenofovir disoproxil fumarate, and efavirenz, emtricitabine, and tenofovir disoproxil fumarate HIV antiretroviral therapy regimens started in pregnancy (IMPAACT 2010/VESTED): a multicentre, open-label, randomised, controlled, phase 3 trial. Lancet. 2021;397(10281):1276-92. [CrossRef]
- Ikumi NM, Anumba D, Matjila M. Pharmacokinetics and placental transfer of dolutegravir in pregnancy. J Antimicrob Chemother. 2022;77(2):283-9. [CrossRef]
- Bornhede R, Soeria-Atmadja S, Westling K, Pettersson K, Navér L. Dolutegravir in pregnancy-effects on HIV-positive women and their infants. Eur J Clin Microbiol Infect Dis. 2018;37(3):495-500. [CrossRef]
- Zash R, Holmes L, Diseko M, Jacobson DL, Brummel S, Mayondi G. Neural-tube defects and antiretroviral treatment regimens in Botswana. N Engl J Med. 2019;381(9):827-40. [CrossRef]
- Zash R, Holmes L, Diseko M, Jacobson DL, Brummel S, Mayondi G. Update on neural tube defects with antiretroviral exposure in the Tsepamo study, Botswana (IAC 2020 July 6-10) [Internet]. New York: The National AIDS Treatment Adcocacy Program (NATAP). [erişim 20 Ocak 2020]. https://www.natap.org/2020/IAC/IAC_112.htm
- Zeng QL, Yu ZJ, Ji F, et al. Tenofovir alafenamide to prevent perinatal hepatitis B transmission: A multicenter, prospective, observational study. Clin Infect Dis. 2021;73(9):3324-32. [CrossRef]
- Warszawski J, Tubiana R, Le Chenadec J, et al. Mother-to-child HIV transmission despite antiretroviral therapy in the ANRS French perinatal cohort. AIDS. 2008;22(2):289-99. [CrossRef]
- Derebe G, Biadgilign S, Trivelli M, et al. Determinant and outcome of early diagnosis of HIV infection among HIV-exposed infants in southwest Ethiopia. BMC Res Notes. 2014;7:309. [CrossRef]
- Grignolo S, Agnello R, Gerbaldo D, et al. Pregnancy and neonatal outcomes among a cohort of HIV-infected women in a large Italian teaching hospital: a 30-year retrospective study. Epidemiol Infect. 2017;145:1658-69. [CrossRef]
- Ishikawa N, Dalal S, Johnson C, et al. Should HIV testing for all pregnant women continue? Cost-effectiveness of universal antenatal testing compared to focused approaches across high to very low HIV prevalence settings. J Int AIDS Soc. 2016;19:21212. [CrossRef]
- Global Health Sector Strategy on HIV 2016–2021: Towards Ending AIDS [Internet]. Geneva: World Health Organization (WHO). [erişim 10 Şubat 2022]. https://www.who.int/publications/i/item/WHO-HIV-2016.05
- Del Bianco G, Bell CS, Benjamins LJ, et al. Persistently high perinatal transmission of HIV: assessment of risk factors. Pediatr Infect Dis J. 2014;33(6):e151-7. [CrossRef]
- Jourdain G, Mary JY, Le Coeur S, et al. Risk factors for in utero or intrapartum mother-to-child transmission of human immunodeficiency virus type 1 in Thailand. J Infect Dis. 2007;196(11):1629-36. [CrossRef]
- van der Merwe TA, van Zyl GU, Lombard CJ, Theron GB. Intrapartum human immunodeficiency virus transmission rate in a central hospital in the Western Cape province after universal antiretroviral therapy roll-out. S Afr J Infect Dis. 2020;35(1):192. [CrossRef]
- Sütçü M, Aktürk H, Somer A, et al. Mother-to-child transmisson of HIV: An eight-year experience. Mikrobiyol Bul. 2015;49(4):542-53. [CrossRef]