En Çok Okunanlar
Özet
Amaç: Çalışmanın öncelikli amacı, merkezimizde takip edilen HIV/AIDS olgularında tedavi ve izlem stratejilerini gözden geçirmek ve virolojik başarı oranlarının yıllar içindeki seyrini gözlemlemektir. Ayrıca, olguların epidemiyolojik özelliklerini, klinik ve laboratuvar bulgularını ve sağkalım sürelerini etkileyen faktörler de çalışma kapsamında irdelenmiştir.
Yöntemler: 1996-2015 yılları arasında başvuran HIV ile infekte olgular geriye dönük olarak değerlendirildi. HIV tanısı serolojik olarak doğrulanmış, verilerine ulaşılabilen, 18 yaş ve üzeri olgular çalışmaya alındı. Veriler onar yıllık (1996-2005 ve 2006-2015) iki dilim kapsamında değerlendirildi.
Bulgular: Olguların %80’i erkekti; ortanca (minimum-maksimum) yaş 36.43 (17-77) idi. İlk on yıllık dilimde başvuruların çoğunlukla evre-3, ikinci on yıllık dilimde ise evre-1 veya evre-2’de olduğu görüldü (p=0.00). İlk on yılda, başlangıçtaki CD4+ T lenfositlerinin ortanca (minimum-maksimum) değeri 160 (3-650) hücre/mm3; ikinci dönemde ise 355 (0-1800) hücre/mm3 bulundu (p=0.00). Olguların %94.2’sine tedavi başlanmış olup %70.1’inde 6. ayda ve %78.1’inde toplam takip süresinde HIV RNA saptanabilir düzeyin altına inmişti; HIV RNA ölçümünün negatifleşmesi açısından iki zaman dilimi arasındaki fark anlamlı düzeydeydi (p=0.004). Olguların %12.9’unda AIDS tanımlayan hastalık gelişmişti. İlk ve ikinci dönemde AIDS tanımlayan hastalığı olanların oranı %52.6 ve %11’di (p=0.01). Yan etki oranı %60.8’di; en sık görülen %60.2 oranıyla hiperlipidemiydi. Olguların %6.5’inin öldüğü tespit edilmiş olup en sık karşılaşılan ölüm nedenleri lenfoma (%14.3) ve tüberküloz (%10.9)’du. Çalışma süresi boyunca takip edilen 411 olgunun tahmini sağkalım ortalaması 272 aydı [%95 güven aralığı (GA)=225-320]. HIV RNA’nın negatifleşmemesi, AIDS tanımlayan bir hastalığın bulunması ve başlangıçtaki CD4+ T lenfosit sayısının <200 hücre/mm3 olmasının sağkalım süresini olumsuz etkilediği ve kısalttığı tespit edildi.
Sonuç: Çalışmamızın kohortunda, HIV infeksiyonunun tedavi ve izleminde zaman içinde olumlu gelişmeler olmuş ve ikinci on yıllık zaman diliminde kaskadın ikinci ve üçüncü basamaklarında Birleşmiş Milletler HIV/AIDS Programı (Joint United Nations Programme on HIV/AIDS – UNAIDS)’nın 90-90-90 hedeflerinin üzerine çıkılmıştır. Bu sonucun elde edilmesinde, antiretroviral tedavideki gelişme ve yeniliklerin yanı sıra, uzun yıllardır HIV izlemi yapan Ege Üniversitesi Tıp Fakültesi İnfeksiyon Hastalıkları ve Klinik Mikrobiyoloji Anabilim Dalı sağlık hizmeti ekibinin tüm elemanlarının katkısı yadsınamaz.
GİRİŞ
Birleşmiş Milletler HIV/AIDS Programı (Joint United Nations Programme on HIV/AIDS – UNAIDS) 2014 yılında, insan bağışıklık yetmezlik virusu (human immunodeficiency virus –HIV) infeksiyonunu kontrol altına almak ve ihmal edilebilir düzeye indirmek amacıyla 2020 yılı için 90-90-90 hedeflerini belirlemiştir. Bu hedefler uyarınca HIV ile yaşayan bireylerin %90’ına tanı koyulması, tanı alanların %90’ına ART başlanması ve tedavi başlananların %90’ında virolojik baskılanmanın sağlanması amaçlanmaktadır (1). Bu hedeflere ulaşıldığı takdirde, 2030 yılında 95-95-95 hedefine erişilebileceği ve HIV infeksiyonunun ihmal edilebilir düzeye ineceği öngörülmektedir (2). 2019 yılı sonunda 90-90-90 hedeflerine ulaşmanın mümkün olmadığı belirtilmiş ve 2020 yılında başlayan COVID-19 pandemisi HIV alanında yapılan çalışmaları önemli ölçüde engellemiştir; ancak 2030 yılı için 95-95-95 hedefleri halen geçerliliğini korumaktadır (3).
Son on yıl içinde küresel anlamda yeni HIV infeksiyonlarının sayısında dikkati çeken bir azalma olmuştur. Ancak halen belirli bölgelerde, özellikle de Doğu Avrupa ve ülkemizin de içinde bulunduğu Orta Avrupa ülkelerinde yeni tanıların sayısı hızla artmaya devam etmektedir. Türkiye’de de son on yıl içinde yeni tanıların sayısında dikkati çeken bir artış olmuştur ve artış aynı hızla devam etmektedir (4,5). 2005-2014 yılları arasında Orta Avrupa için Avrupa Hastalık Önleme ve Kontrol Merkezi (European Centre for Disease Prevention and Control – ECDC)’ne bildirilen yeni olguların %70’inden Polonya (%29), Türkiye (%22) ve Romanya (%20)’nın sorumlu olduğu tespit edilmiştir (6). ECDC 2021 raporunda da Türkiye, Orta Avrupa bölgesinde yeni tanıların sayısının en hızlı artış gösterdiği ülkeler arasında yer almıştır (7). Avrupa bölgesini ve dolayısıyla ülkemizi de ilgilendiren bir başka önemli sorun da olguların yaklaşık yarısının geç [CD4+ T lenfosit sayısı ≤350 hücre/mm3 ve/veya edinilmiş bağışık yetmezlik sendromu (acquired immune deficiency syndrome – AIDS) tanımlayan bir hastalık] tanı almasıdır (4,7).
HIV ile infekte bireylerin erken tanımlanması, tanı alanların sağlık sistemine hemen dâhil edilerek sistemin içinde kalmasının sağlanması ve ART’ye erken başlanması, HIV ile yaşayan bireylerin uzun ve kaliteli yaşamasını sağlarken diğer yanda toplum içinde bulaşmaların da azalmasına önemli ölçüde katkı sağlamaktadır (8). Ülkemizde yapılan modelleme çalışmaları, olguların ancak %40-50’sine tanı koyulabildiğine işaret etmektedir (9,10,11). Oysa tanı alıp bir sağlık kuruluşuna yönlendirilen olgularda, HIV kaskadının ikinci ve üçüncü 90 basamaklarında başarı oranları hayli yüksektir (4,9,12).
Çalışmanın öncelikli amacı, merkezimizde takip edilen HIV/AIDS olgularında tedavi ve izlem stratejilerini gözden geçirmek ve virolojik başarı oranlarının yıllar içindeki seyrini gözlemlemektir. Ayrıca, olguların epidemiyolojik özelliklerini, klinik ve laboratuvar bulgularını ve sağkalım sürelerini etkileyen faktörler de çalışma kapsamında irdelenmiştir.
YÖNTEMLER
1996-2015 yılları arasında arasında Ege Üniversitesi Tıp Fakültesi İnfeksiyon Hastalıkları ve Klinik Mikrobiyoloji Anabilim Dalı’na başvuran HIV ile infekte olgular geriye dönük olarak değerlendirildi. Hasta dosyalarına, HIV/AIDS özel takip formlarına ve hastane elektronik bilgi sistemindeki verilerine ulaşılabilen HIV/AIDS tanısı serolojik olarak doğrulanmış 18 yaş ve üzeri olgular çalışmaya alındı. Olgulara ilişkin aşağıdaki parametreler incelendi:
- Demografik özellikler (yaş, cinsiyet, meslek, eğitim ve yaşadığı yer),
- Bulaşma yolu,
- Kliniğe ilk başvurusunda yeni tanı/sevk olması, CD4+ T lenfosit ve HIV RNA düzeyleri, klinik evresi,
- Fırsatçı infeksiyon ve kanserlerin varlığı ve ortaya çıkma zamanları,
- ART başlanıp başlanmadığı,
- Virolojik yanıt olup olmadığı ve olduysa zamanı,
- Başlangıçtaki CD4+ T lenfosit <200 hücre/mm3 olanlarda >200 hücre/mm3 düzeyine çıkana kadar geçen süre,
- İlaç değişikliği olup olmadığı ve varsa nedenleri,
- Virolojik başarısızlık gelişme oranı ve nedenleri,
- Tedavinin kesilmesi ve nedenleri,
- Yan etkilerin sıklığı ve niteliği ile ilaç değişikliğine neden olup olmaması,
- Ölüm gelişip gelişmediği, geliştiyse nedeni,
- Sağkalım süresi ve sağkalım ile ilişkili faktörler.
Hastaların HIV infeksiyonu evresi; ABD Hastalık Kontrol ve Korunma Merkezleri (Centers for Disease Control and Prevention – CDC) 2008 yılı kılavuzundaki sınıflamaya göre kategorize edilip kaydedildi (13). Başvuru sırasında CD4+ T lenfosit sayısı <350 hücre/mm3 olan ve/veya AIDS tanımlayan hastalığı bulunanlar “geç başvuru”, CD4+ T lenfosit sayısı <200 hücre/mm3 olan ve/veya AIDS tanımlayan hastalığı bulunanlar ise “ileri düzeyde başvuru” olarak değerlendirildi. HIV ile ilintili hastalıklar için CDC tarafından yayımlanmış olan AIDS tanımlayan hastalıklar tablosu esas alındı (13). Hastaların günümüzde merkezimiz tarafından hâlen takip edilip edilmediğine, en son poliklinik kontrolünden sonra geçen süre temel alınarak karar verildi; son bir yıl içerisinde HIV polikliniğine başvurmuş olan hastalar halen “takipli”, bir yılı aşkın süredir
polikliniğe başvurmayan hastalar “takip dışı” olarak kabul edildi. Hastaların
polikliniğimize ilk geldiği gün başvuru tarihi olarak kabul edildi.
ART alan hastalarda, altı ay içerisinde HIV RNA ölçümünün saptanabilir düzeyin (50 kopya/ml) altına indirilememesi virolojik başarısızlık olarak değerlendirildi. Hastalara ilişkin tüm demografik, klinik ve laboratuvar parametreleri hasta dosyalarından ve hastanenin elektronik bilgi sisteminden alındı; ölüm tarihleri hakkındaki veriler ise hasta dosyalarına eklenen notlardan ve ölüm bildirim sisteminden elde edildi.
Çalışma, Ege Üniversitesi Tıp Fakültesi Klinik Araştırmalar Etik Kurulu tarafından 18 Ekim 2017 tarih ve 16-12/10 sayılı karar numarasıyla onaylandı.
İstatistiksel Analiz
Verilerin analizinde SPSS (“Statistical Package for the Social Sciences”) versiyon 18.0 programı (IBM Corp., Armonk, NY, ABD) kullanıldı. Nicel değişkenler için ortalama, standart sapma, ortanca, minimum ve maksimum değerler kullanıldı; sürekli değişkenlerin normal dağılıma uygunluğu araştırıldı ve değişkenlerin tümünün normal dağılıma uymadığına karar verildi. Söz konusu değişkenlerin karşılaştırmalarında parametrik olmayan yöntemler kullanıldı. Bağımsız gruplar Mann-Whitney U testi ile karşılaştırıldı. Değişkenler arasındaki ilişki korelasyon yöntemi ile araştırıldı. Nitel değişkenler çapraz tablolar halinde frekans ve yüzdeler halinde sunuldu; dağılımları χ² testi ile karşılaştırıldı. Sağkalım araştırmaları için Kaplan-Meier yöntemi kullanıldı; bağımsız grupların sağkalım karşılaştırmaları Log-Rank testi ile yapıldı. Tüm testlerde tip-1 hata payı için α=0.05 olarak kabul edilmiş olup çift yönlü olarak test edildi; p<0.05 olduğu durumlarda gruplar arasındaki fark istatistiksel olarak anlamlı düzey olarak kabul edildi.
BULGULAR
1996-2015 yılları arasında takip edilen 431 HIV/AIDS olgusu çalışmaya dâhil edildi. Veriler onar yıllık (1996-2005 ve 2006-2015) iki dilim kapsamında değerlendirildi ve kıyaslandı. Tüm grup dikkate alındığında, olguların %79.1 (341/431)’i yeni tanı, %20.9 (90/431)’u ise başka merkezden sevk olarak kliniğe başvurmuştu. Takip sürecinde olguların %77.3 (333/431)’ünün takibinin sürdürülmüş olduğu, %16.2 (70/431)’sinin başka merkeze sevk edildiği veya takipten çıktığı, %6.5 (28/431)’inin ise öldüğü tespit edildi.
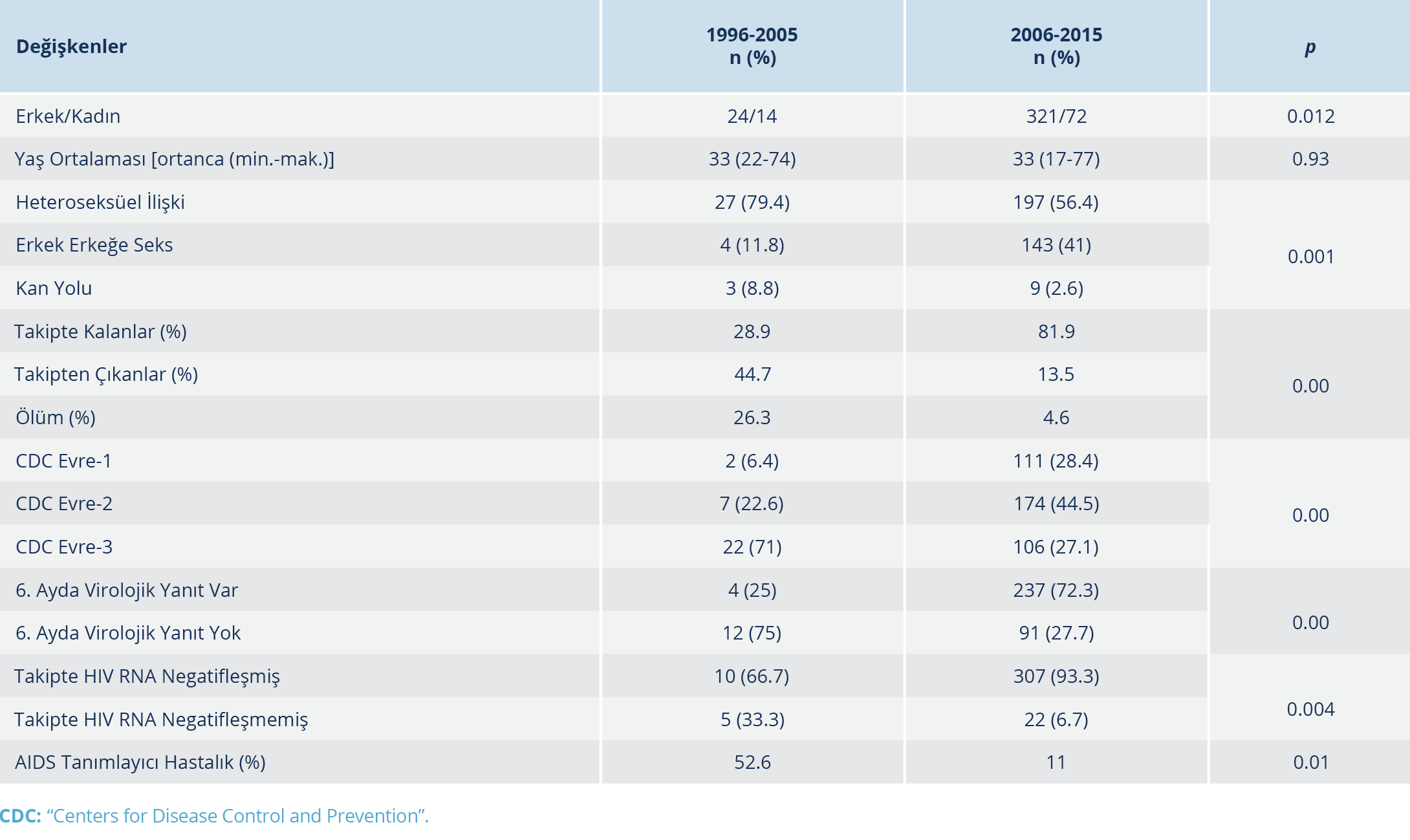
Çalışmaya alınan olguların 345 (%80)’i erkek, 86 (%20)’sı kadındı; 278 (%64.5)’inin İzmir’de ikamet ettiği görüldü. Katılımcıların başvuru anındaki ortanca yaş değeri 36.43 (17-77) yıl olarak bulundu. Çalışmanın ilk zaman diliminde erkek ve kadın olguların sayısı sırasıyla 24 (%63.2) ve 14 (%36.8) idi; ikinci zaman diliminde sayılar önemli ölçüde artmış olup sırasıyla 321 (%81.7) ve 72 (%18.3) olarak tespit edildi (p=0.012) (Tablo 1). Ancak yaş dağılımları açısından iki dönem arasında anlamlı bir fark olmadığı gözlendi; ortanca yaş sırasıyla 33 (22-74) ve 33 (17-77) idi (p=0.93).
HIV’in olası bulaşma yollarına ilişkin 386 (%89.6) olgunun verilerine ulaşılabildi. Heteroseksüel bulaşma tespit edilen olgu sayısı 224 (%52), erkek erkeğe seks veya iki cinsle seks yapan olgu sayısı 147 (%34.1), kan yolu ile bulaşma sayısı 12 (%2.8), vertikal bulaşma sayısı 3 (%0.7) olarak saptandı. Kalan 45 (%10.4) olgunun olası bulaşma yolu “bilinmeyen” olarak sınıflandırıldı. İki zaman dilimi arasında bulaşma yollarında gözlenen fark istatistiksel açıdan anlamlı düzeydeydi (Tablo 1) (p=0.001).
Yirmi yılı kapsayan izlem sürecinin ilk zaman diliminde olguların %28.9’unun takipte kaldığı, %44.7’sinin takipten çıktığı, %26.3’ünün öldüğü tespit edildi; ikinci zaman diliminde ise bu oranlar sırasıyla %81.9, %13.5 ve %4.6 olarak bulundu. Takipte kalan olguların sayısının ikinci on yıllık dilimde anlamlı düzeyde arttığı, takipten çıkanların ve ölenlerin sayılarının ise anlamlı düzeyde azaldığı görüldü (p=0.00) (Tablo 1).
CDC’nin kılavuzuna uygun olarak kayıtlı 431 olgunun 422’sinin başvuru anındaki HIV infeksiyonu evresinin sınıflaması yapıldı; olguların 113 (%26.8)’ü evre-1, 181 (%42.9)’i evre-2 ve 128 (%30.3)’i evre-3 olarak değerlendirildi. AIDS aşaması olan evre-3’te başvuran olguların sayısının ikinci on yılda azaldığı ve ilk başvuruların çoğunlukla evre-1 veya evre-2’de olduğu görüldü (p=0.00) (Tablo 1).
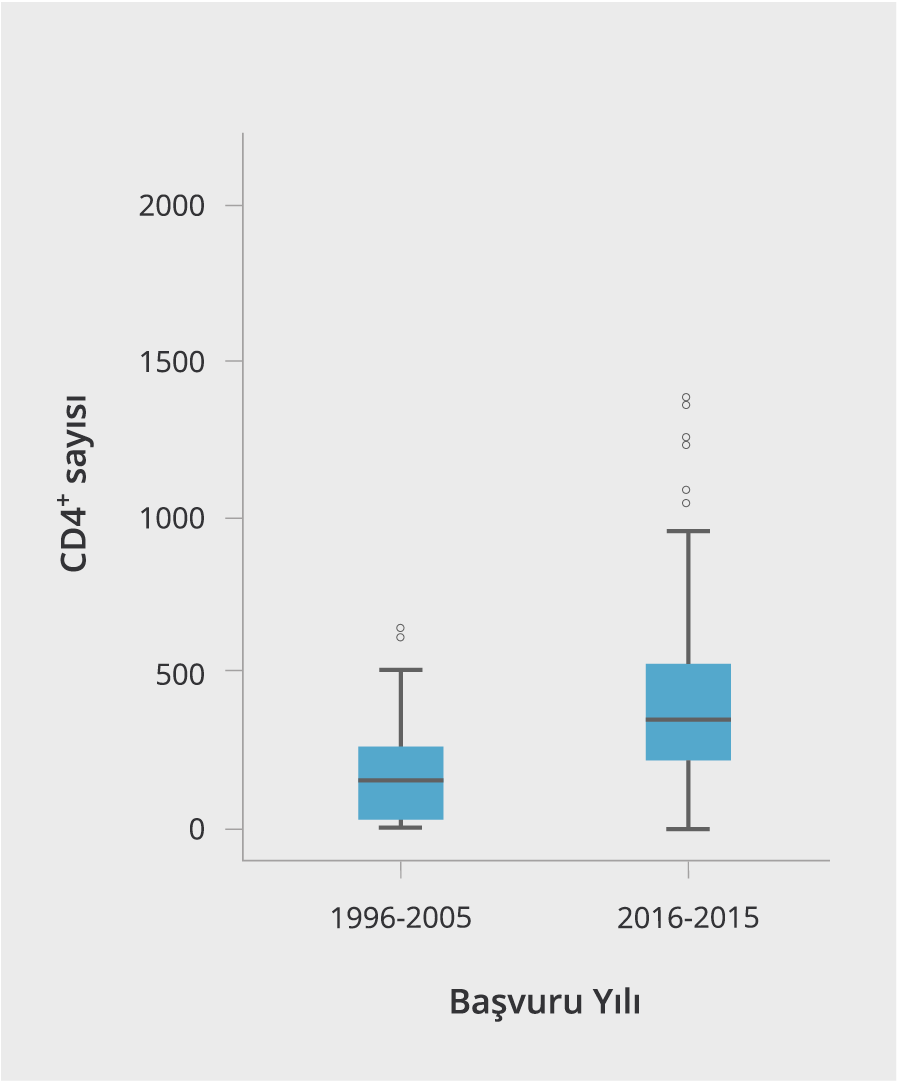
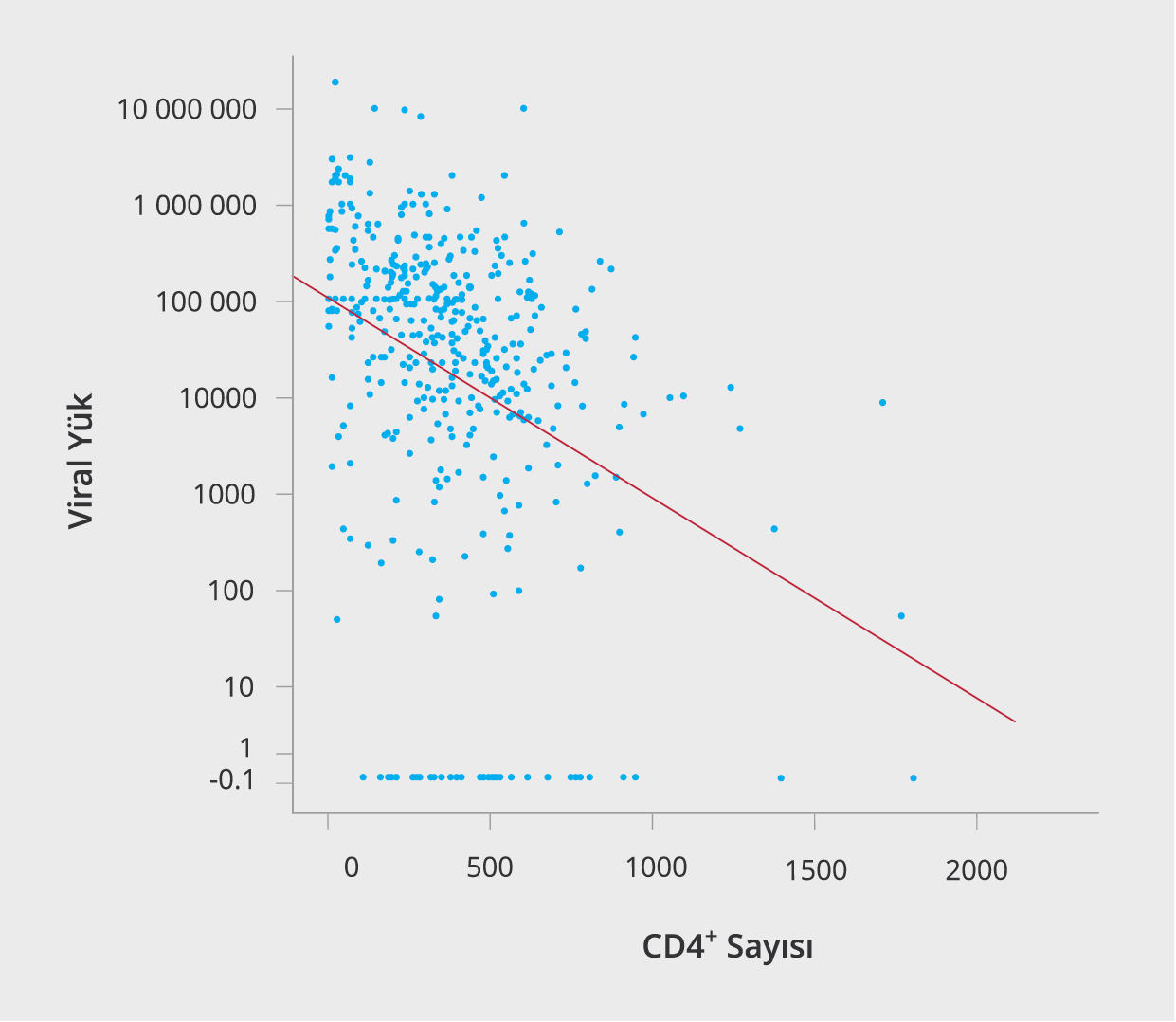
Çalışmanın ilk on yıllık diliminde, başvuru anındaki CD4+ T lenfositlerinin ortanca değeri 160 (3-650) hücre/mm3 iken, 2006-2015 yılları arasında bu değer 355 (0-1800) hücre/mm3 bulundu (p=0.00). Başvuru anındaki ortanca HIV-RNA değeri; 1996-2005 yılları arasında 75 000 (200- 1 000 001) kopya/ml ve 2006-2015 yılları arasında 39 685 (0-19 000 000) kopya/ml olarak tespit edildi (p=0.169) (Şekil 1). CD4+ T lenfositlerinin sayısı ile HIV RNA düzeyi arasında negatif bir korelasyon (r=-0.396) olduğu saptandı (Şekil 2).
Çalışmanın ilk 10 yılında olguların 28 (%75.8)’inin ve ikinci on yılda ise 194 (%49.5)’ünün geç dönemde başvurduğu görüldü. İleri evrede başvuran olguların oranları ise ilk on yılda %65.5 ve ikinci on yılda %22.7 idi (p=0.00).
Olguların 406 (%94.2)’sına tedavi başlanırken, 25 (%5.8)’inin tedavisiz izlendiği görüldü. Tedavi başlanan 406 olgudan 344 (%84.7)’ü tedavi başlandıktan sonra 6. ayda virolojik yanıt açısından değerlendirilmiş olup 241 (%70.1)’inde virolojik yanıtın elde edildiği, 103 (%29.9)’ünde virolojik yanıtın sağlanamadığı anlaşıldı. Olguların 38 (%9.4)’inde kliniğe başvuru anında HIV RNA negatifti; bu olgular dışarıda tutularak yapılan istatistiksel analizde, iki zaman dilimi arasında 6. ayda virolojik yanıt elde etme açısından anlamlı düzeyde bir fark olduğu tespit edildi (p=0.00) (Tablo 1). ART başlanan 406 olgu, toplam takip süresince HIV RNA ölçümünün negatifleşmesi açısından da değerlendirildi; olguların 317 (%78.1)’sinde HIV RNA ölçümünün saptanabilir düzeyin altına indiği, 27 (%6.6)’sinde negatifleşme sağlanamadığı, 24 (%5.9)’ünde de HIV RNA ölçümüne ilişkin bilgi olmadığı anlaşıldı. İki zaman dilimi arasında HIV RNA ölçümünün saptanabilir düzeyin altına inmesi açısından istatistiksel açıdan anlamlı düzeyde fark tespit edildi (p=0.004) (Tablo 1).
Takip sürecinde, 406 olgunun 158 (%38.9)’inde tedavi değişikliği yapıldığı görüldü. Tedavi değişikliği nedenleri; 76 olguda (%48.1) yan etki, 18 (%11.4) olguda viral yükün baskılanamaması, 16 (%10.1) olguda bilinmeyen nedenler, 12 (%7.6) olguda rejimin basitleştirilmesi, 9 (%5.7) olguda düzensiz kullanım, 8 (%5) olguda olası direnç, 5 (%3.2) olguda ilacın temin edilememesi, 5 (%3.2) olguda kullanım zorluğu, 4 (%2.5) olguda ilaç etkileşimi ve 5 (%2.2) olguda gebelik (n=5; %2.2) olarak tespit edildi.
AIDS tanımlayan hastalık açısından 410 olgunun verilerine ulaşıldı; 53 (%12.9) olguda AIDS tanımlayan hastalık geliştiği ve bunların 44 (%83)’ünün bu nedenle hastaneye yatırıldığı anlaşıldı. Çalışmanın ilk ve ikinci on yıllık diliminde AIDS tanımlayan hastalığı olan olguların oranları sırasıyla %52.6 ve %11 olarak saptandı (p=0.01) (Tablo 1). Olgularda tespit edilen AIDS tanımlayan hastalıkların dağılımı; tüberküloz (%38), Kaposi sarkomu (%11), sitomegalovirus (CMV) infeksiyonu (%10), Toksoplazma gondii ansefaliti (%8), non-Hodgkin lenfoma (%8), Cryptosporidium spp. infeksiyonu (%6), Pneumocystis jirovecii pnömonisi (%5), JC virusuna (JCV) bağlı progresif multifokal ansefalopati (%5), yaygın varisella zoster virusu (VZV) infeksiyonu (%5), yaygın Candida spp. infeksiyonu (%2), Mycobacterium avium kompleksi infeksiyonu (%2) ve herpes simpleks virusu (HSV) infeksiyonu (%2) şeklindedir.
Kliniğe başvuran olguların 104 (%24.1)’ünün CD4+ T lenfosit sayısı <200 hücre/mm3 olarak tespit edildi. Olguların 90 (%86.5)’ında takip sürecinde CD4+ T lenfosit sayısı >200 hücre/mm3 düzeyine ulaşırken, 14 (%13.5)’ünde sayı bu düzeyin altında kalmıştı. CD4+ T lenfosit sayıları <200 hücre/mm3 olup takip sürecinde >200 hücre/mm3 düzeyine yükselenlerin oranı ilk ve ikinci zaman diliminde sırasıyla %57.1 ve %91.1 olarak bulundu (p=0.003).
CD4+ T lenfosit <200 hücre/mm3 olan olguların CD4+ T lenfosit sayılarının >200 hücre/mm3 olmasına kadar geçen süre 1996-2005 yılları arasında ortanca 9 (1-24) ay, 2006-2015 yılları arasında ise 3 (1-50) ay bulundu.
ART kullanan 406 olgunun üçünde ilk on yılda, 28’inde ise ikinci on yılda olmak üzere toplam 31(%7.6) olguda virolojik başarısızlık geliştiği görüldü. Sayıların az olması nedeniyle iki grup arasında istatistiksel karşılaştırma yapılamadı. Virolojik başarısızlığın nedeni; olguların 18 (%58)’inde ART’nin düzensiz kullanılması, 6 (%19.3)’sında antiretroviral ilaçlara direnç, 1(%3.2)’inde ise hem antiviral tedavinin düzensiz kullanımı hem de ilaçlara direnç olarak belirlendi; olguların 6 (%19.3)’sında başarısızlığın nedeni bilinmemektedir.
İzlem sürecinde, verilerine ulaşılabilen 384 olgunun 262 (%60.8)’sinde yan etki geliştiği tespit edildi. Olguların 231 (%60.2)’inde hiperlipidemi, 39 (%10.2)’unda kemik metabolizmasında bozukluk, 30 (%7.8)’unda psikiyatrik bozukluk, 17 (%4.4)’sinde anemi, 14 (%3.6)’ünde karaciğer fonksiyon testlerinde bozukluk, 14 (%3.6)’ünde böbrek fonksiyon testlerinde bozukluk, 10 (%2.6)’unda gastrointestinal sistem (GİS) bozukluğu, 2 (%0.5)’sinde kas enzimlerinde bozukluk ve cilt lezyonları ve 1 (%0.3)’inde nörolojik yan etkiler görüldü. En sık görülen yan etki olan hiperlipideminin ilk on yıllık dönemde oranı %93.3 olup ikinci on yıllık dilimde bu oran %67.2’ye düşüyordu; bu fark istatistiksel olarak anlamlı bir düzeyde değildi (p=0.44). Söz konusu yan etkilerin kullanılan antiretroviral ilaçlarla ilişkisi bilinmemektedir.
Takip sürecinde olguların 32 (%7.4)’sinde tedaviye ara verildiği gözlendi. Bunun nedeni 24 (%78.1) olguda uyumsuzluk, 3 (%9.4) olguda ilaç yan etkisi, 2 (%6.3) olguda ilacın bulunamaması, 1 (%3.1) olguda akut hepatit B gelişmesi ve 1 (%3.1) olguda ilacın yanlış kullanılması idi.
Olguların 28 (%6.5)’i hayatını kaybetmişti. Ölümlerin %35.7’si 1996-2005 yılları arasında, %64.3’ü ise 2006-2015 yılları arasında gerçekleşmiş olup 11 (%39.2) olgunun ölüm nedeni tespit edilemedi. Ölüm nedeni bilinenlerin 2 (%14.3)’sinin lenfoma, 3 (%10.9)’ünün tüberküloz, 2 (%7.1)’sinin AIDS tükenmişlik sendromu, 2 (%7.1’sinin) çoklu organ yetmezliği, 2 (%7.1)’sinin konjestif kalp yetmezliği, 1 (%3.8)’inin lösemi, 1(%3.8)’inin diyabetik ketoasidoz, 1 (%3.8)’inin aspirasyon ve 1 (%3.8)’inin de ateşli silahla vurulma sonucu hayatını kaybettiği tespit edildi.
Ölüm nedeni bilinen 17 olgunun 2 (%11.8)’si ilk on yıllık dilimde, 15 (%88.2)’i ikinci on yıllık dilimde hayatını kaybetmişti. Bunların 9 (%52.9)’u AIDS ile ilişkili olarak, 8 (%47.1)’i AIDS dışı nedenlerden dolayı ölmüştü. İlk dönemde ölüm nedeni bilinen iki hasta AIDS ile ilişkili nedenlerden hayatını kaybederken, ikinci dönemdeki15 hastanın 7 (%46.7)’si AIDS ile ilişkili olarak, 8 (%53.3)’i AIDS dışı nedenlerden dolayı ölmüştü. Ölüm nedenleri açısından iki grup arasında istatistiksel açıdan anlamlı düzeyde fark saptanmadı (p=0.471).
Çalışma süresi boyunca takip edilen ve verilerine ulaşılabilen 431 olgudan 411’nin tahmini sağkalım ortalaması 272 (%95 GA=225-320) ay olarak tespit edildi. HIV RNA değerlerine ulaşılabilen 379 olgudan, HIV RNA ölçümü saptanabilir düzeyin altına inenlerin tahmini sağkalım ortalaması 325 (%95 GA=302-348) ay iken, HIV RNA düzeyi negatifleşmeyenlerin ortalaması ise 107 ay (%95 GA=66-148) idi (p=0.00).
AIDS tanımlayan hastalığın sağkalım süresine etkisi açısından 410 olgu değerlendirildi. AIDS tanımlayan hastalığı olanların tahmini sağkalım ortalaması 175 (%95 GA=146-203) ay ve AIDS tanımlayan hastalığı olmayanların tahmini sağkalım ortalaması 295 (%95 GA=244-346) ay olarak bulundu (p=0.00).
Klinik evreleri belirlenen 407 olgu, klinik evrenin sağkalım süresine etkisi açısından değerlendirildi. CD4+ T lenfosit sayıları >200 hücre/mm3 olan olgularda tahmini sağkalım süresi 314 (%95 GA=260-367) ay, <200 hücre/mm3 olanlarda ise 184 (%95 GA=163-204) olarak tespit edildi (p=0.00).
İRDELEME
Bu çalışma, Ege Üniversitesi HIV kohortunda, karma antiretroviral tedavinin kullanıma girdiği 1996 yılından itibaren yapılan izlem ve tedavinin, bunların sonuçlarının ve olguların epidemiyolojik özelliklerinin onar yıllık iki zaman dilimde önemli farklılıklar sergilediğini ortaya koymaktadır. Tüm dünyada yeni HIV olgularının sayısı azalma eğilimi göstermekteyken (14, 15), artış eğiliminin sürdüğü Orta ve Doğu Avrupa bölgesinde, Türkiye artışın en yüksek olduğu üç ülkeden biri durumundadır (6). Son 10 yıl içinde T.C. Sağlık Bakanlığı’na bildirimi yapılan yeni olgu sayıları, dikkati çekecek düzeyde artmıştır ve artmaya devam etmektedir (5). Yapılan çalışmalar, mevcut durumun sürmesi halinde 2040 yılında yıllık yeni olgu sayısının 150 000, toplam olgu sayısının da 400 000 civarına yaklaşacağını öngörmektedir (9). Bu bağlamda, HIV ile yaşayan bireylerin tanımlanması ve en kısa zamanda ART’ye başlanması, virolojik açıdan baskılanması ve sağlık sisteminin içinde tutulması son derece önemlidir. Dolayısıyla HIV ile yaşayan bireylerin izlendiği sağlık kurumlarının, kendi hasta profillerini tanıması, izlemde güçlü ve zayıf yönlerini bilmesi, başarı oranlarını izlemesi, zaman içindeki değişimi görmesi ve eksik kalan yönlerini tamamlaması kritik öneme sahiptir. Bu çalışma, Ege Üniversitesi kohortunun yıllar içindeki performansını göstermektedir ve bildiğimiz kadarıyla, ülkemizde iki farklı dönemi kıyaslayan ilk kohort çalışmasıdır.
Ülkemizde yeni tanı alan olguların profillerinin yıllar içinde ciddi değişiklikler gösterdiği daha önce başka çalışmalarda da bildirilmiştir. T.C Sağlık Bakanlığı istatistiklerinde de bu değişimi görmek mümkündür (5). Ancak kohortlarda bildirilen değişimin, bakanlığa yapılan bildirimlerdekine kıyasla çok daha büyük oranda olduğu bilinmektedir. Örneğin, 2011-2016 yıllarını kapsayan bir çalışmada heteroseksüel bulaşma oranı %69’dan %50’ye düşerken, erkek erkeğe seks yoluyla bulaşma oranları iki kat artarak %16’dan %31’e yükselmiştir; T.C. Sağlık Bakanlığı’nın aynı dönemi kapsayan istatistiklerinde ise bu oranlar sırasıyla %42 ve %11.4 şeklinde bildirilmiştir (4). Bulaşma yolu bilinmeyenlerin oranları arasında da ciddi farklılıklar görülmektedir; T.C. Sağlık Bakanlığı verilerine göre %42.7 olan bu oran, belirtilen çalışmada %12.5 bulunmuştur (4). Çalışmamızın verileri de erkeklerle seks yapan erkekler arasında bulaşma oranlarının yıllar içinde dikkati çekecek düzeyde yükseldiğini ve bulaşma yolu bilinmeyenlerin oranının, diğer birçok kohortta olduğu gibi, T.C. Sağlık Bakanlığı’nın verilerinin aksine, hayli düşük düzeyde olduğunu ortaya koymaktadır. Bunun temel nedeni, özellikle erkeklerle seks yapan erkeklerin ilk başvuru anında kurumlara ve hekimlere duyduğu güvensizlik nedeniyle bulaşma yolunu söylemekten kaçınmasıdır. Zaman içinde hekim ve hasta arasındaki güvenin tesis edilmesi sonucu doğru bulaşma yolu dosyaya kaydedilmekle birlikte bakanlığa bu düzeltme bildirilmemektedir.
Geç tanı alan olgu sayıları, tüm Avrupa’da olduğu gibi, ülkemizde de yüksek oranlardadır. Dünya Sağlık Örgütü, Avrupa bölgesinde 2020 yılında geç tanı alanların oranı halen %50 olarak bildirilmektedir (7). Ülkemizde yapılan çalışmalarda da bu oranın benzer olduğu görülmektedir (4, 16). Çalışmamızda ilk ve ikinci on yıllık dilimler kıyaslandığında, ikinci zaman diliminde geç tanı alan olgu sayısında anlamlı bir azalma olmasına karşın, yine de olguların neredeyse yarısının geç tanı almış olduğu tespit edildi. Benzer şekilde, CDC kılavuzunda yer alan tanıma göre ileri evrede tanı alanların da sayısı, ikinci zaman diliminde dikkati çekecek ölçüde azalmıştır; ancak yine de olguların dörtte birinden fazlasını oluşturmaktadır. Ülkemizdeki gerçekleştirilen yıllık HIV test sayısı 7-8 milyon düzeyine ulaşmıştır; bu rakamlar fazla yüksek gibi görünmekle birlikte gerçekleştirilen testler HIV infeksiyonu açısından riski daha yüksek hassas (kilit) gruplar için bir test stratejisinin sonucu değil genel toplumun taranması kaynaklıdır.
UNAIDS, 2014 yılında HIV infeksiyonunu kontrol altına almak ve ihmal edilebilir düzeye indirmek amacıyla 2020 yılı için 90-90-90 hedeflerini belirlemiştir. Orta Avrupa ülkeleri arasında 2018 yılında dahi bu hedefe ulaşan hiçbir ülke olmamasına karşın, kohortumuzda ART başlama oranları, 90-90-90 hedeflerinde öngörülenin çok üzerinde olup Batı Avrupa ülkelerindeki oranlara eşdeğerdir (17). Ülkemizde yapılmış diğer çalışmalarda da bu düzeyde olmasa da birçok Avrupa ülkesinden bildirilenlerden daha yüksek oranlar elde edilmiştir (4,12,18,19,20). Bunun temel nedenlerinden biri, 2012 yılında Amerika Birleşik Devletleri HIV ile Yaşayan Erişkin ve Ergenlerde Antiretroviral İlaçların Kullanımı Kılavuzu’na, “CD4+ T lenfosit sayısına bakılmaksızın herkese ART başlanması” önerisinin BIII kanıt düzeyi ile dâhil edilmesinin ardından (21), 2013 yılında yayımlanmış olan T.C. Sağlık Bakanlığı HIV/AIDS Tanı Tedavi Rehberi’nde (22) de yer alması ve aynı tarihte Avrupa’da kabul görmese de Türk hekimleri tarafından uygulanmaya başlanmış olmasıdır. Bunun yanı sıra, genel sağlık sigortası sistemine geçildikten sonra ART’ye erişimin önünde ciddi bir engel ve kısıtlama kalmaması ve HIV ile yaşayan bireylerin izleminin özenle ve yakın ilgi ile yapılması da bu sonuca katkıda bulunmuş olabilir.
Benzer şekilde, kohortumuzda üçüncü 90’ı ifade eden virolojik başarı elde etme basamağında da seviyenin hayli yüksek olduğu tespit edildi. Tüm grup dikkate alındığında, ilk 6 ayda ve toplam izlem süresinde virolojik baskılanma oranları hedefin altında görünse de iki zaman dilimi karşılaştırıldığında, birinci zaman diliminde %25 ve %66.7 oranlarıyla çok daha düşük olmasına karşın, ikinci zaman diliminde aynı oranların %73.3 ve %93.3’e yükseldiği gözlendi. Bu koşullarda, ikinci zaman diliminde, UNAIDS’in virolojik baskılanma için hedeflediği %90 hedefinin üzerine çıkıldığı söylenebilir. Bu önemli farklılığın olası nedenleri olarak; yeni antiretroviral ilaçların kullanımının daha kolay olması, yan etki profillerinin daha tolere edilebilir olması nedeniyle hasta uyumunun geçmişe göre daha yüksek olması ve ülkemizde 2012 yılında ilk kez ruhsatlandırılmış olan entegraz inhibitörü grubuna ait ilaçların HIV RNA düzeyini diğer ilaç gruplarına göre daha hızla baskılamaları şeklinde sıralanabilir (23-26).
Çalışmadaki virolojik başarısızlık oranlarının son derece düşük olması sevindiricidir. Diğer birçok çalışmada belirtildiği ve beklendiği üzere, her iki zaman diliminde de virolojik başarısızlığın, tedaviyi uyumsuz kullananlarda ve/veya antiretroviral ilaçlara direnci bulunanlarda geliştiği görülmektedir (19,27,28). Ancak bu olgularda tedavi değişikliği yapılarak virolojik başarı sağlanıp sağlanmadığı konusunda veri toplanmadı.
Olguların önemli bir bölümünde yan etki geliştiği gözlendi. Özellikle hiperlipideminin en sık görülen yan etki olması ve çalışmanın ilk 16 yılında gözlenen yan etki oranları günümüzde kullanılan ilaçlar yerine daha fazla olan proteaz ve nonnükleozid revers transkriptaz inhibitörlerinin kullanılmış olmasına bağlanabilir (29-31). Nitekim çalışmanın iki zaman dilimi karşılaştırıldığında, hiperlipidemi oranlarının ikinci dilimde azaldığı görülmektedir.
Çalışmamızda, %7.4 olan tedaviye ara verme oranı, Türkiye’de yakın tarihte yapılmış geniş çaplı bir kohort (HIV-TR kohortu) çalışmasında bildirilen %11.6 oranına yakın bulundu (18). Ancak iki çalışma arasında tedavinin kesilme nedenleri açısından önemli farklılıklar bulunmaktadır. Çalışmamızın kohortunda, olguların %78.1’inde ilaç, tedaviye uyumsuzluk nedeniyle kesilirken, yan etki nedeniyle tedavinin kesilme oranı %9.4’tür. Buna karşılık HIV-TR kohortunda olguların %45’inde toksisite/intolerans nedeniyle tedaviye ara verilmiştir (18). Bu farkın en olası nedeni; tedaviye ara verme gerekçesi olarak hasta dosyasında uyumsuzluk bildirilmekle birlikte, söz konusu uyumsuzluğun muhtemel nedeni ilaç yan etkisi/intoleransı olmasıdır. Ayrıca, HIV-TR kohortu, tedavi seçeneklerinin bol olduğu 2011-2017 yıllarını kapsarken, çalışmamızda ilaç seçeneklerinin son derece sınırlı olduğu bir zaman diliminde izlenen hastalar da kohorta dâhil edildi. Seçeneklerin sınırlı olduğu durumlarda ciddi bir yan etki olmadığı takdirde ilaç değişikliği yerine yan etkinin semptomatik yaklaşım ile giderilmesi yolu seçilmiş olabilir.
AIDS tanımlayan hastalığı olan ve/veya CD4+ T lenfosit sayısı <200 hücre/mm3 olan bireylerde klinik tablonun ağır seyirli ve ölümle sonuçlanma ihtimalinin yüksek olduğu, öte yandan HIV RNA düzeyinin hızla baskılanmasının, bağışıklığın yeniden yapılanmasını sağlayacağından, morbidite ve mortaliteyi azaltacağı gösterilmiştir (32). Söz konusu çalışmalarda elde edilen sonuçlar uyarınca, 2015 yılından bu yana CD4+ T lenfosit sayısından ve HIV RNA düzeyinden bağımsız olarak yeni tanı alan her olguya en kısa zamanda ART başlanması önerilmektedir (21,33,34). Nitekim çalışmamızda da başlangıçtaki CD4+ düzeyi >200 hücre/mm3 olan, AIDS tanımlayıcı hastalığı bulunmayan ve virolojik başarı sağlanmış bireylerde sağkalım süresi, diğerlerine görece anlamlı ölçüde daha yüksek bulundu ve ölüm sayıları da daha az tespit edildi. Bu bulgu, çalışmanın ilk zaman dilimi ile kıyaslandığında ikinci zaman diliminde ileri evre hastalıkla başvuran hasta sayısının az olmasına, 2012 yılından itibaren tüm olgulara CD4+ T lenfosit sayısından ve HIV RNA düzeyinden bağımsız olarak ART başlanmasına, dolayısıyla virolojik baskılanmanın daha yüksek oranda elde edilmesine ve CD4+ T lenfosit sayısının daha hızlı yükselmesine bağlanabilir.
Sonuç olarak; tüm dünyadaki gelişmelerle paralel olarak, Ege Üniversitesi HIV kohortunda da HIV infeksiyonunun tedavi ve izleminde zaman içinde olumlu gelişmeler yaşanmıştır. Kohortta, özellikle de ikinci on yıllık zaman diliminde UNAIDS hedeflerinin ikinci ve üçüncü basamaklarındaki hedefler üzerine çıkılmış olması sevindiricidir. Bu sonucun elde edilmesinde, antiretroviral tedavide elde edilen gelişme ve yenilikler önemli rol oynarken, uzun yıllardır HIV izlemi yapan Ege Üniversitesi Tıp Fakültesi sağlık hizmeti ekibinin tüm elemanlarının katkısı da yadsınamaz.
Etik Kurul Kararı
Çalışma, Ege Üniversitesi Tıp Fakültesi Klinik Araştırmalar Etik Kurulu tarafından 18 Ekim 2017 tarih ve 16-12/10 sayılı karar numarasıyla onaylanmıştır.
Danışman Değerlendirmesi
Bağımsız dış danışman.
Yazar Katkıları
Fikir/Kavram – D.G.; Tasarım – D.G., H.P.; Denetleme – D.G., H.P.; Kaynak ve Fon Sağlama – D.G.; Malzemeler/Hastalar – D.G., H.P.; Veri Toplama ve/veya İşleme – D.G., H.P.; Analiz ve/veya Yorum – D.G.; Literatür Taraması – G.G., D.A., D.G.; Makale Yazımı – G.G., D.A., D.G.; Eleştirel İnceleme – D.G., G.G., D.A.
Çıkar Çatışması
Yazarlar herhangi bir çıkar çatışması bildirmemiştir.
Finansal Destek
Yazarlar finansal destek beyan etmemiştir.
Referanslar
- Bain LE, Nkoke C, Noubiap JJN. UNAIDS 90–90–90 targets to end the AIDS epidemic by 2020 are not realistic: comment on “Can the UNAIDS 90–90–90 target be achieved? A systematic analysis of national HIV treatment cascades”. BMJ Glob Health. 2017;2(2):e000227. [CrossRef]
- Global AIDS update 2016. [Internet]. Geneva: Joint United Nations Programme on HIV/AIDS (UNAIDS). [erişim 13 Mart 2022]. https://www.unaids.org/en/resources/documents/2016/Global-AIDS-update-2016
- Global AIDS update 2020. [Internet]. Geneva: Joint United Nations Programme on HIV/AIDS (UNAIDS). https://www.unaids.org/en/resources/documents/2020/global-aids-report
- Erdinc FS, Dokuzoguz B, Unal S, et al. Temporal trends in the epidemiology of HIV in Turkey. Curr HIV Res. 2020;18(4):258-66. [CrossRef]
- HIV-AIDS İstatistik [Internet]. Ankara: T.C. Sağlık Bakanlığı Halk Sağlığı Genel Müdürlüğü Bulaşıcı Hastalıklar ve Erken Uyarı Dairesi Başkanlığı. [erişim 13 Mart 2022]. https://hsgm.saglik.gov.tr/tr/bulasici-hastaliklar/hiv-aids/hiv-aids-liste/hiv-aids-istatislik.html
- Gökengin D, Oprea C, Uysal S, Begovac J. The growing HIV epidemic in Central Europe: a neglected issue? J Virus Erad. 2016;2(3):156-61.
- HIV/AIDS surveillance in Europe 2021 [Internet]. Solna: European Centre for Disease Prevention and Control (ECDC). [erişim 13 Mart 2022]. https://www.ecdc.europa.eu/en/publications-data/hiv-aids-surveillance-europe-2021-2020-data
- Brault MA, Spiegelman D, Hargreaves J, Nash D, Vermund SH. Treatment as prevention: concepts and challenges for reducing HIV incidence. J Acquir Immune Def Synd. 2019;82(2):S104. [CrossRef]
- Yaylali E, Gokengin D, Korten V, et al. Modelling the future of HIV in Turkey: disease implications of improving prevention, diagnosis and treatment [Abstract]. In: Abstracts of HIV Glasgow Congress 2020 (Glasgow, October 5-8, 2020). 2020:96-7.
- Sayan M, Hınçal E, Şanlıdağ T, Kaymakamzade B, Sa’ad FT, Baba IA. Dynamics of HIV/AIDS in Turkey from 1985 to 2016. Qual Quant. 2018;52(1):711-23. [CrossRef]
- Berktaş M, Unal S. Türkiye’de HIV enfeksiyonu ile yaşayan yetişkin sayısının tahmin edilmesi [Özet]. In: HIV/AIDS Kongresi 2017 (16-19 Kasım 2017, Antalya) Özet Kitabı.
- Mete B, Gunduz A, Bolukcu S, et al. HIV care in Istanbul, Turkey: How far is it from the UNAIDS 90–90–90 targets? Int J STD AIDS. 2019;30(13):1298-303. [CrossRef]
- Schneider E, Whitmore S, Glynn MK, Dominguez K, Mitsch A, McKenna MT. Revised surveillance case definitions for HIV infection among adults, adolescents, and children aged< 18 months and for HIV infection and AIDS among children aged 18 months to< 13 years—United States. MMWR. 2008;57(RR-10):1-12.
- UNAIDS data 2021 [Internet]. Geneva: Joint United Nations Programme on HIV/AIDS (UNAIDS). [erişim 13 Mart 2022]. https://www.unaids.org/en/resources/documents/2021/2021_unaids_data
- HIV data and statistics [Internet]. Geneva: World Health Organization (WHO). [erişim 13 Mart 2022]. https://www.who.int/teams/global-hiv-hepatitis-and-stis-programmes/hiv/strategic-information/hiv-data-and-statistics
- Dokuzoguz B, Korten V, Gökengin D, et al. Transmission route and reasons for HIV testing among recently diagnosed HIV patients in HIV‐TR cohort, 2011–2012. J Int AIDS Soc. 2014;17:19595. [CrossRef]
- Brown AE, Hayes R, Noori T, et al. HIV in Europe and Central Asia: progress in 2018 towards meeting the UNAIDS 90-90-90 targets. Euro Surveill. 2018;23(48):1800622. [CrossRef]
- Korten V, Gökengin D, Eren G, et al. Trends and factors associated with modification or discontinuation of the initial antiretroviral regimen during the first year of treatment in the Turkish HIV-TR Cohort, 2011–2017. AIDS Res Ther. 2021;18(1):4. [CrossRef]
- Bolukcu S, Mete B, Gunduz A, et al. Assessment of the 24th week success of anti-retroviral therapy in ACTHIV-IST database: Results from a region with increasing incidence. Jpn J Infect Dis. 2019;72(3):173-8. [CrossRef]
- Korten V, Gökengin D, Fincanci M, et al. Outcomes of initial antiretroviral treatment (ART) among recently diagnosed HIV patients in HIV‐TR cohort, 2011–2012. J Int AIDS Soc. 2014;17:19678. [CrossRef]
- Guidelines for the use of antiretroviral agents in HIV-1-infected adults and adolescents [Internet]. HHS Panel on Antiretroviral Guidelines for Adults and Adolescents – A Working Group of the Office of AIDS Research Advisory Council (OARAC). [erişim 13 Mart 2022]. https://clinicalinfo.hiv.gov/sites/default/files/guidelines/archive/AdultandAdolescentGL003093.pdf
- HIV/AIDS Tanı Tedavi Rehberi [Internet]. Ankara: TC Sağlık Bakanlığı Türkiye Halk Sağlığı Kurumu. [erişim 13 Mart 2022]. https://hsgm.saglik.gov.tr/depo/birimler/Bulasici-hastaliklar-db/hastaliklar/HIV-ADS/Tani-Tedavi_Rehberi/hiv_aids_tani_tedavi_rehberi_2013.pdf
- Kısa Ürün Bilgisi: ISENTRESS® 400 mg film kaplı tablet [Internet]. İstanbul: Merck Sharp Dohme İlaçları Ltd. Şti. [erişim 13 Mart 2022]. https://pdf.ilacprospektusu.com/3839-isentress-400-mg-film-kapli-tablet-kub.pdf
- Rockstroh JK, DeJesus E, Lennox JL, et al. Durable efficacy and safety of raltegravir versus efavirenz when combined with tenofovir/emtricitabine in treatment-naive HIV-1–infected patients: final 5-year results from STARTMRK. J Acquir Immune Defic Syndr. 2013;63(1):77-85. [CrossRef]
- Brooks KM, Sherman EM, Egelund EF, et al. Integrase inhibitors: after 10 years of experience, is the best yet to come? Pharmacotherapy. 2019;39(5):576-98. [CrossRef]
- Scarsi KK, Havens JP, Podany AT, Avedissian SN, Fletcher CV. HIV-1 integrase inhibitors: a comparative review of efficacy and safety. Drugs. 2020;80(16):1649-76. [CrossRef]
- Touloumi G, Pantazis N, Chaix ML, et al. Virologic and immunologic response to cART by HIV-1 subtype in the CASCADE collaboration. PloS ONE. 2013;8(7):e71174. [CrossRef]
- Lagi F, Kiros ST, Di Giambenedetto S, et al. Long-term maintenance of virologic suppression in native and migrant HIV-1 naïve patients: an Italian cohort study. AIDS Care. 2021;33(9):1159-66. [CrossRef]
- Young J, Weber R, Rickenbach M, et al. Lipid profiles for antiretroviral-naive patients starting PI-and NNRTI-based therapy in the Swiss HIV cohort study. Antiv Ther. 2005;10(5):585-91.
- Clotet B, Negredo E. HIV protease inhibitors and dyslipidemia. AIDS Rev. 2003;5(1):19-24.
- Lagathu C, Béréziat V, Gorwood J, et al. Metabolic complications affecting adipose tissue, lipid and glucose metabolism associated with HIV antiretroviral treatment. Expert Opin Drug Saf. 2019;18(9):829-40. [CrossRef]
- Babiker AG, Emery S, Fätkenheuer G. Considerations in the rationale, design and methods of the Strategic Timing of AntiRetroviral Treatment (START) study. Clin Trials. 2013;10(1 Suppl):S5-S36. [CrossRef]
- Guidelines Version 11.0 October 2021 [Internet]. Brussels: European AIDS Clinical Society (EACS). [erişim 13 Mart 2022]. https://www.eacsociety.org/media/final2021eacsguidelinesv11.0_oct2021.pdf
- Waters L, Ahmed N, Angus B, et al. BHIVA Guidelines for the treatment of HIV-1-positive adults with antiretroviral therapy 2015 (2016 interim update) [Internet]. Hertford: British HIV Association (BHIVA). [erişim 13 Mart 2022]. https://www.bhiva.org/file/RVYKzFwyxpgiI/treatment-guidelines-2016-interim-update.pdf