En Çok Okunanlar
Özet
Amaç: Keratoplasti öncesi korneada hasar kontrolünün yapılması, endotel hücre sayımı ile birlikte serolojik taramalarda insan sağlığı için oldukça önem arz etmektedir. Bu nedenle çalışmamızda; postmortem kornea donörlerinin, transplantasyon öncesi hepatit B virusu (HBV), hepatit C virusu (HCV), insan bağışıklık yetmezliği virusu (HIV) ve Treponema pallidum serolojik test sonuçlarını ortaya koymak ve özellikle düşük reaktif/pozitif test sonuçlarını desteklemek veya doğrulamak için serolojik ve moleküler testlerle korelasyonunun saptamak amaçlandı.
Yöntemler: Ocak 2015-Aralık 2020 tarihleri arasında göz bankasından gönderilen postmortem kornea donörlerinin serolojik test sonuçları retrospektif olarak incelendi. Donörlerin demografik ve serolojik test verilerine Cerrahpaşa Tıp Fakültesi Hastanesi’nin ISHOP sistemi Elisa Laboratuvarı verilerinden ulaşıldı.
Bulgular: Toplam 424 postmortem kornea donörünün 161 (%37.7)’i kadın, 263 (%62.03)’ü erkekti. Yapılan tarama sonucunda 424 donörün 13 (%3.06)’ünde HBsAg yüksek pozitiflik, 23 (%5.42)’ünde anti-HCV düşük reaktiflik, 19 (%4.48)’unda anti-HIV 1/2 düşük reaktiflik ve 2 (%0.47)’sinde Tp-Ab IgG yüksek reaktiflik saptandı. Düşük reaktivite saptanan donörlerde doğrulama amaçlı yapılan gerçek zamanlı polimeraz zincir reaksiyonu (RT-PCR) testi sonucunda HCV RNA’sı pozitif olan 30 yaşındaki bir kadın donörün, HBsAg yüksek titrede pozitiflik alan 13 donörün ve Tp-Ab IgG test sonucu yüksek reaktiflik saptanan 2 donörün korneaları göz bankası tarafından kullanılamamıştır.
Sonuç: Kornea transplantasyonu öncesi mikrobiyolojik bulaşmaları önlemek için yapılan serolojik testler ile postmortem koagulum hemolizi nedeniyle meydana gelebilen düşük pozitiflik/reaktiflik durumundan kaynaklı olarak yapılan doğrulama testlerinin ortak ve belirli bir algoritma çerçevesinde uygulanması oldukça önemlidir.
GİRİŞ
Keratoplasti olarak da adlandırılan kornea nakli ilk kez 1905 yılında Eduard Konrad Zirm tarafından yapılmış olup o zamandan bu yana en sık yapılan nakil türüdür (1). Korneanın tam kalınlıkta değiştirilmesini içeren bir prosedür olan penetran keratoplasti (PK), yarım yüzyıldan fazla bir süredir yaygın olarak uygulanmaktadır (2-4). Bununla birlikte bazı çalışmalar, PK’yı takiben uzun vadeli kornea greft sağ kalım oranlarının tatmin edici olmadığını göstermiştir; bu durum esas olarak endotelyal immünolojik allogreft reddine ve donör kornealarının endotel hücrelerinin sürekli kaybına bağlanmaktadır (2-4). Bu nedenle son yıllarda, ön lamellar keratoplastinin (ALK) yanı sıra özellikle derin ön lamellar keratoplastini (DALK) daha fazla öne çıkmaktadır (5). ALK, endotelin etkilenmediği keratopati vakalarında sağlıklı kornea endotelini koruyarak endotel reddi riskini ortadan kaldırabilmektedir (6).
Türkiye’de ilk olarak 1963 yılında Ankara Eğitim ve Araştırma Hastanesi’nin ardından 1993 yılında İstanbul Tıp Fakültesi’nde faaliyetlerine başlayan göz bankaları aracılığıyla yürütülen keratoplasti işlemlerinin sayısı eğitimler ve yazılı/görsel medya zeminli bilgilendirmelerin katkısıyla giderek artmaktadır (7). T.C. Sağlık Bakanlığı verilerine göre 2020 yılında 1734 keratoplasti yapılmıştır (8). Birçok organ nakli bekleyen kişide olduğu gibi keratoplastide de uygun donör bulmak oldukça zordur. Ayrıca, infeksiyonlar (viral infeksiyonlar ve septisemi), maligniteler, geçirilmiş göz içi cerrahi müdahaleler ve hastalıklar kornea naklinde kontrendike kabul edilmekte ve uygun olan dokunun imha edilmesine neden olmaktadır (9). Uluslararası Göz Bankaları Federasyonu (“International Federation of Eye Banks – IFEB”) ve Avrupa Göz Bankası Birliği (“European Eye Bank Association – EEBA”) tarafından kornea transplantasyonu öncesi immünolojik (serolojik) testler zorunlu tutulmuştur (10). Ülkemizde de keratoplasti öncesinde söz konusu taramalar, Organ ve Doku Alınması, Saklanması, Aşılanması ve Nakli Hakkında Kanun kapsamında zorunlu kılınmıştır (11, 12). Kornea transplantasyonu sonrası infeksiyon etkenlerinin bulaşı nadir olmakla birlikte infeksiyon etkenlerinin serolojik taramasının yapılması ile reaktiflik/pozitiflik saptanan postmortem kornea donörlerinin belirlenmesi post keratoplasti süreci için hem gelişebilecek infeksiyon hastalıkları hem de korneanın kullanımı yönünden çok önemlidir. Bu süreçte en sıkıntılı ve kafa karıştırıcı problem, postmortem kornea donörlerinde sıkça hemolize bağlı olarak gözlenen düşük reaktiviteli, özellikle antikor saptamaya yönelik serolojik test sonuçlarıdır. Postmortem kornea dönorlerindeki pre-op dönemde düşük reaktiviteli serolojik test sonuçları ve algoritmaları ile ilintili sorunlara dönük ulusal düzeyde yapılan çalışmaların sayısı az olup bu hususta farklı merkezlerce yeni çalışmaların yapılması önemlidir.
Retrospektif olarak gerçekleştirilen çalışmamızda; Cerrahpaşa Tıp Fakültesi Hastanesi Göz Bankası’na keratoplasti için başvuran olgular için, korneaları hazırlanan postmortem kornea donörlerinin transplantasyon öncesi hepatit B virusu (HBV), hepatit C virusu (HCV), insan bağışıklık yetmezliği virusu (HIV) ve Treponema pallidum serolojik test sonuçlarının ortaya konması ve özellikle düşük reaktif/pozitif test sonuçlarını desteklemek veya doğrulamak için serolojik ve moleküler testlerle korelasyonunun saptanması amaçlandı. Aynı zamanda, bu verilerle birlikte kornea hastalıklarında önemli bir çözüm yolu olan keratoplasti işleminde, serolojik test sonucu karmaşasından dolayı gelişebilecek kornea donör kaybı sorununa dönük oluşturulacak tanısal algoritmalara bir katkı sunmayı hedefledik.
YÖNTEMLER
Çalışmamız, Ocak 2015-Aralık 2020 tarihleri arasında Cerrahpaşa Tıp Fakültesi Göz Hastalıkları Anabilim Dalı, Kornea Polikliniği’ne başvurmuş ve keratoplasti endikasyonu alan hastalar için hastanemizin göz bankası tarafından temin edilen kornea donörlerinde transplantasyon öncesi yapılan serolojik testlerin retrospektif olarak taranmasını kapsamaktadır. Kornea dokularının temininde IFEB ve EEBA tarafından belirlenen koşullar göz önünde tutuldu (10). Bu doğrultuda öncelikle; nedeni bilinmeyen ölüm, tanısı konulmamış nörolojik hastalıklardan ölüm, Creuzfeldt-Jacob hastalığı, subakut sklerozan panensefalit, progresif multifokal lökoensefalit, konjenital rubella, Reyes sendromu, intrinsik göz hastalıkları gibi sistemik durumlardan herhangi birini içeren donörlerden korneaları alınmadı. Çalışmamızda değerlendirilen 424 postmortem kornea donörünün demografik ve serolojik test bilgilerine, Cerrahpaşa Tıp Fakültesi Hastanesi’nin ISHOP sistemi Elisa Laboratuvarı verilerinden ulaşıldı. Seroloji ünitesine gönderilen 424 postmortem kornea donör serumunda; HBV, HCV, HIV ve T. pallidum için pre-op tarama testleri olarak HBsAg, Anti-HCV, HIV Ag/Ab, RPR ile TP-Ab IgG testleri gerçekleştirildi ve düşük reaktiflik saptanan donörlerde doğrulama testi olarak RT-PCR kiti (İontek, İstanbul Türkiye) kullanıldı. İlintili yöntemlerin değerlendirilmeleri tarafımızca belirlenmiş olup düşük (1-9.99), orta (10.00-19.99) ve yüksek (>20.00) düzey [S/CO (“signal/cut-off”)] aralıkları Tablo 1’de verilmiştir.
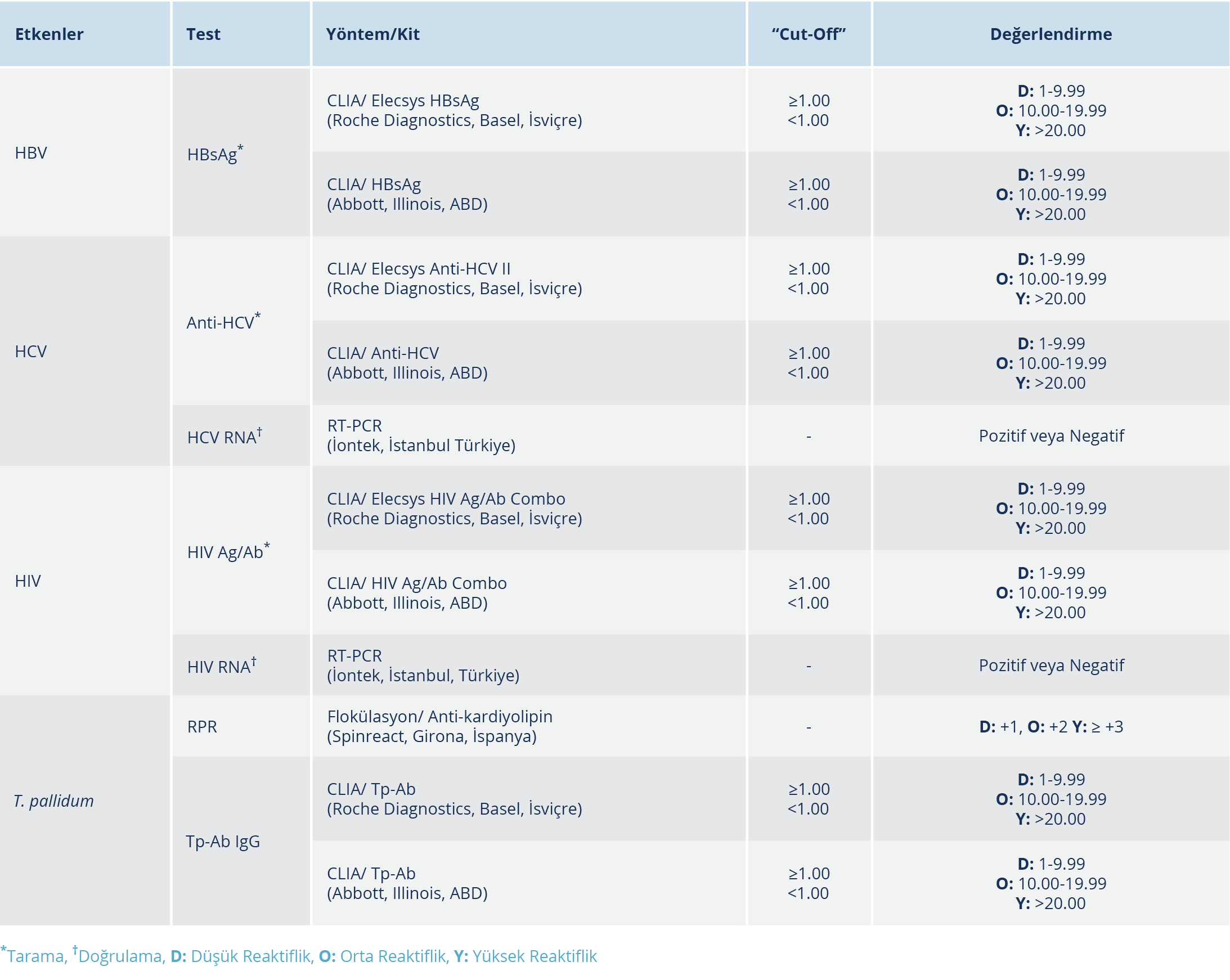
Tablo 1. Mikrobiyolojik Olarak İncelenen Etkenlere Yönelik Tarama, Doğrulama Testlerinde “Cut-Off” ve Değerlendirme Aralık Düzeyleri
Merkezimizde, Ocak 2014-Haziran 2016 tarihleri arasında serolojik sifilis tanısı için konvansiyonel algoritma izlenmiş olup tüm serum örneklerine non-treponemal tarama testi olarak RPR (“rapid plasma reagin”) (Spinreact, Girona, İspanya) uygulanmıştır (13). Temmuz 2016’dan itibaren ise konvansiyonel algoritma değiştirilmiş olup ABD Hastalık Kontrol ve Korunma Merkezleri (“Centers for Disease Control and Prevention – CDC”) (14) ve Avrupa Hastalık Önleme Kontrol Merkezi (“European Centre for Disease Prevention and Control – ECDC”) (15) önerileri doğrultusunda ters algoritma uygulanmaya başlamıştır. 2016-2018 yılları arasında Tp-Ab IgG (Abbott, Illinois, ABD), 2019’da Elecsys® Syphilis (Roche Diagnostics, Basel, İsviçre), 2020 itibariyle ise tekrar Tp-Ab IgG Abbott (Abbott, Illinois, ABD) kullanılarak kemilüminesans immünoessey (CIA) yöntemi uygulanmıştır (13) (Tablo 1).
Çalışma için, İstanbul Üniversitesi Cerrahpaşa Tıp Fakültesi Klinik Araştırmalar Etik Kurulu’dan 06 Temmuz 2021 tarih ve A-66 karar numarası ile onay alınmıştır.
BULGULAR
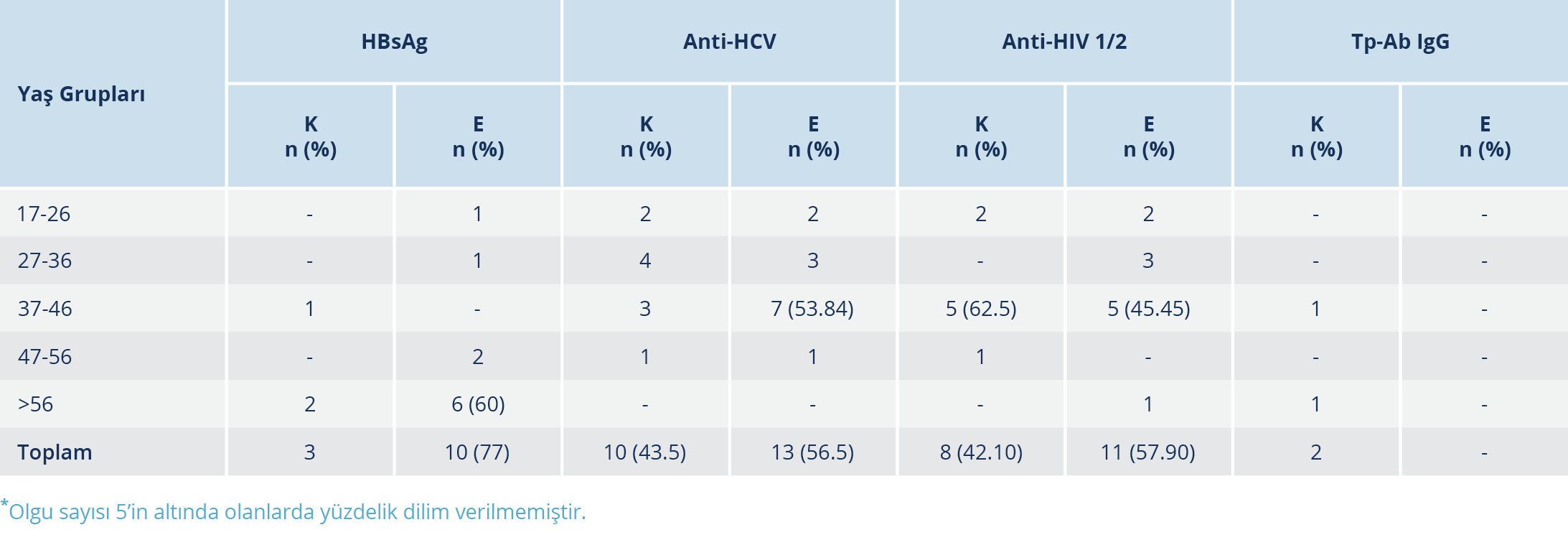
Tablo 3. Serolojik Olarak Pozitiflik/Reaktiflik Saptanan Kornea Donörlerinin Yaş ve Cinsiyete Göre Dağılımı
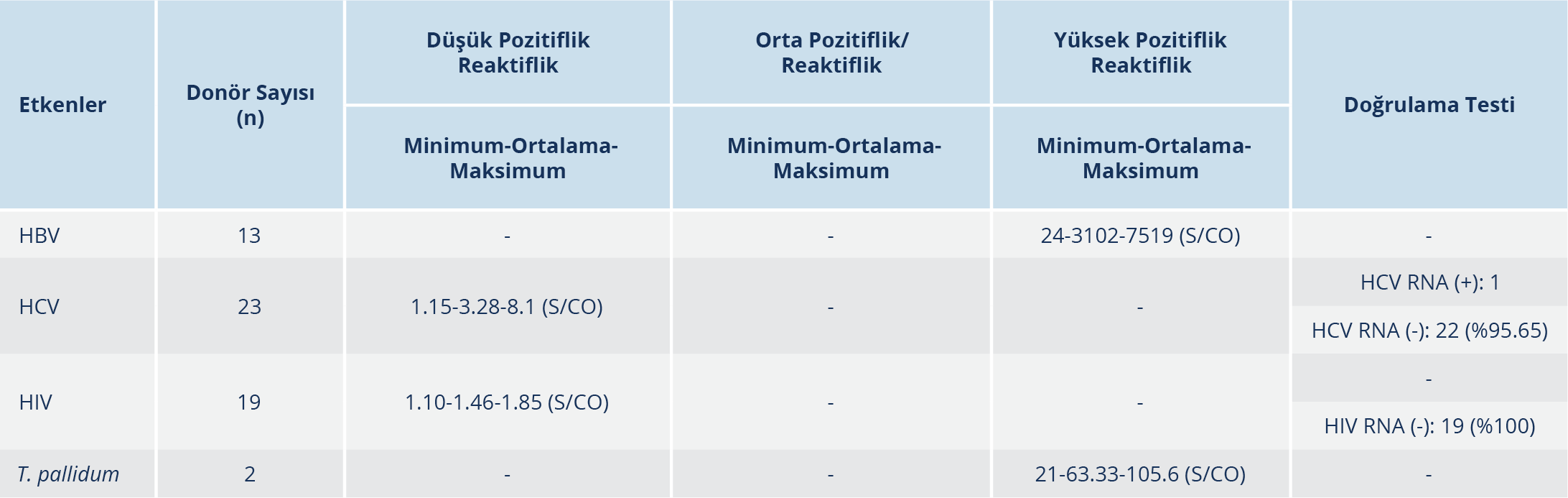
Tablo 5. Serolojik Olarak Pozitiflik/Reaktiflik Saptanan Kornea Donörleri ve Doğrulama Test Sonuçları
424 donöre ait demografik veriler Tablo 2’de yer almaktadır. Postmortem kornea donörlerinin 161 (%37.7)’i kadın iken 263 (%62.03)’ü erkektir. En az postmortem kadın donör sayısı 10 (%6.21) olup 17-26 yaş aralığındadır; çoğunlukta olan 71 (%44.1) kadın donörse 56 yaş ve üzerindedir. En az postmortem erkek donör sayısı ise 22 (%8.36) olup 17-26 yaş aralığındadır; çoğunlukta olan 111 (%42.21) erkek donörse 56 yaş ve üzerindedir. Erkek ve kadın donör sayılarının kıyaslamasına yüzdelik olarak bakıldığında en fazla donörün 56 yaş ve üzerindeki kadınlar [71 (%44.1)] olduğu görülmektedir.
Pozitiflik/reaktiflik saptanan donörlerin yaş ve cinsiyete göre dağılımı Tablo 3’te verilmiştir. HBsAg pozitifliği saptanan 13 donörün 10 (%76.92)’u erkek ve 3 (%23.07)’ü kadın olup yaş ortalaması 55.23’tür. Anti-HCV reaktifliği olan 23 donörün 10 (%43.47)’u erkek ve 13 (%56.52)’ü kadın olup yaş ortalaması 35.69’dur. Anti-HIV 1/2 reaktifliği olan 19 donörün 11 (%57.89)’i erkek ve 8 (%42.10)’i kadın olup yaş ortalaması 35.63’tür. Tp-Ab IgG reaktifliği olan 2 donörün ise tamamı (%100) kadın olup yaş ortalaması 64.5’tir.
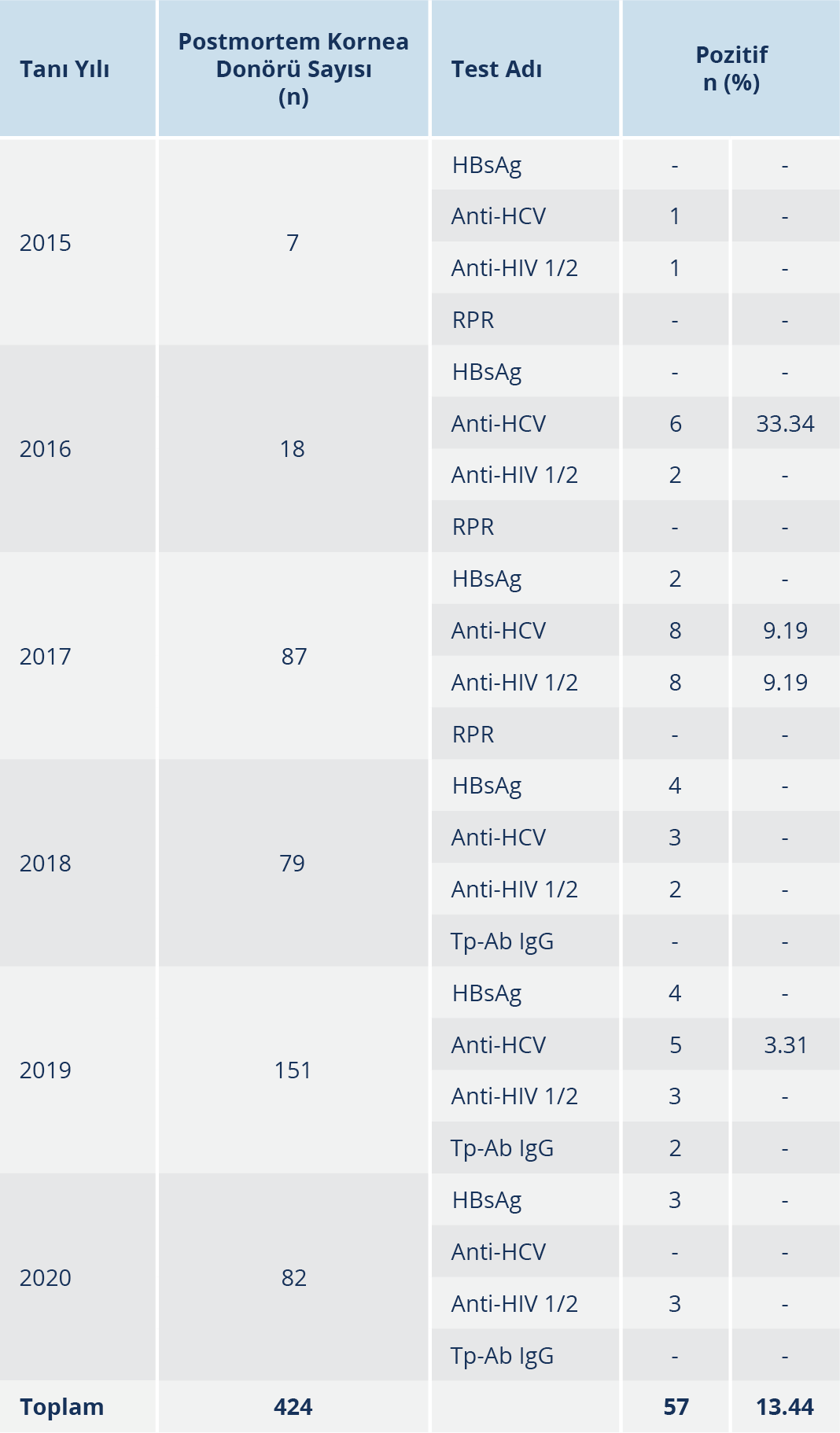
Postmortem kornea donörlerinin; HBV, HCV, HIV ve T. pallidum reaktiflik/pozitiflik sıklığının yıllara göre dağılımı ise Tablo 4’te verilmiştir. Beş yıllık dönemde incelenen 424 donörün; 13 (%3.06)’ünde HBsAg pozitifliği, 23 (%5.42)’ünde Anti-HCV reaktivitesi, 19 (%4.48)’unda anti-HIV 1/2 reaktivitesi ve 2 (%0.47)’sinde ise Tp-Ab IgG reaktivitesi saptanmıştır. HBsAg pozitifliğine 2015- 2016 yılları arasında rastlanmazken en fazla pozitiflik 4 donörle 2018-2019 yıllarında tespit edilmiştir. Anti-HCV reaktifliği 2020 yılında görülmemiş; en fazla reaktiflik 8 donörle 2017 yılında bildirilmiştir. Anti-HIV 1/2 reaktifliği bir donörle en az olarak 2015 yılında bildirilirken 8 donörle en fazla reaktiflik 2017 yılındadır. Tp-Ab IgG reaktifliği 2 donörle sadece 2020 yılında bildirilmiştir. Toplamda, Ocak 2015-Aralık 2020 yılları arasında etkenlerin varlığı yönünden 57 reaktiflik/pozitiflik saptanmıştır.
HBsAg yüksek pozitifliği saptanan 13 donörün, Tp-Ab IgG yüksek reaktifliği olan iki donörün ve anti-HCV, anti-HIV 1/2 test sonucunda düşük reaktivite saptanan toplam 42 donörün reaktifliklerinin minimum, ortalama ve maksimum değerleri Tablo 5’te ayrıntılı olarak gösterilmiştir. HBsAg yüksek pozitiflikte minimum değer 24 S/CO iken maksimum değer 7519 S/Co olarak saptanmıştır. Tp-Ab IgG’de ise yüksek reaktiflikte minimum değer 21 S/CO iken maksimum değer 105.6 S/CO olarak saptanmıştır. Bununla birlikte, yapılmış olan doğrulama testi sonucu anti-HCV düşük reaktifliği bulunan 23 donörün 22 (%95.65)’sinde anti-HIV 1/2 düşük reaktifliği saptanan 19 donörün ise tamamında (%100) RT-PCR sonucu negatif saptanmıştır. 2018-2020 yılları arasında HBsAg pozitifliği saptanan 13 donörün, 2015 yılında düşük reaktivite tespit edilen fakat HCV RT-PCR sonucu pozitif olan 30 yaşındaki bir kadının ve 2019 yılında Tp-Ab IgG test sonucu pozitif saptanan iki donörün korneaları infeksiyon varlığı nedeniyle göz bankası tarafından kullanılmamıştır.
İRDELEME
İnsan hayatını doğrudan etkileyebilecek keratoplasti öncesi yapılan donör seçiminde korneada hasar olup olmadığının tespiti için endotel hücre sayımının yanı sıra infeksiyon etkenlerinin varlığına dönük olarak yapılan taramalar da son derece önemlidir. Ocak 2015-Aralık 2020 tarihleri arasında yaptığımız tarama sonucunda 424 donörün 13 (%3.06)’ünde HBsAg yüksek pozitiflik, 23 (%5.42)’ünde anti-HCV düşük reaktiflik, 19 (%4.48)’unda anti-HIV 1/2 düşük reaktiflik ve 2 (%0.47)’sinde Tp-Ab IgG yüksek reaktiflik saptanmıştır. Hindistan’dan bildirilen bir araştırmada Aralık 2012 – Haziran 2017 yılları arasında 509 kornea donöründe yapılan serolojik testler sonucu 12 HBsAg pozitif, bir anti-HCV reaktif donör saptanırken anti-HIV 1/2 ve sifilis IgG reaktifliğine rastlanmamıştır (16). Söz konusu çalışmanın sonuçlarının karşılaştırılması yapıldığı zaman HBsAg verileri yönünden bizim çalışmamızla benzer olduğu görülmektedir. Güney Brezilya’da 2019 yılında yapılan bir çalışmada ise 4 yıllık bir retrospektif tarama sonucunda 4645 donörden 9290 kornea alındığı fakat 2097 (%49.6) korneanın seropozitiflikten ötürü kullanılamadığı tespit edilmiştir (17). Altınkurt ve arkadaşları (18) tarafından 2020 yılında 23 yıllık donör verilerinin analizinin yapıldığı bir çalışmada, 2018 donörden alınan toplam 3048 kornea dokusunun 206 (%5.35)’sının serolojik testlerin pozitifliği nedeniyle kullanılamadığı bildirilmiştir. Kocazeybek ve arkadaşları (19) tarafından 229 kornea donöründe yapılan çalışmada, 15 (%6.6.) donörde HbsAg pozitifliği, 2 (%0.9) donörde anti-HCV reaktifliği ve bir donörde ise her iki etken için yapılan testler pozitif olarak saptanmıştır (19). Söz konusu çalışmanın sonuçları HBsAg pozitifliği açısından bizim bulgularımızla uyumlu olmakla birlikte zaman içerisinde anti-HCV reaktifliğinde artış olduğu ve bu artışın yapılan moleküler doğrulama sonucunda yanlış pozitiflikten kaynaklandığı gösterilmiştir.
Kan, Doku ve Organların Güvenliği Danışma Kurulu (“Advisory Committee on the Safety of Blood, Tissues and Organs – SaBTO”), kornea donörlerinde HCV taraması açısından anti-HCV testinin tek başına yeterli olmadığını; HIV antikor taramasının ise tek başına düşük duyarlılığa sahip olduğunu ve bu etkenlerin bir nükleik asit amplifikasyon testiyle (NAAT) RNA varlığı açısından taranarak doğrulanması gerektiğini belirtmektedir (20). Bu doğrultuda, çalışmamızda gerçekleştirilen tarama testlerinde anti-HCV düşük reaktivite saptanan 23 donör ve anti-HIV 1/2 düşük reaktivite saptanan 19 donör dış merkezde doğrulama testine tabi tutulmuş olup doğrulama testi sonucunda HCV ve HIV RNA saptanmayan 41 donörün korneaları göz bankası tarafından kullanılmıştır. Gerçekleştirilen tüm serolojik ve moleküler testlerin sonucunda; toplamı 16 olmak üzere, HBV varlığı saptanan 13, HCV varlığı saptanan bir ve T. pallidum varlığı saptanan iki donörün korneaları halk sağlığı nedeniyle kullanılmamıştır. Çalışmamızdaki bazı donör serumlarında düşük reaktiviteli HCV ve HIV saptanmasının nedeni; ölüm sonrası geçen süre (düşük HCV ve HIV reaktivitesi gösteren postmortem serumlar transplantasyondan önce laboratuvarımıza mikrobiyolojik çalışmalar için minimum 12 saat, maksimum 36 saat ortalama 24 saat içerisinde iletilmiştir), çevre şartları ve antijen-antikor reaksiyonlarına bağlı olarak postmortem vücut sıvılarındaki biyokimyasal ve mikrobiyolojik inceleme sonuçlarının değişmesi olabilir. Klinik ölümün gerçekleşmesi ile tüm organizmada hücre düzeyinde oksijen yetmezliği, karbondioksit birikimi, pH değişiklikleri, toksik ürünlerin birikimi meydana gelmektedir (21-23). Ölüm sonrası kanda ve diğer vücut sıvılarında meydana gelen değişiklikler nedeniyle biyokimyasal ve mikrobiyolojik incelemeler hızla değerini yitirmektedir (21-23). Postmortem koagulum genellikle ölümden 3-4 saat sonra hemolize olmaya başlar ve bu olay 24 saatte tamamlanır (21-23). İsrail’de yapılan bir çalışmada, postmortem kornea donörlerinde HCV antikor test sonuçlarını etkileyebilecek en önemli parametrenin ölüm saati olduğu; korneanın tedariki ile ölüm saati arasındaki zaman aralığının anti-HCV reaktifliği için oldukça önemli bir risk faktörü olduğu bildirilmiştir. Söz konusu çalışmada, 10 saatten az zaman aralığı olan donörlerde pozitif test sonuçlarının oranı sadece %2.9 iken, 10 saatten uzun olanlarda %10 olduğu tespit edilmiştir (24). Bu durum yanlış pozitifliklerin verilmesine ve sonucunda korneanın bu hatadan ötürü kullanılamamasına neden olabilmektedir. Bununla birlikte, postmortem kanlarında bakılan HBV, HCV, HIV ve T. pallidum etkenlerinin immünolojik (serolojik) test sonuçlarında, antijen-antikor arası bağların non-spesifik olarak bağlanması ve hidrojen bağları gibi van Der walls kuvvetlerinin zayıf oluşumu sonucu düşük reaktivite ya da yanlış pozitiflik meydana gelebilir (21-23). Lee ve arkadaşları (25) tarafından yapılan çalışmada, bir yıl boyunca Kanada Göz Bankası’na gelen 1619 potansiyel postmortem kornea donörü ilk olarak serolojik olarak taranmış ve bunların 15’inde anti-HCV reaktifliğinin saptandığı belirtilmiştir. Aynı çalışmada yapılan moleküler temelli doğrulama testi ile kornea donörlerinin 7’sinde HCV RNA tespit edildiği belirtilmiştir. Bu sebeple, postmortem kornea donörlerinde yapılan serolojik pre-op tarama testlerinin, doğrulama testleriyle desteklenmesi halk sağlığı açısından son derece önemlidir.
Sonuç olarak, yapılan bu retrospektif tarama; kornea transplantasyonu öncesinde, seropozitif vericilerdeki HBV, HCV, HIV ve T. pallidum’un alıcı sağlığı açısından oldukça önemli bir risk olduğunu, transplantasyon öncesi bu taramaların ve doğrulamaların titizlikle yapılmasının gerekliliğini bir kez daha göstermiştir. Ayrıca, kornea transplantasyonu öncesi mikrobiyolojik bulaşmaları önlemek için mikrobiyoloji laboratuvarlarında kullanılan test ve kitlerin optimize, duyarlığı ve özgüllüğü yüksek olması oldukça önemlidir. Postmortem kornea donörlerinin kısıtlı bağışlardan dolayı yeterince bulunamaması göz önüne alınarak donörlerde saptanabilecek düşük pozitif/reaktif sonuçların korneaların kullanılamamasına neden olmaması için her laboratuvarın belirli bir algoritmasının olması gerekmektedir. Böylelikle dünyada sık nakledilen bir doku olmasına rağmen Türkiye’de halen istenilen düzeyde olmayan kornea transplantasyonunun serolojik taramalar sonucu yanlış pozitifliğe/reaktifliğe bağlı kullanılamamasının önüne geçilebileceğini düşünüyoruz. Ayrıca, ulusal düzeyde bu tür taramaların ve çalışmaların artırılmasının yanı sıra ortak ve özellikle düşük reaktiviteli sonuçlara yönelik bir pre-op tarama ve tanı algoritmasının tekrar gözden geçirilmesi gerektiği kanaatindeyiz. Elde ettiğimiz veriler neticesinde kornea transplantasyonu öncesinde postmortem donörlerde HCV, HIV ve HBV için doğrulama testi olarak RT-PCR’ın, T. pallidum içinse RPR testlerinin uygulanmasının etkin olduğunu tespit ettik.
Etik Kurul Kararı
Çalışma için İstanbul Üniversitesi-Cerrahpaşa Cerrahpaşa Tıp Fakültesi Klinik Araştırmalar Etik Kurulu’ndan 06 Temmuz 2021 tarih ve A-66-06.07.2021 karar numarasıyla onay alınmıştır.
Danışman Değerlendirmesi
Bağımsız dış danışman.
Yazar Katkıları
Fikir/Kavram – B.S.K., O.Ş.A., H.B.T., A.S.S., M.D., R.A.; Tasarım –C.D., R.A., S.S., H.Ö.D., D.Ö.; Denetleme – B.S.K., O.Ş.A., H.B.T., A.S.S., M.D.; Kaynak ve Fon Sağlama – R.A., B.S.K., H.Ö.D.; Veri Toplama ve/veya İşleme – R.A., D.Ö., S.S., C.D., M.D., H.Ö.D.; Analiz ve/veya Yorum – R.A., D.Ö., H.Ö.D.; Literatür Taraması – R.A., S.S., C.D.; Makale Yazımı – R.A., D.Ö., H.Ö.D., S.S.; Eleştirel İnceleme – B.S.K., O.Ş.A., H.B.T., A.S.S., R.A.
Çıkar Çatışması
Yazarlar herhangi bir çıkar çatışması bildirmemiştir.
Finansal Destek
Yazarlar finansal destek beyan etmemiştir.
Referanslar
- Zirm EK. Eine erfolgreiche totale keratoplastik. Graefes Arch Clin Exp Ophthalmol. 1906;64:580-93.
- Nishimura JK, Hodge DO, Bourne WM. Initial endothelial cell density and chronic endothelial cell loss rate in corneal transplants with late endothelial failure. Ophthalmology. 1999;106(10):1962-5. [CrossRef]
- Thompson RW Jr, Price MO, Bowers PJ, Price FW Jr. Long-term graft survival after penetrating keratoplasty. Ophthalmology. 2003;110(7):1396-402. [CrossRef]
- Tan DTH, Dart JKG, Holland EJ, Kinoshita S. Corneal transplantation. Lancet. 2012;379(9827):1749-61. [CrossRef]
- Wylegała E, Tarnawska D, Dobrowolski D. Deep lamellar keratoplasty for various corneal lesions. Eur J Ophthalmol. 2004;14(6):467-72. [CrossRef]
- Reinhart WJ, Musch DC, Jacobs DS, Lee WB, Kaufman SC, Shtein RM. Deep anterior lamellar keratoplasty as an alternative to penetrating keratoplasty: A report by the American Academy of Ophthalmology. Ophthalmology. 2011;118(1):209-18. [CrossRef]
- Alparslan N. Kornea nakli. Klinik Gelişim Dergisi. 2012;25:35-9.
- Sağlık İstatistikleri Yıllığı [İnternet]. Ankara: T.C. Sağlık Bakanlığı Sağlık Bilgi Sistemleri Genel Müdürlüğü. [erişim 13 Haziran 2021]. https://dosyasb.saglik.gov.tr/Eklenti/43399,siy2020-tur-26052022pdf.pdf?0
- Vajpayee, RB. Corneal Transplantation. 1st ed. New Delhi: Jaypee Brothers Medical Publishers Ltd, 2002.
- Minimum Medical Standards [İnternet]. The European Eye Bank Association. [erişim 13 Haziran 2021]. https://www.eeba.eu/files/pdf/EEBA%20Minimum%20Medical%20Standards%20Revision%205%20Final.pdf
- Organ ve Doku Alınması, Saklanması, Aşılanması ve Nakli Hakkında Kanun [İnternet]. Ankara: Resmi Gazete. [3 Haziran 1979; erişim 13 Mayıs 2021]. https://www.mevzuat.gov.tr/MevzuatMetin/1.5.2238.pdf
- Göz Bankası ve Kornea Nakli Merkezleri Yönergesi [İnternet]. T.C. Sağlık Bakanlığı, Kan, Doku ve Organ Nakli Sistemleri Birimi. [erişim 13 Mayıs 2021]. https://webcache.googleusercontent.com/search?q=cache:h00rm56akpYJ:https://shgm.saglik.gov.tr/TR-865
- Dinç HÖ, Alkan S, Özbey D, et al. [Evaluation of syphilis coinfection in HIV-infected individuals]. Klimik Derg. 2020;33(3):292-6. Turkish. [CrossRef]
- Workowski KA, Bolan GA; Centers for Disease Control and Prevention. Sexually transmitted diseases treatment guidelines, 2015. MMWR Recomm Rep. 2015;64(RR-03):1-137. Erratum in: MMWR Recomm Rep. 2015;64(33):924.
- French P, Gomberg M, Janier M, et al. IUSTI: 2008 European guidelines on the management of syphilis. Int J STD AIDS. 2009;20(5):300-9. [CrossRef]
- Raj A, Mittal G, Bahadur H. Factors affecting the serological testing of cadaveric donor cornea. Indian J Ophthalmol. 2018;66(1):61-5. [CrossRef]
- Almeida de Freitas R, DellʼAgnolo CM, Augusto de Melo W, et al. Do donated corneas become transplanted corneas? The causes of discard in Southern Brazil. Cornea. 2019;38(4):419-25. [CrossRef]
- Altınkurt E, Avcı Ö, Cebeci Z, Alparslan N. Göz bankasının 23 yıllık donör verilerinin analizi [Özet]. In: TOD 17. Mart Sempozyumu (8 Kasım 2020, Antalya) Kitabı. İstanbul: Türk Oftalmoloji Derneği, 2020.
- Kocazeybek B, Çakan H, Sansoy N, Küçükateş E, Özdemir F. [Donor serotyping in cornea transplantation]. Klimik Derg. 2000;13(3):101-3. Turkish.
- Guidance on the Microbiological Safety of Human Organs, Tissues and Cells Used in Transplantation: Code of Practice. London: Advisory Committee on the Safety of Blood, Tissue and Organs (SaBTO). (güncelleme Mart 2020; erişim 13 Mayıs 2021). https://assets.publishing.service.gov.uk/government/uploads/system/uploads/attachment_data/file/518341/SaBTO_Code_of_Practice_Jan16.pdf
- Guyton AC. Textbook of Medical Physiology, 7th ed. Philadelphia: W.B. Saunders Co. 1986: 2-30.
- Arslan MN, Koç S. [Postmortem changes]. Turkiye Klinikleri J Foren Med-Special Topics. 2016;2(1):12-9. Turkish.
- Schmack I, Ballikaya S, Erber B, et al. Validation of spiked postmortem blood samples from cornea donors on the Abbott ARCHITECT and m2000 systems for viral infections. Transfus Med Hemother. 2020;47(3);236-43. [CrossRef]
- Cahane M, Barak A, Goller O, Avni I. The incidence of hepatitis C virus positive serological test results among cornea donors. Cell Tissue Bank. 2000;1(1);81-5. [CrossRef]
- Lee HM, Naor J, Alhindi R, et al. Detection of hepatitis C virus in the corneas of seropositive donors. Cornea. 2001;20(1);37-40. [CrossRef]