En Çok Okunanlar
Özet
Amaç: Obstrüktif olmayan koroner arterlere sahip miyokart infarktüsü (MINOCA) tanısı alan hastalarda hastane içi infeksiyon gelişim sıklığını ve buna katkıda bulunabilecek klinik ile laboratuvar faktörlerini değerlendirmek ve bulguları obstrüktif koroner arter hastalığına bağlı miyokart infarktüsü (MI-CAD) hastalarıyla karşılaştırmak amaçlandı.
Yöntemler: Prospektif ve tek merkezli bu çalışmada, Ekim 2019–Ekim 2020 döneminde akut miyokart infarktüsü ön tanısıyla başvuran 1120 hasta değerlendirildi; koroner arter hastalığı öyküsü olanlar dışlandı. MINOCA tanı kriterlerini karşılayan 104 hasta ile MI-CAD tanısı alan 601 hasta analiz edildi. Başvuru anındaki C-reaktif protein (CRP) düzeyleri, laboratuvar bulguları ve hastane içi komplikasyonlar kaydedildi. İnfeksiyonla ilişkili faktörleri belirlemek için çok değişkenli lojistik regresyon analizi uygulandı.
Bulgular: MINOCA grubunda CRP düzeyleri MI-CAD grubuna göre anlamlı olarak daha yüksekti [3.0 (1.0–9.0) mg/lt vs. 0.7 (0.3–2.3) mg/lt; p<0.001]. İnfeksiyon oranı MINOCA hastalarında %21.2, MI-CAD hastalarında %11.3 bulundu (p=0.010). Çok değişkenli analizlerde CRP ve diğer karıştırıcı değişkenler modele eklenmesine rağmen MINOCA grubu infeksiyon için bağımsız bir risk faktörü olarak kaldı (Model 3 OR 4.206; %95 GA: 2.040–8.670; p=0.001). Hastanede kalış süresi, diabetes mellitus ve kalp yetersizliği infeksiyon riskini artırırken hiperlipidemi koruyucu etki gösterdi.
Sonuç: MINOCA hastalarında infeksiyon gelişme oranlarının yüksek olması, bu grupta farklı bir inflamatuar ve immün yanıt profili olabileceğini düşündürmektedir. Bulgular, MINOCA hastalarının klinik yönetiminde infeksiyon riskinin dikkate alınması ve kapsamlı, multidisipliner bir yaklaşım benimsenmesi gerektiğini göstermektedir.
GİRİŞ
Miyokart infarktüsü (Mİ), anjiyografik olarak anlamlı obstrüktif koroner arter hastalığı (KAH) bulunmaksızın hastaların yaklaşık %1–14’ünde ortaya çıkabilmektedir (1). Elektrokardiyografide iskemik semptomların veya ST segment elevasyonunun görülmesine rağmen epikardiyal arterlerde <%50 darlık saptanması, aterotrombotik bir mekanizmanın dışlandığı anlamına gelmez (2). Avrupa Kardiyoloji Derneği (European Society of Cardiology, ESC) tarafından bu klinik tablo “Obstrüktif Olmayan Koroner Arterlere Sahip Miyokart İnfarktüsü” (Myocardial Infarction with Non-Obstructive Coronary Arteries, MINOCA)” olarak tanımlanmıştır (3).
MINOCA, altta yatan nedenlerin ayrıntılı olarak araştırılmasını gerektiren geçici bir tanıdır. Plak rüptürü veya erozyonunun trombotik oklüzyona yol açtığı tip 1 Mİ’ye benzer şekilde MINOCA da koroner vazospazm, spontan koroner arter diseksiyonu (Spontaneous Coronary Artery Dissection, SCAD), koroner embolizm veya mikrovasküler disfonksiyon gibi tip 2 Mİ mekanizmaları sonucu gelişebilir (4-7). Avrupa Kardiyoloji Derneği’nin 2017 kılavuzunda, MINOCA terminolojisinin standartlaştırılması, sistematik etiyolojik değerlendirme yapılması ve oksijen arz-talep dengesizliğinin tip 2 Mİ’deki rolü vurgulanmıştır (1,8).
Epidemiyolojik olarak MINOCA, tüm Mİ olgularının %5–10’unu oluşturmaktadır; genç yaş gruplarında ve kadınlarda daha sık görülmektedir. Bununla birlikte, prognozu obstrüktif Mİ’ye benzer olabilir (9). MINOCA’nın patofizyolojisi heterojendir; plak bozulması, mikrovasküler disfonksiyon, vazospazm, SCAD, miyokardit ve Takotsubo sendromu gibi çeşitli durumları içerebilir (10-12).
Güncel veriler, MINOCA hastalarında proinflamatuar bir fenotipin olabileceğine işaret etmektedir. İnflamasyonun hassas bir biyobelirteci olan C-reaktif protein (CRP), akut koroner sendromlarda olumsuz sonuçlarla ilişkilendirilmiştir (13). Öte yandan CRP düzeylerinin MINOCA’da mortalite ve majör kardiyovasküler olaylarla (Major Adverse Cardiovascular Events, MACE) bağımsız ilişkili olduğu gösterilmiş olup bu prognostik değer, obstrüktif koroner arter hastalığına bağlı miyokart infarktüsü ile karşılaştırıldığında anlamlı bir fark göstermemektedir (14). Eggers ve arkadaşları (15), İsveç kohortunda hastane başvurusu sırasında ölçülen CRP düzeylerinin tüm nedenlere bağlı mortalite [“hazard ratio” (HR)=1.22; %95 güven aralığı (GA): 1.17–1.26)] ve MACE (HR=1.08; %95 GA: 1.04–1.12) için öngördürücü olduğunu bildirmiştir (15).
Son yıllarda yapılan gözlemler, MINOCA hastalarında inflamasyonun yalnızca kardiyak doku hasarına değil, sistemik immün yanıtın düzenlenmesine de yol açabileceğini düşündürmektedir (16). Bu hastalarda saptanan yüksek CRP düzeyleri, artmış inflamatuar aktivitenin bir yansıması olup infeksiyonlara yatkınlık açısından da klinik olarak önem taşıyabilir. Özellikle diabetes mellitus, kalp yetersizliği ve uzamış hastane yatışı gibi durumlar, MINOCA hastalarında infeksiyon gelişme riskini artıran faktörlerdir. Bu nedenle, MINOCA’nın değerlendirilmesinde yalnızca kardiyovasküler prognoz değil, hastane içi infeksiyonların sıklığı ve bu infeksiyonlarla ilişkili belirleyicilerin de araştırılması önem kazanmıştır (17). Literatürde bu konuyu prospektif olarak değerlendiren veri oldukça sınırlıdır; bu çalışma bu açıdan mevcut bilgi birikimine katkı sunmayı amaçlamaktadır.
YÖNTEMLER
Çalışma Popülasyonu ve Veri Toplama
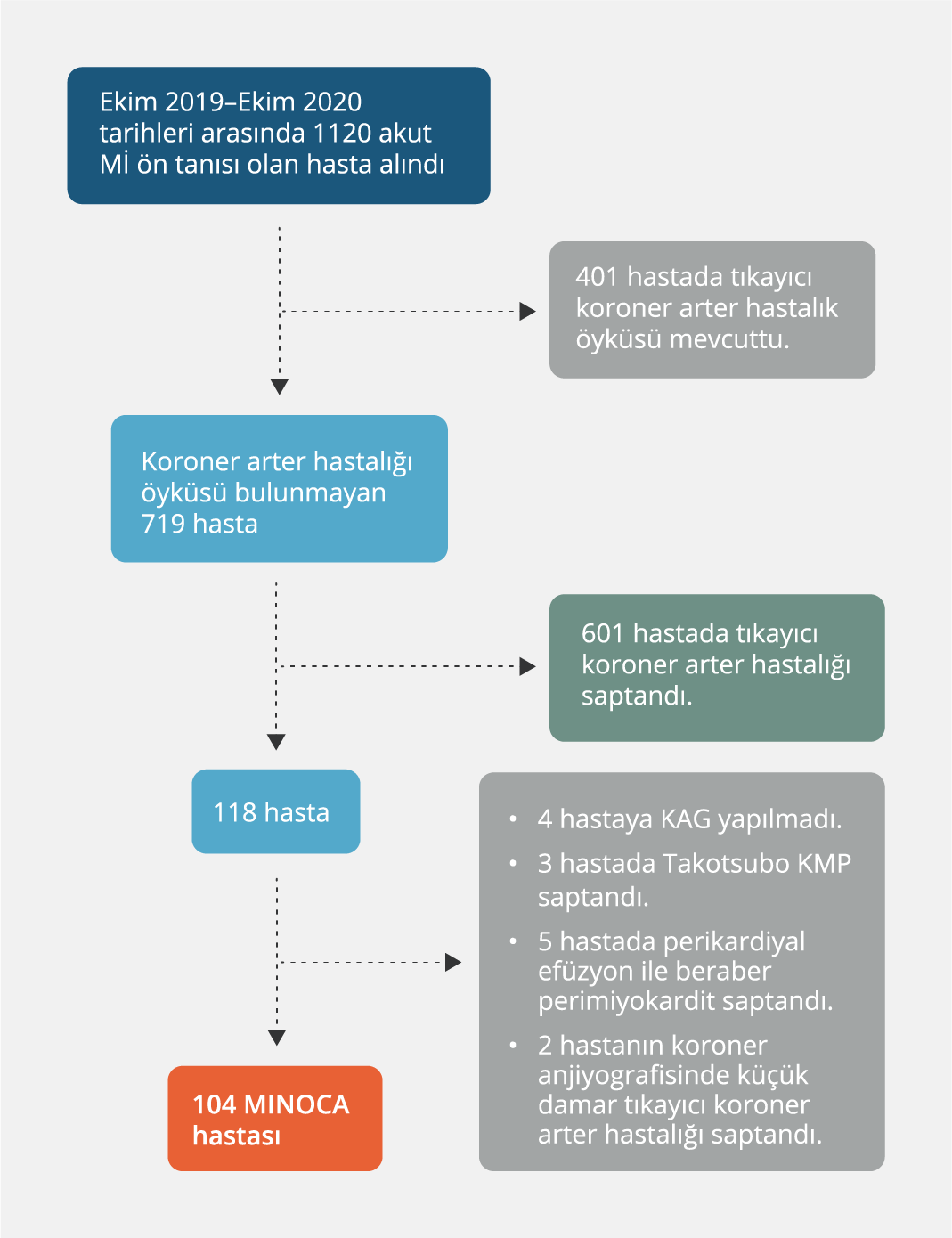
Prospektif olarak yürütülen bu çalışmada, 1 Ekim 2019 ile 1 Ekim 2020 tarihleri arasında hastanemizin acil servisine akut koroner sendrom (Acute Coronary Syndrome, AKS) ön tanısı ve kardiyak biyobelirteç yüksekliği ile başvuran 1120 hasta değerlendirildi. Bu hastaların 401’i bilinen KAH öyküsü nedeniyle çalışma dışı bırakıldılar. Kalan 719 hastanın 601’inde koroner anjiyografide obstrüktif KAH saptandı. Geriye kalan 118 hastanın; 4’üne anjiyografi yapılmadı, 3’ü Takotsubo kardiyomiyopatisi tanısı aldı, 5’inde perikardiyal efüzyona bağlı atipik semptomlar gözlendi ve 2 hastada ise sonradan obstrüktif koroner lezyonlar saptandı. Bu hastalar da çalışma dışında bırakılınca MINOCA tanısı alan 104 hasta ile çalışma tamamlandı (Şekil 1).
Veriler, hastaların ilk başvurudaki tıbbi öykülerinden, hastane bilgi sisteminden ve hasta dosyalarından elde edildi. Analizlerde yalnızca başvuru sırasında ölçülen CRP düzeyleri kullanıldı.
MINOCA tanısı koymak için hastaların Mİ kriterlerini karşılaması, koroner arterlerinde normal ya da normale yakın (<%50 darlık) lezyon olması, önceden geçirilmiş Mİ veya koroner girişim öyküsü bulunmaması ve hastanede yatarak tedavi süresince herhangi bir girişim uygulanmamış olması gerekiyordu. Kritik darlık (%50 ve üzeri) tespit edilen hastalar obstrüktif KAH olarak sınıflandırılarak MINOCA grubundan çıkarıldılar. Önceki Mİ ya da koroner revaskülarizasyon öyküsü olan AKS hastaları, mevcut KAH’ın sonuçlar üzerindeki etkisini ortadan kaldırmak amacıyla çalışma dışı bırakıldılar.
Dahil Etme Kriterleri
Koroner anjiyografi sırasında ≥18 yaş olmak,
Yükselmiş miyokardiyal hasar biyobelirteçlerine (tercihen kardiyak troponinler) sahip AKS tanısı [ST segment elevasyonlu miyokart infarktüsü (ST-Elevation Myocardial Infarction, STEMI) veya ST segment elevasyonu olmayan miyokart infarktüsü (non-ST-Elevation Myocardial Infarction, NSTEMI)],
STEMI veya NSTEMI tanısı ile koroner anjiyografi yapılmış olmak,
Çalışmaya katılım için bilgilendirilmiş onam vermiş olmak.
Dışlama Kriterleri
Stabil koroner arter hastalığı için anjiyografik değerlendirme yapılan hastalar,
Enzim yüksekliği olmaksızın unstabil angina (unstable angina) değerlendirmesi yapılan hastalar,
Önceden koroner revaskülarizasyon [perkütan koroner girişimi (Percutaneous Coronary Intervention, PCI) veya koroner arter baypas greftleme cerrahisi (Coronary Artery Bypass Grafting, CABG)] öyküsü olanlar,
Stabil koroner hastalık için girişimsel tedavi sırasında AKS gelişen hastalar (“no-reflow”, stent trombozu, vb.),
Stabil KAH nedeniyle cerrahi tedavi sonrasında AKS gelişen hastalar,
Koroner anjiyografi sırasında <18 yaş olan hastalar,
Bilgilendirilmiş onam vermemiş olan hastalar.
Bu çalışmada hastalar kısa dönem klinik sonuçlar açısından takip edildi. Komplikasyonlar, yeniden hastaneye yatışlar ve mortalite gibi veriler takip süresince sistematik olarak kaydedildi. Eksik klinik veriler, T.C. Sağlık Bakanlığı’nın dijital sağlık kayıt sistemi olan e-Nabız üzerinden tamamlandı (18).
CRP Ölçümü
Bu çalışmada kullanılan CRP düzeyleri, hastaneye başvuru sırasında alınan kan örneklerinden elde edildi ve bu ölçümler hastane merkez laboratuvarında standart biyokimyasal yöntemlerle yapıldı.
İstatistiksel Analiz
İstatistiksel analizler, SPSS İstatistik Yazılımı Sürüm 27.0 (IBM Corp., Armonk, NY, ABD) kullanılarak gerçekleştirildi. Sürekli değişkenlerin normal dağılım varsayımı Kolmogorov-Smirnov testi ile değerlendirildi. Kategorik veriler sayı (n) ve yüzde (%); normal dağılım gösteren sürekli veriler ortalama ± standart sapma (SS), normal dağılım göstermeyen sürekli veriler ise medyan (25.–75. persentil) şeklinde sunuldu.
Kategorik değişkenler arasındaki ilişkiler Ki-kare testi, Fisher kesin testi veya Fisher-Freeman-Halton testi ile değerlendirildi. Sürekli ve kategorik değişkenlerin karşılaştırılmasında veri dağılımına göre Mann-Whitney U testi veya bağımsız örneklem t-testi kullanıldı.
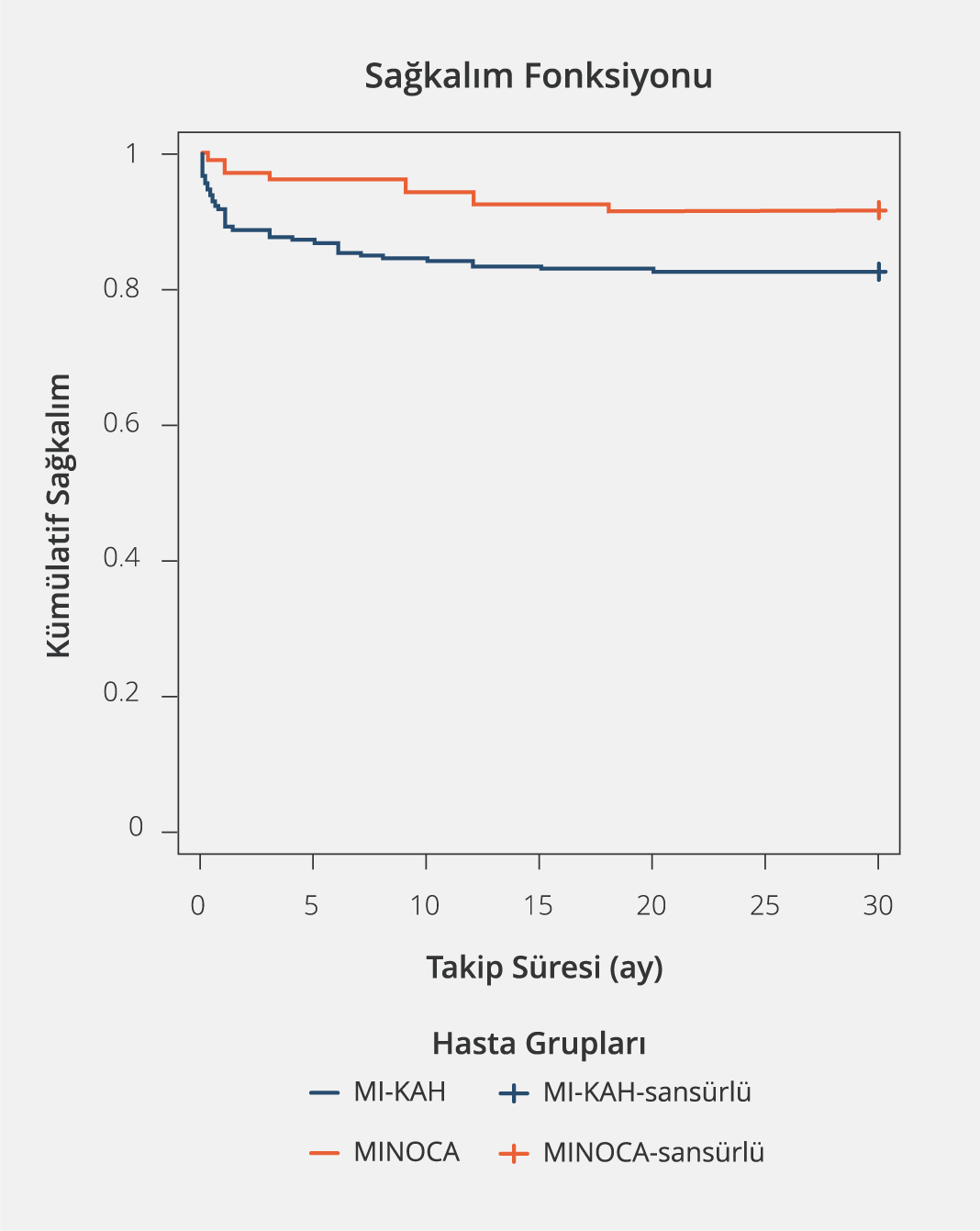
Sağkalım verileri %95 güven aralıkları ile sunuldu. Kategorik değişkenlerin sağkalım üzerine etkisi Kaplan-Meier analizi ile yapıldı ve anlamlılık log-rank testi ile değerlendirildi (Şekil 2). İstatistiksel anlamlılık düzeyi p<0.05 olarak kabul edildi.
C-reaktif protein düzeyleri ile MINOCA ve obstrüktif koroner arter hastalığına bağlı miyokart infarktüsü (Myocardial Infarction due to Obstructive Coronary Artery Disease, MI-CAD) hastalarında klinik değişkenler arasındaki ilişkiyi araştırmak için Nagelkerke R² modelleme çerçevesinde aşağıdaki çok değişkenli lojistik regresyon modelleri uygulandı (Tablo 5):
Model 1: Yaş, cinsiyet ve hasta grubu.
Model 2: Model 1 + kronik hastalık öyküsü + sigara kullanımı.
Model 3: Model 2 + hastanede kalış süresi.
MINOCA grubunda infeksiyöz komplikasyonların daha sık görülmesi ve bazal CRP düzeylerinin daha yüksek olması nedeniyle CRP düzeyi her modelde karıştırıcı değişken (confounder) olarak modele dahil edildi.
BULGULAR
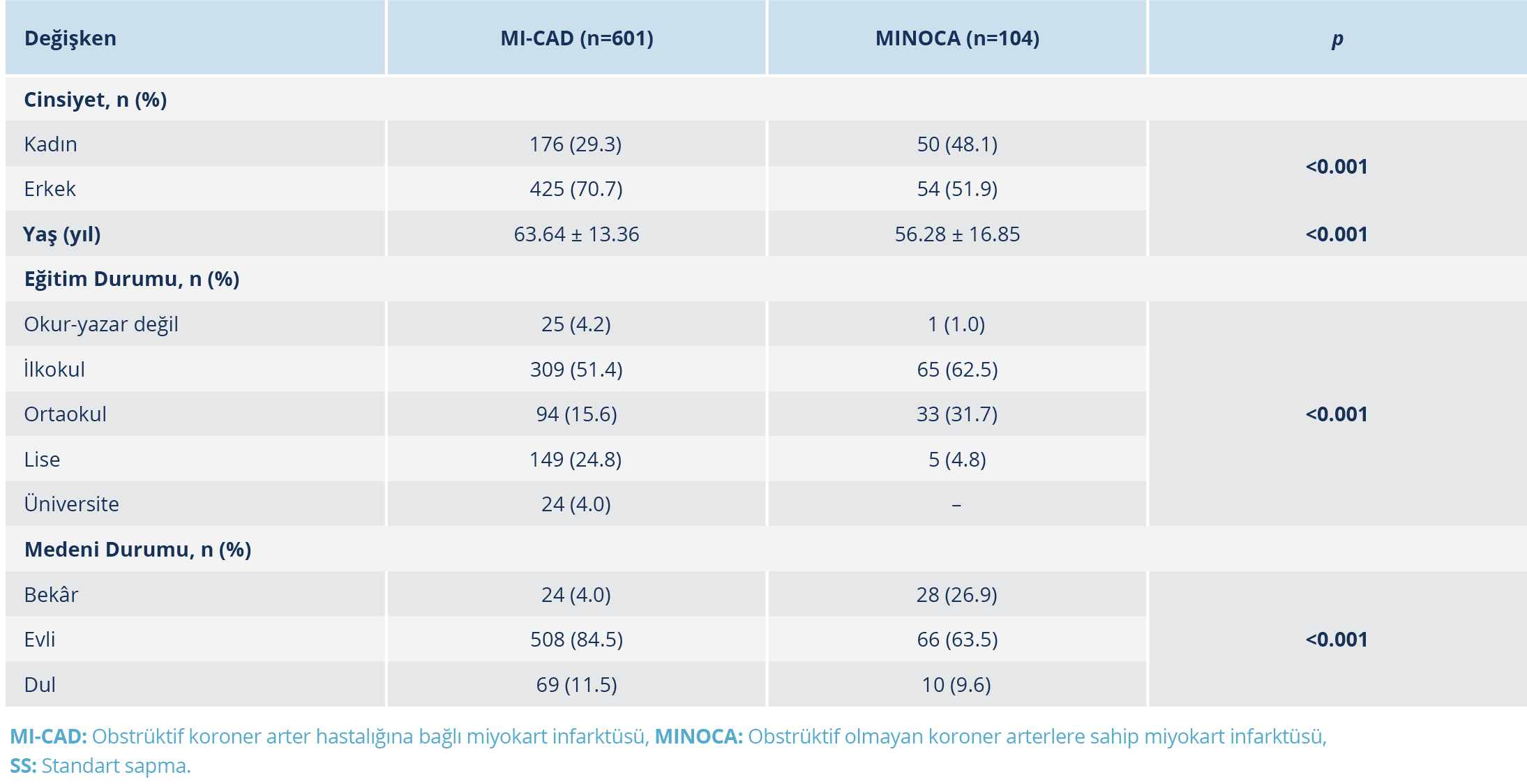
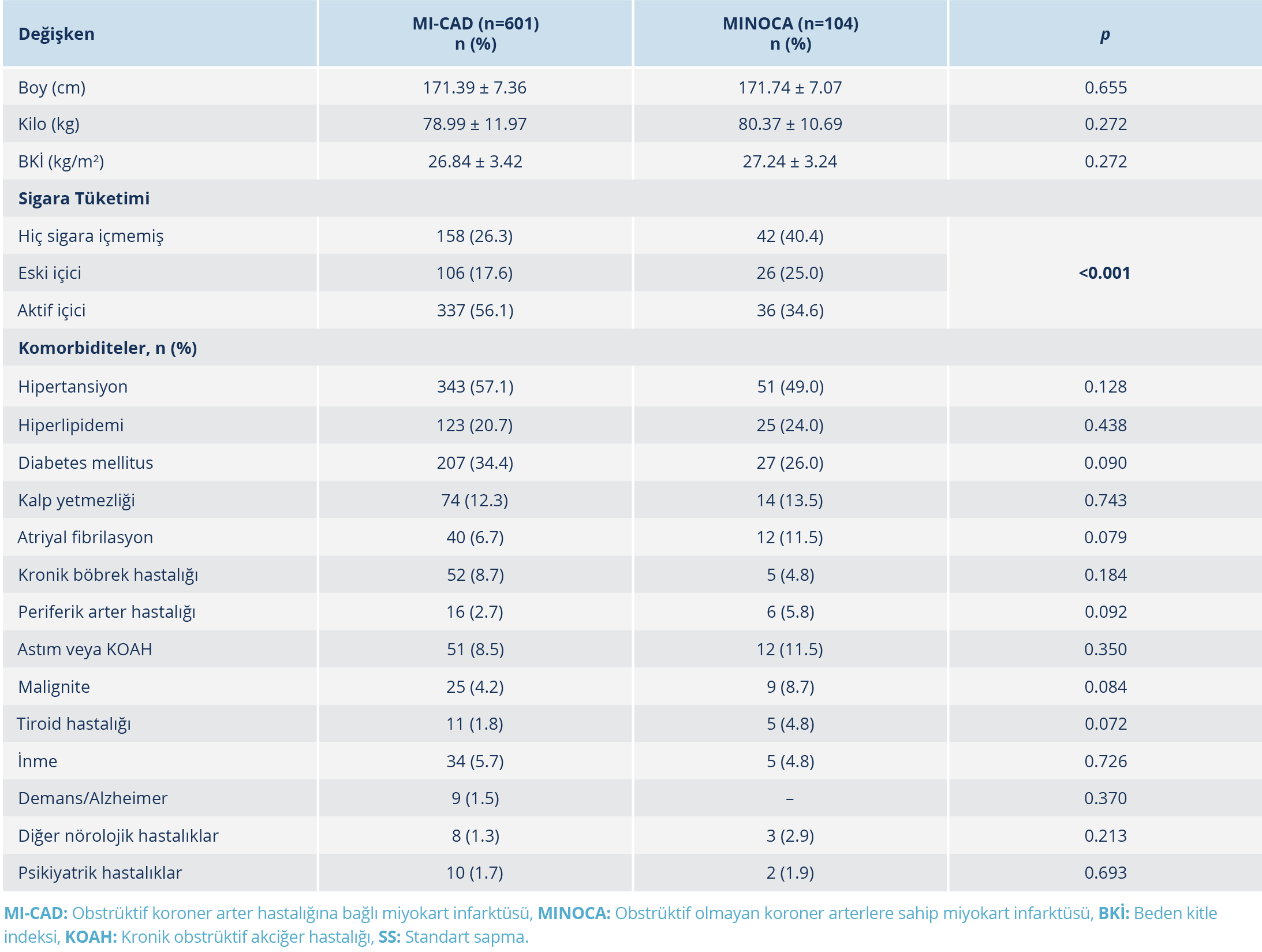
Bu çalışmada 104 MINOCA ve 601 MI-CAD hastası değerlendirildi (Tablo 1 ve Tablo 2). Başvuru anındaki medyan CRP düzeyi MINOCA grubunda 3.0 (1.0–9.0) mg/dl iken MI-CAD grubunda 0.7 (0.3–2.3) mg/dl saptandı (p<0.001). Bu sonuç, MINOCA grubunda CRP düzeylerinin anlamlı olarak daha yüksek olduğunu göstermektedir (Tablo 3).
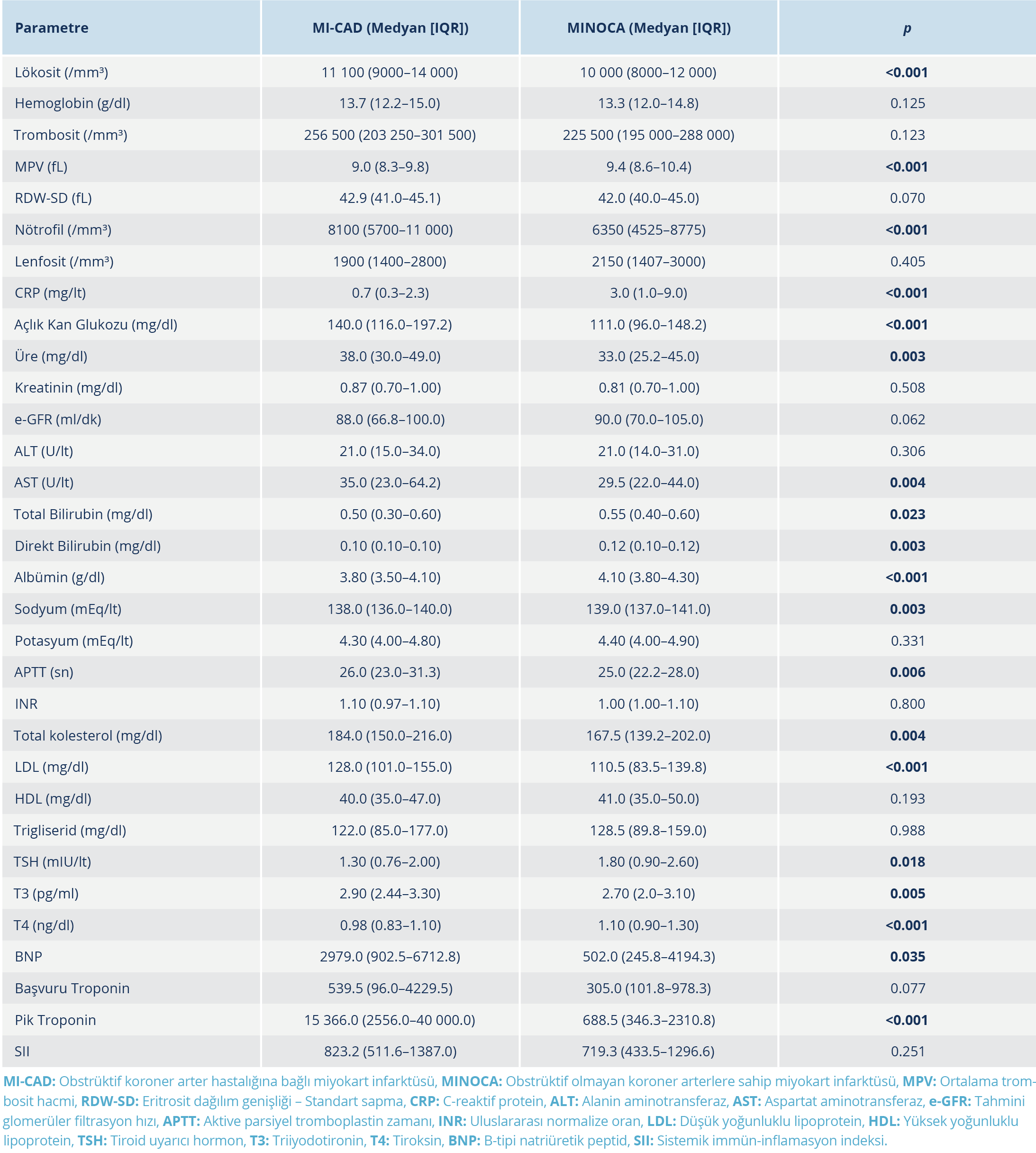
Laboratuvar parametreleri karşılaştırıldığında; ortalama trombosit hacmi (MPV) (p<0.001), albümin (p<0.001), sodyum (p=0.003), T4 (p<0.001) ve direkt bilirubin (p=0.003) düzeylerinin MINOCA grubunda anlamlı olarak daha yüksek olduğu saptandı. Buna karşılık, lökosit (p<0.001), nötrofil (p<0.001), açlık glukozu (p<0.001), üre (p=0.003), AST (p=0.004), total kolesterol (p=0.004), LDL (p<0.001), T3 (p=0.005), BNP (p=0.035) ve pik troponin (p<0.001) düzeyleri MINOCA grubunda MI-CAD grubuna kıyasla daha düşüktü.
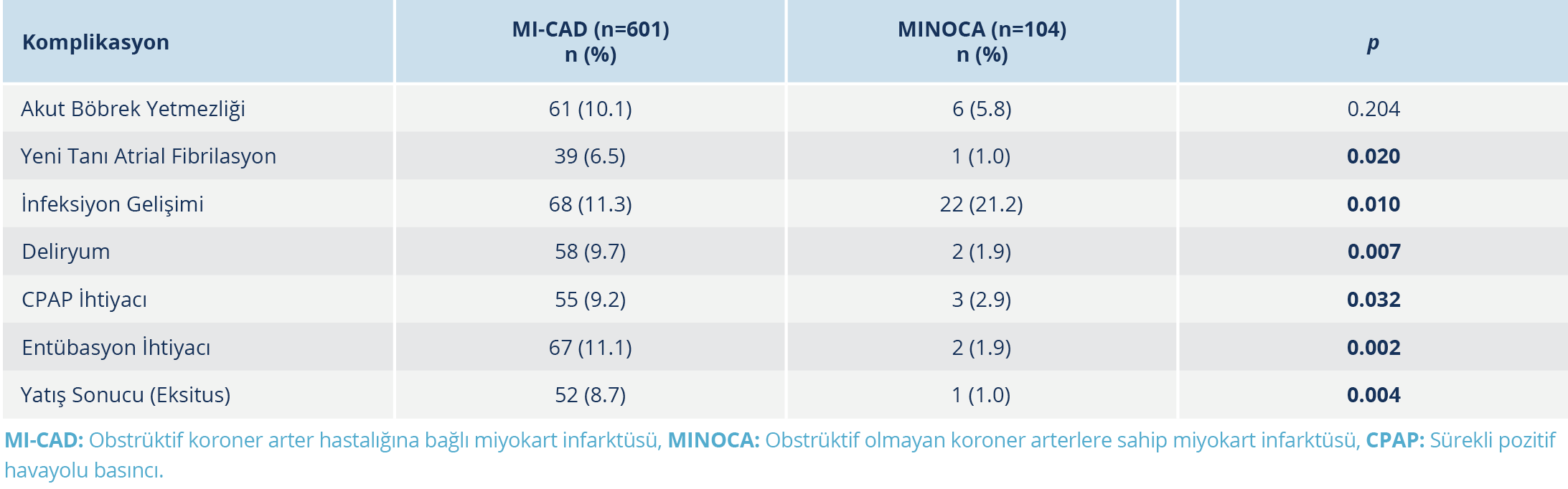
Tablo 4. MI-CAD ve MINOCA Gruplarında Hastane Yatışı Sırasında Gelişen Komplikasyonların Dağılımı ve İstatistiksel Karşılaştırması
Hastane içi komplikasyonlar açısından, infeksiyon sıklığı MINOCA grubunda %21.2; MI-CAD grubunda ise %11.3 olarak bulundu (p=0.010). MINOCA grubunda başvuru sırasında CRP düzeylerinin daha yüksek olmasına rağmen infeksiyon oranlarının hastane yatışı süresince de artmaya devam ettiği gözlendi. Yeni gelişen atriyal fibrilasyon (p=0.020), deliryum (p=0.007), sürekli pozitif hava yolu basıncı (Continuous Positive Airway Pressure, CPAP) ihtiyacı (p=0.032), entübasyon ihtiyacı (p=0.002) ve hastane içi mortalite (p=0.004) gibi diğer komplikasyonlar MI-CAD grubunda daha yüksek orandaydı (Tablo 4).
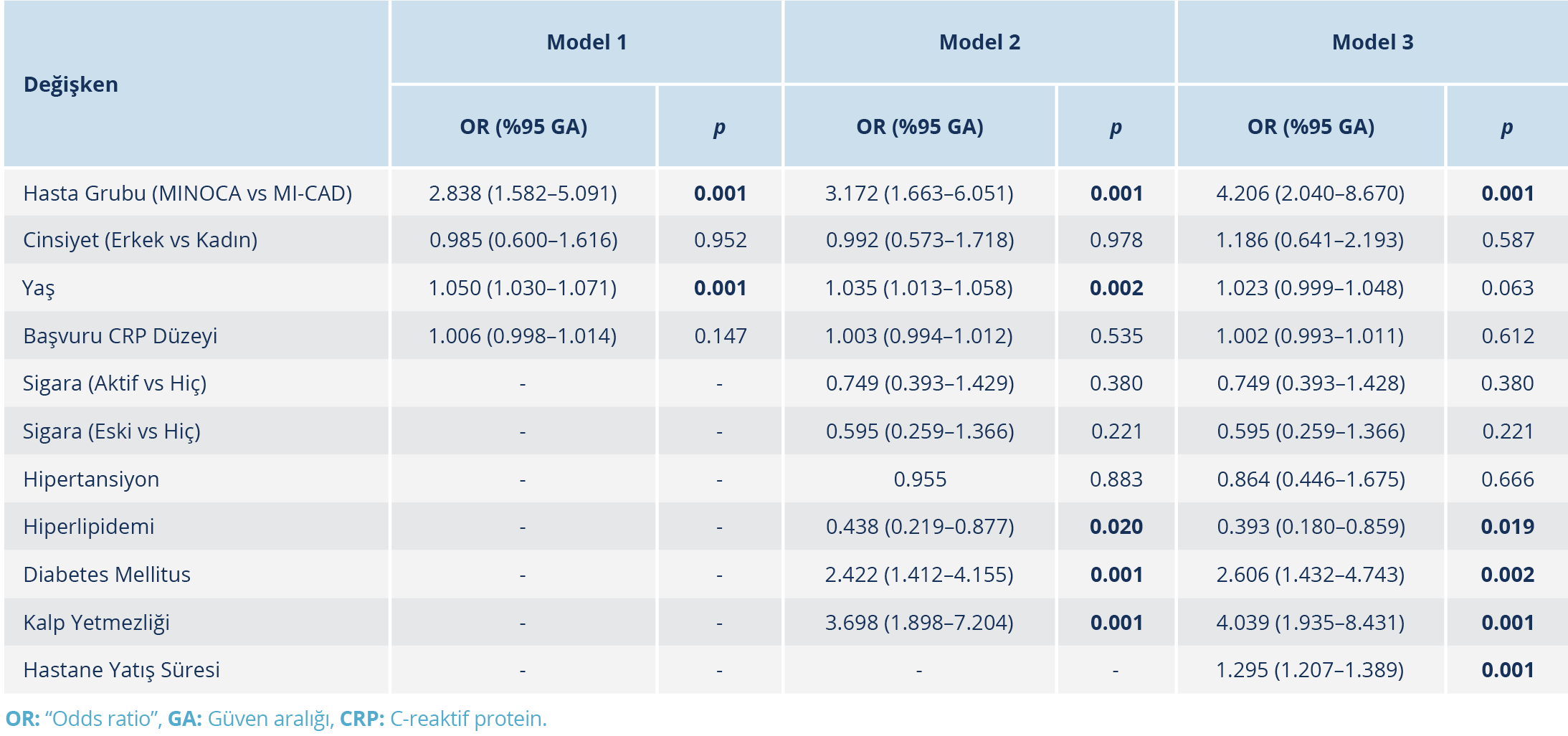
Çok değişkenli lojistik regresyon analizine göre, MINOCA grubu, infeksiyon açısından bağımsız bir risk faktörü olarak belirlendi. Model 1’de “odds ratio” (OR) 2.838 (%95 GA: 1.582–5.091; p=0.001), Model 2’de OR 3.172 (%95 GA: 1.663–6.051; p=0.001) ve Model 3’te OR 4.206 (%95 GA: 2.040–8.670; p=0.001) idi (Tablo 5). Üç modelde de CRP düzeyi karıştırıcı değişken olarak yer almasına rağmen, MINOCA grubu infeksiyon açısından bağımsız risk faktörü olarak kalmaya devam etti.
Model 3’te hastanede kalış süresi (OR 1.295; %95 GA: 1.207–1.389; p=0.001), diabetes mellitus (OR 2.606; %95 GA: 1.432–4.743; p=0.002) ve kalp yetersizliği (OR 4.039; %95 GA: 1.935–8.431; p=0.001) infeksiyon gelişimi ile anlamlı şekilde ilişkili bulundu. Buna karşılık, hiperlipidemi varlığının infeksiyon açısından koruyucu bir faktör olabileceği değerlendirildi (OR 0.393; %95 GA: 0.180–0.859; p=0.019) (Tablo 5).
Bu bulgular hem CRP düzeylerinin hem de hastanede kalış süresinin infeksiyon gelişimi ile ilişkili olabileceğini, ancak MINOCA grubunun bu parametrelerden bağımsız olarak sürekli yüksek infeksiyon riski taşıdığını göstermektedir.
İRDELEME
Çalışmamızda MINOCA hastalarında hastane içi infeksiyon gelişim oranları ve bu durumla ilişkili klinik faktörler değerlendirildi. Bulgularımız, MINOCA grubunda infeksiyon gelişiminin MI-CAD hastalarına kıyasla anlamlı derecede daha sık olduğunu ortaya koydu. Başvuru anındaki CRP düzeylerinin MINOCA grubunda daha yüksek bulunması, bu hastalarda farklı bir inflamatuar ve immün yanıt profili olabileceğini göstermektedir. Bu sonuçlar, MINOCA’nın yalnızca iskemik bir süreçten ibaret olmayıp sistemik inflamatuar süreçlerle de ilişkili olabileceğini düşündürmektedir. Bu durum, MINOCA’nın yalnızca epikardiyal koroner akım bozukluklarıyla değil, mikrovasküler inflamasyon, endotel disfonksiyonu ve immün yanıt farklılıklarıyla da ilişkili olabileceğini desteklemektedir. Elde edilen bulgular, MINOCA hastalarının yalnızca kardiyovasküler riskler açısından değil, aynı zamanda infeksiyon eğilimi bakımından da yakından izlenmesi gerektiğini göstermektedir.
Çalışmamızda, MINOCA grubunda anlamlı şekilde yüksek bulunan CRP düzeyleri, bu hastalarda sistemik inflamasyonun daha belirgin olduğunu ortaya koymaktadır. Daha önce yapılan çalışmalar da benzer şekilde CRP gibi inflamatuar belirteçlerin MINOCA’da prognostik değere sahip olduğunu göstermiştir. Ciliberti ve arkadaşlarının (13) çalışmasında yüksek CRP düzeylerinin MINOCA hastalarında olumsuz olaylarla ilişkili olduğu bildirilmiştir. Jia ve arkadaşları (19) ise sistemik inflamasyonun majör kardiyak olaylarla bağımsız olarak ilişkili olduğunu ve CRP’nin klinik seyri öngörmede etkili olduğunu bildirmiştir.
İnflamasyon, AKS gelişiminde kilit rol oynamaktadır. Sitokin salınımı (IL-1β, TNF-α, vb.), makrofaj aktivasyonu ve endotel disfonksiyonu gibi süreçler plak rüptürü ve tromboza zemin hazırlayabilir (20). Yüksek duyarlılıklı CRP ve sistemik inflamasyon indeksleri [Sistemik İmmün-İnflamasyon İndeksi (Systemic Immune-Inflammation Index, SII), Sistemik İnflamasyon Yanıt İndeksi (Systemic Inflammation Response Index, SIRI), vb.] AKS hastalarında yaygın olarak kabul gören prognostik belirteçlerdir (21). Son veriler, başvuru anındaki inflamatuar biyobelirteç düzeylerinin uzun dönem kardiyovasküler mortaliteyle ilişkili olduğunu göstermektedir (22).
Obstrüktif KAH bulunmasa da MINOCA olgularında farklı inflamatuar mekanizmalar rol oynayabilir. Güncel çalışmalar, perikardiyal yağ dokusu inflamasyonu (perikoroner yağ zayıflaması) gibi lokal inflamatuar süreçler ve sistemik inflamasyon indekslerinin [SII, SIRI, monosit / HDL oranı (Monocyte-to-HDL Ratio, MHR), vb.] olumsuz kardiyovasküler sonuçlarla ilişki olduğunu göstermektedir (23,24). Bu bulgular, MINOCA’daki inflamasyonun rastlantısal olmayıp patofizyolojik sürecin bir parçası olduğunu düşündürmektedir (25).
Çalışmamızda, hastane içi infeksiyon sıklığı MINOCA grubunda anlamlı olarak daha yüksek bulundu ve çok değişkenli lojistik regresyon analizlerinde de MINOCA grubunun infeksiyon için bağımsız bir risk faktörü olduğu görüldü. Bu durum; immün-inflamatuar dengesizlik, mikrovasküler disfonksiyon, doku hipoperfüzyonu, komorbiditeler ve tedaviyle ilişkili faktörler gibi birden fazla mekanizma ile ilişkili olabilir. Söz konusu mekanizmalar birlikte değerlendirildiğinde, MINOCA hastalarında inflamasyonun yalnızca patofizyolojik sürecin bir bileşeni değil, aynı zamanda sekonder infeksiyon riskini artıran bir unsur olabileceği öngörülebilir. MINOCA grubunda gözlenen yüksek infeksiyon oranları, bu hastalarda erken tanısal farkındalık ve yakın klinik izlem gerekliliğini göstermektedir. Özellikle diyabet, kalp yetersizliği veya uzun hastane yatışı olan hastalarda profilaktik önlemler, hijyen uygulamalarının güçlendirilmesi ve uygun durumlarda erken antibiyotik başlanması multidisipliner bir yaklaşım gerektirmektedir.
Çalışmamız, MINOCA hastalarında infeksiyon riskinin değerlendirilmesine odaklanan az sayıdaki prospektif analizden biridir. Zhou ve arkadaşlarının (26) çalışmasında MINOCA hastalarında inflamatuar biyobelirteçlerin [nötrofil / lenfosit oranı (neutrophil-to-lymphocyte ratio, NLR), SII, CRP] yüksekliğinin majör kardiyak olaylarla ilişkili olduğu bildirilmiştir. Diau ve arkadaşlarının (27) çalışması ise obstrüktif lezyon bulunmayan hastalarda koroner inflamasyonun kardiyovasküler olaylardan bağımsız olarak mortaliteyle ilişkili olduğunu göstermiştir. Bizim çalışmamız, bu bulgulara ek olarak infeksiyon sıklığının da arttığını ortaya koymakta ve MINOCA’nın sistemik inflamasyon ile immün disfonksiyonun kesiştiği özgün bir klinik tablo olabileceğine işaret etmektedir.
Ayrıca, diabetes mellitus, kalp yetersizliği ve uzamış hastane yatışı infeksiyon gelişimiyle anlamlı şekilde ilişkili bulundu. Nedensellik tam olarak açıklanamasa da bu değişkenlerin inflamasyon ve immün yanıt ile etkileşim içinde olabileceği düşünülebilir. Dikkat çekici bir şekilde, hiperlipidemi varlığı infeksiyon riskini azaltıcı bir etki göstermiştir. Bu bulgu, statin tedavisinin antiinflamatuar özellikleri ile uyumludur (28). Ridker ve arkadaşlarının (29) yürüttüğü “Justification for the Use of Statins in Prevention: An Intervention Trial Evaluating Rosuvastatin” (JUPITER) çalışmasında da yüksek CRP düzeyine sahip hastalarda statin kullanımının fayda sağladığı gösterilmiştir. Önceki çalışmalarda, CRP düzeylerinin 2–10 mg/lt aralığında olmasının kardiyovasküler riskle ilişkili olduğu bildirilmiştir (30). Bizim çalışmamızda da MINOCA hastalarının CRP düzeylerinin bu risk aralığında olduğu görüldü.
Her ne kadar MINOCA hastaları, MI-CAD hastalarına kıyasla genel olarak daha iyi bir klinik profile sahip olarak değerlendirilebilse de güncel veriler MINOCA’nın benign bir durum olmadığını göstermektedir (31). Çalışmamızda hastane içi mortalite oranı MI-CAD grubunda %8.7 iken MINOCA grubunda %1.0 idi. Kaplan-Meier sağkalım analizine göre, MINOCA grubunda ortalama sağkalım süresi 28.03 ay (%95 GA: 26.75–29.30) iken MI-CAD grubunda 25.23 ay (%95 GA: 24.39–26.06) olarak bulundu (p=0.020). Bu sonuçlar, obstrüktif lezyon olmamasına rağmen MINOCA hastalarının orta vadeli sağkalım açısından daha iyi sonuçlara sahip olabileceklerini düşündürmektedir.
Bununla birlikte, bir yıllık takip verilerinde tekrarlayan Mİ ve mortalite açısından gruplar arasında anlamlı bir fark izlenmedi. Bu durum, MINOCA hastalarının kardiyovasküler risklerinin devam ettiğini göstermektedir. Ayrıca, çalışmamızda MINOCA grubunda kardiyak dışı nedenlerle hastaneye yeniden yatış oranlarının daha yüksek olduğu saptandı. Bu bulgular, MINOCA hastalarında komorbiditelerin etkisinin önemli olduğunu göstermektedir. Dolayısıyla MINOCA hastalarının yönetiminde kapsamlı tanısal değerlendirme, bireyselleştirilmiş risk sınıflandırması ve mikrovasküler disfonksiyon, vazospazm ve inflamasyon gibi altta yatan mekanizmaların göz önünde bulundurulması gereklidir. MINOCA’nın heterojen doğası (örneğin spontan koroner arter diseksiyonu, koroner vazospazm, mikrovasküler disfonksiyon) nedeniyle inflamasyonun rolü daha ayrıntılı araştırılmalıdır.
Çalışmamızın tek merkezli olması, sonuçların genellenebilirliğini sınırlamaktadır. Ayrıca optik koherens tomografi, intravasküler ultrasonografi ve kardiyak manyetik rezonans görüntüleme gibi ileri görüntüleme yöntemlerinin kullanılmamış olması da önemli bir sınırlılıktır. Bu yöntemleri içeren çalışmaların yapılması, inflamasyon ile MINOCA’nın altta yatan patofizyolojik mekanizmaları arasındaki ilişkinin daha net ortaya konulmasını sağlayabilir. Öte yandan CRP ölçümlerinin yalnızca başvuru sırasında yapılmış olması, zaman içindeki değişimlerin ve uzun dönem takip sonuçlarının değerlendirilememesine yol açmıştır. Bu nedenle, CRP’nin zaman içindeki prognostik değerinin yeni çalışmalarda araştırılmasının önemli olduğunu düşünüyoruz.
Bu çalışma, MINOCA tanısı alan hastalarda başvuru anındaki CRP düzeylerinin MI-CAD hastalarına kıyasla anlamlı ölçüde daha yüksek olduğunu ve hastane yatışı süresince infeksiyöz komplikasyonların daha sık geliştiğini gösterdi. Bu bulgular, MINOCA’nın farklı bir inflamatuar profile sahip olabileceğini ve bunun hem klinik tabloya hem de hastalığın prognozuna katkıda bulunabileceğini düşündürmektedir. Elde edilen sonuçlar, MINOCA hastalarında inflamatuar parametrelerin yakından izlenmesinin önemini vurgulamakta ve inflamatuar mekanizmaların hastalığın patofizyolojisinde önceki değerlendirmelere kıyasla daha merkezi bir rol oynayabileceğini göstermektedir. Bu nedenle, MINOCA’nın yönetiminde daha bireyselleştirilmiş tanısal ve tedavi yaklaşımlarının benimsenmesi gerektiğini düşünüyoruz. Sonuç olarak; inflamasyonun MINOCA etiyopatogenezindeki yerinin daha net ortaya konulabilmesi için çok merkezli, geniş hasta popülasyonlarını içeren ve kapsamlı tanısal yöntemlerle desteklenmiş ileri araştırmalara ihtiyaç bulunmaktadır.
Hasta Onamı
Çalışmaya katılan tüm hastalardan bilgilendirilmiş gönüllü onam alınmıştır.
Etik Kurul Kararı
Bu çalışma için Trakya Üniversitesi Tıp Fakültesi Bilimsel Araştırmalar Etik Kurulu’ndan 16 Eylül 2019 tarih ve TUTF–BAEK–2019/343 karar numarasıyla onay alınmıştır.
Danışman Değerlendirmesi
Bağımsız dış danışman
Yazar Katkıları
Fikir/Kavram – M.D., S.A.; Tasarım – M.D., S.A.; Denetleme – M.D., S.A.; Malzemeler/Hastalar – M.D., S.A.; Veri Toplama ve/veya İşleme – M.D., S.A.; Analiz ve/veya Yorum – M.D., S.A.; Literatür Taraması – M.D., S.A.; Makale Yazımı – M.D., S.A.; Eleştirel İnceleme – M.D., S.A.
Çıkar Çatışması
Yazarlar herhangi bir çıkar çatışması bildirmemiştir.
Finansal Destek
Yazar finansal destek beyan etmemiştir.
Tez: Demir M. Obstrüktif koroner arterler veya non-obstrüktif koroner arterler ile beraber miyokard enfarktüsü geçiren hastaların klinik ve ekokardiyografik özellikleri ile kısa dönem prognozlarının karşılaştırılması [Uzmanlık tezi]. Edirne: Trakya Üniversitesi Tıp Fakültesi, Kardiyoloji Anabilim Dalı; 2023. Danışman: Prof. Dr. Servet Altay.
Referanslar
- Agewall S, Beltrame JF, Reynolds HR, et al; WG on Cardiovascular Pharmacotherapy. ESC working group position paper on myocardial infarction with non-obstructive coronary arteries. Eur Heart J. 2017;38(3):143-53. [CrossRef]
- Yildiz M, Ashokprabhu N, Shewale A, Pico M, Henry TD, Quesada O. Myocardial infarction with non-obstructive coronary arteries (MINOCA). Front Cardiovasc Med. 2022;9:1032436. [CrossRef]
- Thygesen K, Alpert JS, Jaffe AS, et al; Executive Group on behalf of the Joint European Society of Cardiology (ESC)/American College of Cardiology (ACC)/American Heart Association (AHA)/World Heart Federation (WHF) Task Force for the Universal Definition of Myocardial Infarction. Fourth universal definition of myocardial infarction (2018). Circulation. 2018;138(20):e618-51. Erratum in: Circulation. 2018;138(20):e652. [CrossRef]
- Özkan U, Kayıkçıoğlu M, Altay S. Ferroptosis: A novel paradigm in the pathophysiology of MINOCA. Atherosclerosis. 2025;402:119097. [CrossRef]
- Öztürk C, Taylan G, Ustabaşıoğlu FE, Ege T. Is MINOCA syndrome causing fatal left ventricular aneurysms less innocent than it appears? Balkan Med J. 2025;42(3):274-5. [CrossRef]
- Yılmaz E, Vurucu U, Karahan F, Öztürk C. A life-threatening focal refractory vasospasm: Is stenting the last or first option? Inter Cardio Pers. 2025;1(1):32-4. [CrossRef]
- Pasupathy S, Air T, Dreyer RP, Tavella R, Beltrame JF. Systematic review of patients presenting with suspected myocardial infarction and nonobstructive coronary arteries. Circulation. 2015;131(10):861-70. Erratum in: Circulation. 2015;131(19):e475. [CrossRef]
- Occhipinti G, Bucciarelli-Ducci C, Capodanno D. Diagnostic pathways in myocardial infarction with non-obstructive coronary artery disease (MINOCA). Eur Heart J Acute Cardiovasc Care. 2021;10(7):813-22. [CrossRef]
- Bakhshi H, Gibson CM. MINOCA: Myocardial infarction no obstructive coronary artery disease. Am Heart J Plus. 2023;33:100312. [CrossRef]
- Scalone G, Niccoli G, Crea F. Editor’s Choice- Pathophysiology, diagnosis and management of MINOCA: an update. Eur Heart J Acute Cardiovasc Care. 2019;8(1):54-62. [CrossRef]
- Yalta K, Madias JE, Kounis NG, et al. Takotsubo syndrome: An international expert consensus report on practical challenges and specific conditions (Part-2: Specific entities, risk stratification and challenges after recovery). Balkan Med J. 2024;41(6):442-57. [CrossRef]
- Yalta K, Madias JE, Kounis NG, et al. Takotsubo syndrome: An international expert consensus report on practical challenges and specific conditions (Part-1: Diagnostic and therapeutic challenges). Balkan Med J. 2024;41(6):421-41. [CrossRef]
- Ciliberti G, Coiro S, Tritto I, et al. Predictors of poor clinical outcomes in patients with acute myocardial infarction and non-obstructed coronary arteries (MINOCA). Int J Cardiol. 2018;267:41-5. [CrossRef]
- Kong M, Pei Z, Xie Y, Gao Y, Li J, He G. Prognostic factors of MINOCA and their possible mechanisms. Prev Med Rep. 2024;39:102643. [CrossRef]
- Eggers KM, Baron T, Hjort M, Nordenskjöld AM, Tornvall P, Lindahl B. Clinical and prognostic implications of C-reactive protein levels in myocardial infarction with nonobstructive coronary arteries. Clin Cardiol. 2021;44(7):1019-27. [CrossRef]
- Fedele D, Cavallo D, Bodega F, et al. Pathological findings at invasive assessment in MINOCA: A systematic review and meta-analysis. Heart. 2025;111(7):291-9. [CrossRef]
- Khorasani N, Mohammadi Y, Sarpoli M, Kazemi T, Riahi SM. Understanding Myocardial Infarction with Non-Obstructive Coronary Arteries (MINOCA): A comprehensive meta-analysis of clinical characteristics, management, and prognosis compared to MI with the Obstructive Coronary Artery (MIOCA). BMC Cardiovasc Disord. 2025;25(1):143. [CrossRef]
- Birinci Ş. A Digital opportunity for patients to manage their health: Turkey National Personal Health Record System (The e-Nabız). Balkan Med J. 2023;40(3):215-21. Erratum in: Balkan Med J. 2023;40(4):307. [CrossRef]
- Jia F, Fei SF, Tong DB, Zhang S, Li JJ. Do patients with myocardial infarction with non-obstructive coronary arteries have similar prognosis compared to ones with MI-CAD? Angiology. 2023;74(5):407-16. [CrossRef]
- Altay S, Çakmak HA, Kemaloğlu Öz T, et al. Long-term prognostic significance of pentraxin-3 in patients with acute myocardial infarction: 5-year prospective cohort study. Anatol J Cardiol. 2017;17(3):202-9. [CrossRef]
- Odeberg J, Halling A, Ringborn M, et al. Markers of inflammation predicts long-term mortality in patients with acute coronary syndrome – a cohort study. BMC Cardiovasc Disord. 2025;25(1):190. [CrossRef]
- Libby P, Pasterkamp G, Crea F, Jang IK. Reassessing the mechanisms of acute coronary syndromes. Circ Res. 2019;124(1):150-60. [CrossRef]
- Chen YD, Wen ZG, Long JJ, Wang Y. Association between systemic inflammation response index and slow coronary flow phenomenon in patients with ischemia and no obstructive coronary arteries. Int J Gen Med. 2024;17:4045-53. [CrossRef]
- Özkan U, Gürdoğan M, Öztürk C, et al. Systemic Immune-Inflammation Index: a novel predictor of coronary thrombus burden in patients with non-ST acute coronary syndrome. Medicina (Kaunas). 2022;58(2):143. [CrossRef]
- Ciliberti G, Bergamaschi L, Armillotta M, Angeli F, Pizzi C. MINOCA and inflammation: Another piece of the puzzle. Int J Cardiol. 2025;419:132724. [CrossRef]
- Zhou H, Li X, Wang W, et al. Immune-inflammatory biomarkers for the occurrence of MACE in patients with myocardial infarction with non-obstructive coronary arteries. Front Cardiovasc Med. 2024;11:1367919. [CrossRef]
- Diau JL, Lange RA. Coronary inflammation and cardiovascular events in patients without obstructive coronary artery disease. Curr Cardiol Rep. 2025;27(1):68. [CrossRef]
- Koushki K, Shahbaz SK, Mashayekhi K, et al. Anti-inflammatory action of statins in cardiovascular disease: the role of inflammasome and toll-like receptor pathways. Clin Rev Allergy Immunol. 2021;60(2):175-99. [CrossRef]
- Ridker PM, Danielson E, Fonseca FA, et al; JUPITER Study Group. Rosuvastatin to prevent vascular events in men and women with elevated C-reactive protein. N Engl J Med. 2008;359(21):2195-207. [CrossRef]
- Pearson TA, Mensah GA, Alexander RW, et al; Centers for Disease Control and Prevention; American Heart Association. Markers of inflammation and cardiovascular disease: application to clinical and public health practice: A statement for healthcare professionals from the Centers for Disease Control and Prevention and the American Heart Association. Circulation. 2003;107(3):499-511. [CrossRef]
- Sykes R, Doherty D, Mangion K, Morrow A, Berry C. What an interventionalist needs to know about MI with non-obstructive coronary arteries. Interv Cardiol.;16:e10. [CrossRef]